Коррозия металлов и создание жаростойких и жаропрочных сталей и сплавов: классификация и свойства
Разрушение металла под воздействием окружающей среды называют коррозией. Этот процесс не только приводит к безвозвратной потере металла, но и крайне отрицательно влияет на эксплуатационные характеристики деталей, способствуя развитию усталостных трещин и других видов разрушения. Понимание механизмов коррозии является основой для создания долговечных и надежных металлических конструкций, работающих в различных условиях — от агрессивных химических сред до высокотемпературных газовых потоков.
В зависимости от характера окружающей среды различают два основных типа коррозии: химическую и электрохимическую. Электрохимическая коррозия имеет место в водных растворах электролитов, а также в обычной атмосфере, где присутствует влага, конденсирующаяся на поверхности металла. Сущность этого процесса заключается в том, что положительно заряженные ионы металла на поверхности детали, имея слабую связь с кристаллической решеткой, легко отрываются и гидратируются молекулами воды, переходя в раствор.
Металл, потеряв часть положительно заряженных частиц, заряжается отрицательно за счет избыточного количества оставшихся электронов. Одновременно прилегающий к металлу слой воды обогащается ионами металла и приобретает положительный заряд. Возникающая на границе металл-электролит разность потенциалов определяет скорость коррозионного процесса. Если количество ионов, переходящих в раствор, равно количеству ионов, осаждающихся из раствора на металле, устанавливается динамическое равновесие, и процесс разрушения металла прекращается. Этому состоянию соответствует так называемый равновесный потенциал.
За нулевую точку отсчета принят равновесный потенциал водородного электрода в водном растворе при концентрации ионов водорода, равной 1 моль/л. Стандартные электродные потенциалы всех других металлов измеряются и сравниваются именно с водородным потенциалом. Металлы, стандартный потенциал которых является отрицательным, будут корродировать в воде, содержащей растворенный кислород, причем их коррозионная активность тем выше, чем отрицательнее значение их электрохимического потенциала.
Уходящие в раствор ионы железа взаимодействуют с гидроксильными группами (OH⁻), образуя нерастворимые в воде гидроксиды, которые в совокупности называют ржавчиной, а сам процесс — ржавлением. Схема ржавления железа может быть представлена следующим образом: на анодных участках железо переходит в раствор в виде ионов Fe²⁺, а на катодных участках происходит восстановление кислорода, растворенного в воде, с образованием гидроксильных ионов. Взаимодействуя, эти ионы формируют гидроксид железа (II) — Fe(OH)₂. Однако в присутствии кислорода это соединение далее окисляется до гидроксида железа (III) — Fe(OH)₃, который, теряя воду, превращается в смесь оксидов и гидроксидов, известную как ржавчина. Поскольку эти соединения нерастворимы и не образуют на поверхности металла сплошной защитной пленки, равновесный потенциал не достигается, и коррозия продолжается вплоть до полного разрушения изделия.
В зависимости от структуры металла коррозия может проявляться по-разному. На однородном металле коррозионный процесс протекает равномерно по всей поверхности. Однако на неоднородном металле, содержащем включения, границы зерен или зоны с разным химическим составом, возникает избирательная (точечная) коррозия. Это явление наиболее опасно, так как локальные поражения (питтинги) создают очаги концентрации напряжений, которые служат инициаторами трещин и приводят к быстрому разрушению всего изделия при сохранении общей массы металла.
Химическая коррозия протекает при взаимодействии металла с газовой средой (кислородом, парами серы и др.) в условиях высоких температур и полного отсутствия влаги. Продуктом такой коррозии являются оксиды металла. На начальном этапе образуется тончайшая пленка толщиной в 1–2 периода кристаллической решетки. Если эта пленка сплошная, прочная и имеет коэффициент теплового расширения, близкий к металлу, она изолирует поверхность от дальнейшего контакта с газом, прекращая окисление. Такая оксидная пленка также способна защищать металл и от электрохимической коррозии в воде. Именно на этом принципе основано создание коррозионно-стойких сплавов: материал должен обладать повышенным электрохимическим потенциалом и быть по возможности однофазным, чтобы избежать образования гальванических пар.
Классификация коррозионно-стойких сталей и сплавов. Коррозионная стойкость стали может быть кардинально повышена двумя путями: сведением содержания углерода к минимуму или введением легирующего элемента, который, образуя с железом твердый раствор, скачкообразно повышает электродный потенциал сплава до положительных значений. Важнейшими коррозионно-стойкими техническими сплавами являются нержавеющие стали с повышенным содержанием хрома, которые подразделяются на хромистые и более сложнолегированные хромоникелевые.

Рис 20.1. Влияние хрома на потенциал сплавов Fe-Cr
На графике представлена зависимость электродного потенциала железохромистого сплава от содержания хрома. Видно, что при содержании хрома менее 12-13% потенциал сплава остается близким к потенциалу железа. При достижении пороговой концентрации (около 13% Cr) происходит резкое (скачкообразное) повышение потенциала до положительных значений, что и обеспечивает переход стали в пассивное состояние и придает ей коррозионную стойкость.
Хромистые стали. Для обеспечения коррозионной стойкости содержание хрома в таких сталях должно быть не менее 13% (обычно 13–18%). Высокая стойкость объясняется образованием на поверхности прочной и плотной защитной пленки оксида хрома (Cr₂O₃). Углерод в нержавеющих сталях является крайне нежелательным элементом, так как он, связывая хром в карбиды, обедняет им твердый раствор и способствует получению двухфазной структуры. Чем ниже содержание углерода, тем выше коррозионная стойкость стали.
Среди хромистых сталей выделяют несколько классов. Стали ферритного класса (08Х13, 12Х17, 08Х25Т, 15Х28) не имеют фазовых превращений в твердом состоянии и поэтому не упрочняются закалкой. Их существенным недостатком является повышенная хрупкость из-за склонности к росту крупного зерна при нагреве, а также склонность к межкристаллитной коррозии. Этот вид коррозии возникает из-за того, что хром по границам зерен взаимодействует с углеродом, образуя карбиды. Концентрация хрома в приграничных зонах твердого раствора падает ниже 13%, потенциал становится отрицательным, и границы начинают интенсивно растворяться. Для предотвращения этого явления в стали вводят небольшое количество титана, который связывает углерод в более прочные карбиды. Из-за склонности к росту зерна и охрупчиванию при 450–500°С ферритные стали требуют строгих режимов сварки. Из них изготавливают оборудование для азотно-кислотных заводов (емкости, трубы).
Для повышения механических свойств в ферритные стали добавляют 2–3% никеля (стали 10Х13Н3, 12Х17Н2). Эти материалы используются для тяжелонагруженных деталей, работающих в агрессивных средах. После закалки от 1000°С и высокого отпуска при 700–750°С их предел текучести достигает 1000 МПа. Термическая обработка ферритных сталей проводится для гомогенизации твердого раствора, что повышает коррозионную стойкость.
Стали мартенситного класса (20Х13, 30Х13, 40Х13) содержат больше углерода. После закалки и низкого отпуска при 180–250°С стали 30Х13 и 40Х13 приобретают высокую твердость (50–60 HRC) и используются для изготовления режущего инструмента (в том числе хирургического), пружин, работающих при 400–450°С, а также предметов домашнего обихода.
Хромоникелевые стали аустенитного класса. Наиболее высокой коррозионной стойкостью и лучшими технологическими свойствами обладают высоколегированные хромоникелевые стали. Никель, являясь сильным аустенитообразующим элементом, расширяет область существования аустенита, и после охлаждения на воздухе до комнатной температуры сталь сохраняет структуру аустенита (марки 04Х18Н10, 12Х18Н9Т). Эти стали превосходят хромистые по коррозионной стойкости, лучше свариваются, сохраняют прочность до более высоких температур, менее склонны к росту зерна и не теряют пластичности при криогенных температурах.
Для повышения гомогенности и растворения карбидов хрома аустенитные стали подвергают закалке с 1050–1100°С в воде. Быстрое охлаждение фиксирует структуру пересыщенного твердого раствора, обеспечивая высокую пластичность (относительное удлинение 35–45%). Упрочнение таких сталей достигается холодной пластической деформацией (наклепом), что позволяет повысить предел текучести до 1000–1200 МПа. Для экономии дефицитного никеля его частично заменяют марганцем и азотом (стали 40Х14Г14Н3Т, 10Х20Н4АГ11).
Аустенитно-ферритные и никелевые коррозионно-стойкие сплавы. Аустенитно-ферритные стали (12Х21Н5Т, 08Х22Н6Т) созданы как заменители чистых аустенитных сталей с целью экономии никеля. Их свойства зависят от соотношения фаз: оптимальный комплекс механических свойств и коррозионной стойкости достигается при равном соотношении феррита и аустенита (1:1). Эти стали не подвержены коррозионному растрескиванию под напряжением, так как ферритные участки эффективно тормозят распространение трещин, зарождающихся в аустените. Термическая обработка включает закалку от 1100–1150°С и последующий отпуск (старение) при 500–750°С.
Помимо сталей, в промышленности применяют коррозионно-стойкие сплавы на никелевой основе, например, сплавы типа хастеллой. Содержащие до 80% никеля и 15–30% молибдена, они сохраняют стойкость в особо агрессивных средах (кипящие фосфорная или соляная кислоты). После закалки и старения при 800°С эти сплавы демонстрируют высокие механические свойства. Их недостатком является склонность к межкристаллитной коррозии, поэтому содержание углерода в них должно быть минимальным.
Жаростойкость, жаростойкие стали и сплавы. Жаростойкость (окалиностойкость) — это способность металлов и сплавов сопротивляться газовой коррозии (химическому разрушению) при высоких температурах в течение длительного времени. Если изделие работает в окислительной среде при 500–550°С без значительных нагрузок (например, детали печной арматуры), то достаточно, чтобы материал обладал только жаростойкостью.
При температурах выше 570°С железо и низколегированные стали начинают интенсивно окисляться. Образующийся в этих условиях слой окалины содержит фазу вюстит (FeO) — оксид с простой кристаллической решеткой, имеющей дефицит атомов кислорода. Такая структура не является препятствием для диффузии ионов металла наружу, а кислорода — внутрь, поэтому процесс окисления протекает неконтролируемо, формируя толстый слой хрупкой окалины.
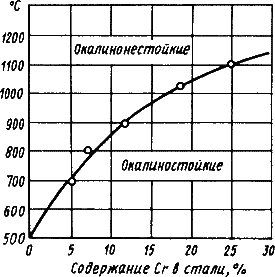
Рис. 20.2. Влияние хрома на жаростойкость хромистой стали
Диаграмма иллюстрирует, как увеличение концентрации хрома в стали влияет на температуру начала интенсивного окисления. Чем выше содержание хрома, тем при более высоких температурах сталь сохраняет способность сопротивляться газовой коррозии. Это связано с формированием на поверхности плотной, хорошо сцепленной с металлом пленки оксида хрома (Cr₂O₃), которая блокирует диффузию.
Для повышения жаростойкости в состав стали вводят элементы, образующие с кислородом плотные, труднопроницаемые оксиды: хром, кремний, алюминий. Степень легирования зависит от рабочей температуры. Например, сталь 15Х25Т, содержащая 25% хрома, является окалиностойкой до 1100–1150°С. Высокой жаростойкостью обладают сильхромы (хромокремнистые стали), сплавы на никелевой основе — нихромы, а также стали 08Х17Т, 36Х18Н25С2 и 15Х6СЮ.
Жаропрочность, жаропрочные стали и сплавы. Жаропрочность — это способность металла сопротивляться пластической деформации и разрушению при высоких температурах. Этот параметр критически важен для деталей, работающих в условиях, где наблюдается явление ползучести — медленной, непрерывной пластической деформации под действием постоянной нагрузки при высокой температуре.
Критериями оценки жаропрочности служат несколько показателей. Кратковременная прочность (σв) определяется при обычных испытаниях на растяжение образцов, нагретых до заданной температуры. Однако более важны характеристики длительной прочности. Пределом длительной прочности называется максимальное напряжение (σ), которое не вызывает разрушения образца при заданной температуре в течение определенного времени (например, σ 600°С/1000 = 200 МПа). Для котельных установок, рассчитанных на годы работы, требуются невысокие напряжения, но гарантия целостности в течение десятков тысяч часов.
Ползучесть — это свойство металла медленно и непрерывно деформироваться во времени при постоянных температуре и нагрузке. При обычных температурах и напряжениях ниже предела упругости ползучесть не наблюдается. Однако при температурах выше 0,6 Тпл (температуры плавления), когда становятся активными диффузионные процессы разупрочнения (возврат и рекристаллизация), ползучесть становится определяющим фактором.
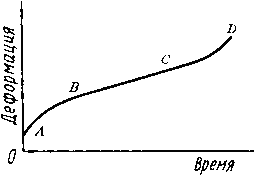
Рис. 20.3. Кривая ползучести
На графике представлена типичная кривая ползучести, отражающая зависимость деформации от времени при постоянных температуре и нагрузке. Участок ОА соответствует мгновенной упругой деформации при нагружении. На участке АВ (неустановившаяся ползучесть) скорость деформации постепенно замедляется. Участок ВС (установившаяся ползучесть) характеризуется постоянной минимальной скоростью деформации. Участок СД (третья стадия) соответствует ускорению ползучести и предшествует разрушению образца.
Для углеродистых сталей ползучесть становится заметной при нагреве выше 400°С. Предел ползучести — это напряжение, которое за определенное время при заданной температуре вызывает заданное суммарное удлинение или заданную скорость деформации (например, σ 600°С/0,2/100, где 0,2 — допустимое удлинение в процентах за 100 часов).
Классификация жаропрочных сталей и сплавов. Современные жаропрочные материалы включают широкий спектр классов: от недорогих перлитных сталей до сложнолегированных сплавов на основе никеля, кобальта и тугоплавких металлов. До 300°С обычно достаточно обычных конструкционных сталей.
В интервале 350–500°С применяют легированные стали перлитного класса. К ним относятся котельные стали и сильхромы, используемые для деталей паровых турбин и двигателей внутреннего сгорания. Они содержат мало углерода и легированы хромом, молибденом и ванадием (12Х1МФ, 20Х3МФ) для повышения температуры рекристаллизации. Используются в закаленном и высокоотпущенном состоянии. Перлитные стали хорошо свариваются и применяются для сварных конструкций (трубы пароперегревателей).
Для деталей газовых турбин, работающих при более высоких температурах, используют сложнолегированные стали мартенситного класса (12Х2МФСР, 15Х12ВНМФ). Повышенное содержание хрома придает им жаростойкость, а вольфрам, молибден и ванадий, образуя карбиды, дополнительно повышают жаропрочность. Термообработка включает закалку с температур выше 1000°С и высокий отпуск.
Для работы в диапазоне 500–700°С применяют стали аустенитного класса. Основой являются хромоникелевые стали (15–20% Cr, 10–20% Ni), дополнительно легированные вольфрамом, молибденом, ванадием (37Х12Н8Г8МФБ, 10Х11Н20Т3Р). Они пластичны, хорошо свариваются, но сложны в механической обработке. Их жаропрочность повышают путем дисперсионного твердения: после закалки проводят старение при 600–750°С, в ходе которого выделяются мелкодисперсные карбиды, упрочняющие сплав.
Детали, работающие при температурах 700–900°С (например, турбины реактивных двигателей), изготавливают из сплавов на основе никеля и кобальта. Никелевые сплавы делятся на гомогенные (нихромы — ХН60Ю, ХН78Т) и гетерогенные (нимоники — ХН77ТЮ, ХН70МВТЮБ). Нихромы обладают высокой жаростойкостью и используются для нагревательных элементов. Нимоники, содержащие титан и алюминий, проходят сложную термическую обработку (закалка + старение) для достижения максимальной жаропрочности за счет выделения интерметаллидной фазы.
Для экстремально высоких температур (выше 900°С, вплоть до 2500°С) применяют сплавы на основе тугоплавких металлов: вольфрама (Тпл=3400°С), тантала, молибдена (Тпл=2640°С), ниобия. Их высокая жаропрочность обусловлена огромной силой межатомных связей. Наиболее часто используют сплавы молибдена, легированные титаном и цирконием. Главная проблема тугоплавких металлов — низкая жаростойкость; например, оксид вольфрама летуч и не защищает металл, поэтому такие сплавы работают в вакууме или защитной атмосфере. Для защиты от окисления применяют силицирование, создавая на поверхности слой MoSi₂.
Сведения об авторах и источниках:
Авторы: Третьякова Н.В.
Источник: Лекции по материаловедению
Данные публикации будут полезны студентам, изучающим материаловедение и металлургию, инженерно-техническим работникам и специалистам, занятым в области машиностроения, а также всем, кто интересуется историей науки о металлах и современными тенденциями разработки новых материалов.
Дата добавления: 2026-03-10; просмотров: 640;
