Железоуглеродистые сплавы: стали и чугуны, диаграмма состояния, структура и свойства фаз
Железоуглеродистые сплавы, включающие стали и чугуны, являются важнейшими металлическими материалами современной техники. По объему производства чугуна и стали превосходят выпуск всех остальных металлов вместе взятых более чем в десять раз, что подчеркивает их фундаментальное значение для промышленности и строительства. Основополагающее представление о строении этих сплавов дает диаграмма состояния железо–углерод, которая служит теоретической базой для понимания фазовых превращений, структурообразования и выбора режимов термической обработки.
Начало систематическому изучению диаграммы железо–углерод положил выдающийся русский металлург Д.К. Чернов в 1868 году. Он впервые указал на существование в стали критических точек фазовых превращений и установил зависимость их положения от содержания углерода, заложив основы современного металловедения. Диаграмма состояния в полном объеме должна распространяться от чистого железа до углерода, однако железо образует с углеродом устойчивое химическое соединение — цементит (Fe₃C). Поскольку каждое химическое соединение можно рассматривать как самостоятельный компонент, диаграмму изучают по частям, и на практике для металлических сплавов с содержанием углерода до 6,67% рассматривают участок диаграммы от железа до цементита.
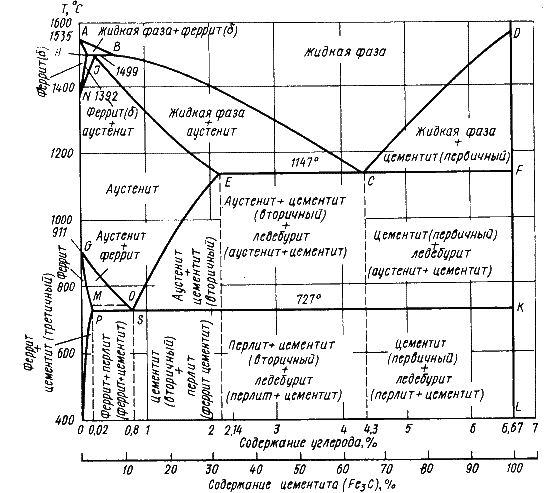
Рис. 9.1. Диаграмма состояния железо – цементит
Компоненты железоуглеродистых сплавов. Основными компонентами железоуглеродистых сплавов являются железо, углерод и цементит, каждый из которых обладает уникальными свойствами и играет определенную роль в формировании структуры. Железо представляет собой переходный металл серебристо-светлого цвета с высокой температурой плавления — 1539°С ± 5°С. В твердом состоянии железо может находиться в двух полиморфных модификациях, причем превращения происходят при температурах 911°С и 1392°С. Ниже 911°С устойчиво α-железо с объемно-центрированной кубической решеткой (ОЦК), в интервале 911–1392°С стабильно γ-железо с гранецентрированной кубической решеткой (ГЦК), а выше 1392°С вновь существует ОЦК-модификация, которую называют δ-железом.
Критическую температуру превращения α↔γ при 911°С обозначают точкой A₃, а температуру превращения γ↔δ при 1392°С — точкой A₄. При температуре ниже 768°С железо обладает ферромагнитными свойствами, а выше — становится парамагнитным; эта точка Кюри обозначается A₂. Железо технической чистоты характеризуется невысокой твердостью (около 80 НВ) и прочностью (предел прочности составляет 250–300 МПа, предел текучести — 120–150 МПа), но при этом отличается высокими показателями пластичности: относительное удлинение достигает 40–50%, а относительное сужение — 70–80%.
Благодаря высокому модулю упругости железа, который сохраняется и в сплавах на его основе, детали из сталей и чугунов обладают необходимой жесткостью. Железо способно образовывать растворы со многими элементами: с металлами формируются твердые растворы замещения, а с углеродом, азотом и водородом — растворы внедрения. Углерод относится к неметаллам и обладает полиморфизмом: в зависимости от условий образования он существует в форме гексагонального графита с температурой плавления около 3500°С или в форме кубического алмаза.
В сплавах железа с углеродом последний может находиться в трех состояниях: в виде твердого раствора с железом, в виде химического соединения — цементита (Fe₃C), а также в свободном состоянии в форме графита, что характерно для серых чугунов. Цементит (Fe₃C) представляет собой карбид железа, содержащий 6,67% углерода, и не испытывает аллотропических превращений. Его кристаллическая решетка образована рядом октаэдров с наклоненными друг к другу осями, что обусловливает высокую твердость материала (более 800 НВ) и практически нулевую пластичность.
Температура плавления цементита точно не установлена и ориентировочно составляет 1250–1550°С. При низких температурах цементит слабо ферромагнитен, но теряет магнитные свойства при нагреве выше 217°С. Цементит способен образовывать твердые растворы замещения, в которых атомы углерода могут замещаться атомами азота или кислорода, а атомы железа — марганцем, хромом, вольфрамом и другими металлами, формируя так называемый легированный цементит. Важной особенностью цементита является его неустойчивость: при определенных условиях он распадается с выделением свободного углерода в виде графита, что имеет ключевое значение при структурообразовании чугунов.
Фазы в системе железо–углерод. В системе железо–углерод различают несколько основных фаз: жидкую фазу, феррит, аустенит и цементит. Жидкая фаза представляет собой однородный расплав, в котором железо растворяет углерод в любых пропорциях, обеспечивая гомогенность жидкого металла перед кристаллизацией. Феррит (Ф) — это твердый раствор внедрения углерода в α-железе, обозначаемый как α(С). Феррит обладает переменной предельной растворимостью углерода: минимальная растворимость составляет 0,006% при комнатной температуре (точка Q на диаграмме), а максимальная достигает 0,02% при температуре 727°С (точка P).
Атомы углерода в решетке феррита располагаются в дефектах и междоузлиях ОЦК-структуры. Выше 1392°С существует высокотемпературный δ-феррит (δ(С)), в котором предельная растворимость углерода повышается до 0,1% при температуре 1499°С (точка J). Свойства феррита близки к свойствам чистого железа: он мягкий (твердость около 130 НВ), пластичный (относительное удлинение достигает 40–50%) и сохраняет ферромагнетизм до температуры 768°С.
Аустенит (А) представляет собой твердый раствор внедрения углерода в γ-железе и обозначается как γ(С). В ГЦК-решетке аустенита атомы углерода занимают центральное положение в элементарной ячейке. Растворимость углерода в аустените также переменна: минимальное содержание 0,8% наблюдается при температуре 727°С (эвтектоидная точка S), а максимальное — 2,14% при температуре 1147°С (эвтектическая точка E). Аустенит обладает твердостью 200–250 НВ, хорошей пластичностью (относительное удлинение около 40–60%) и парамагнитными свойствами.
Цементит как фаза может присутствовать в сплавах в различных морфологических формах: первичный цементит (ЦI), вторичный цементит (ЦII) и третичный цементит (ЦIII). Химические и физические свойства этих фаз идентичны, однако их влияние на механические характеристики сплава различается из-за неодинаковых размеров, количества и расположения выделений. Первичный цементит кристаллизуется непосредственно из жидкой фазы в виде крупных пластинчатых кристаллов. Вторичный цементит выделяется из аустенита при охлаждении и располагается преимущественно по границам зерен бывшего аустенита (в конечной структуре — вокруг зерен перлита). Третичный цементит образуется при выделении из феррита и представляет собой мелкие дисперсные включения, локализованные у границ ферритных зерен. Понимание природы этих фаз и закономерностей их формирования является основой для управления структурой и свойствами сталей и чугунов в процессе термической и химико-термической обработки.
Сведения об авторах и источниках:
Авторы: Третьякова Н.В.
Источник: Лекции по материаловедению
Данные публикации будут полезны студентам, изучающим материаловедение и металлургию, инженерно-техническим работникам и специалистам, занятым в области машиностроения, а также всем, кто интересуется историей науки о металлах и современными тенденциями разработки новых материалов.
Дата добавления: 2026-03-10; просмотров: 709;
