Процесс кристаллизации металлов: термодинамика, механизмы и формирование структуры
Любое вещество в зависимости от внешних условий может находиться в трёх агрегатных состояниях: твёрдом, жидком и газообразном. Переход между этими состояниями возможен исключительно в том случае, если новая фаза является термодинамически более устойчивой в данных условиях и характеризуется меньшим запасом свободной энергии. Изменение внешних параметров, таких как температура и давление, приводит к сложному и нелинейному изменению свободной энергии, причём для жидкого и кристаллического состояний этот закон изменения различен. Графическая интерпретация зависимости свободной энергии жидкой и твёрдой фазы от температуры представлена на рисунке 3.1, который наглядно демонстрирует термодинамические условия фазовых переходов.

Рис.3.1. Изменение свободной энергии жидкой и твёрдой фазы в зависимости от температуры
Согласно термодинамической схеме, при температурах выше точки ТS вещество стремится к минимуму энергии в жидком состоянии, тогда как ниже этой температуры более выгодным становится твёрдое состояние. При температуре, строго равной ТS, наблюдается равновесие фаз: свободная энергия жидкой и твёрдой фазы уравнивается, благодаря чему обе фазы могут сосуществовать одновременно сколь угодно долго без видимых изменений. Данная температура носит название равновесной или теоретической температуры кристаллизации и является ключевым параметром в теории фазовых превращений.
Для того чтобы процесс кристаллизации начался спонтанно, система должна перейти в состояние термодинамической нестабильности, при котором образование твёрдой фазы сопровождается уменьшением свободной энергии. Это условие выполняется при охлаждении жидкости ниже равновесной температуры ТS, однако фактическое начало фазового перехода наблюдается при некоторой более низкой температуре, которая называется фактической температурой кристаллизации. Явление охлаждения жидкости ниже равновесной температуры фазового перехода без начала кристаллизации получило название переохлаждения, количественной характеристикой которого служит степень переохлаждения (ΔТ), рассчитываемая как разность между теоретической и фактической температурами кристаллизации.
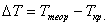
Величина степени переохлаждения не является постоянной для конкретного материала и зависит от совокупности факторов: прежде всего, от природы металла, определяющей его склонность к переохлаждению, от степени его загрязнённости примесями (установлено, что чем выше чистота металла, тем значительнее может быть переохлаждение перед началом кристаллизации), а также от скорости охлаждения расплава (интенсификация теплоотвода способствует увеличению степени переохлаждения). Рассмотрение перехода металла из жидкой фазы в твёрдую требует детального анализа тепловых и структурных изменений, происходящих в системе.
При нагреве абсолютно всех кристаллических тел фиксируется чёткая температурная граница перехода из твёрдого состояния в жидкое, аналогичная граница существует и при обратном процессе — переходе из жидкого состояния в твёрдое, что подчёркивает фазовый характер превращения первого рода. Кристаллизация представляет собой сложный микроструктурный процесс, заключающийся в образовании устойчивых участков кристаллической решётки внутри жидкой фазы и последующем росте кристаллов из сформировавшихся центров. Данный процесс протекает исключительно в условиях, когда система стремится к термодинамически более устойчивому состоянию, характеризующемуся глобальным минимумом свободной энергии.
Кинетику перехода металла из жидкого состояния в кристаллическое традиционно изображают с помощью кривых охлаждения, построенных в координатах «время — температура». На рисунке 3.2 представлена характерная кривая охлаждения для чистого металла, которая демонстрирует ключевые этапы фазового перехода. На данной кривой отчётливо выделяются площадка и перегибы, соответствующие выделению скрытой теплоты кристаллизации, которая компенсирует отвод тепла в окружающую среду и обеспечивает постоянство температуры на фронте кристаллизации.

Рис.3.2. Кривая охлаждения чистого металла с обозначением теоретической (Тs) и фактической (Тф) температур кристаллизации
Начальный участок кривой охлаждения (до точки 1) соответствует остыванию металла, находящегося исключительно в жидком состоянии, при этом процесс сопровождается плавным и монотонным понижением температуры. На отрезке между точками 1 и 2 протекает собственно процесс кристаллизации, сопровождающийся выделением специфического тепла, которое в физике металлов именуется скрытой теплотой кристаллизации. Выделяющееся тепло полностью компенсирует рассеивание тепловой энергии в окружающее пространство, благодаря чему температура системы на этом этапе остаётся строго постоянной, формируя характерную площадку на кривой охлаждения.
После завершения фазового перехода в точке 2, когда весь объём металла перешёл в твёрдое состояние, температура вновь начинает закономерно снижаться, что соответствует охлаждению уже полностью затвердевшего металла. Такой характер кривой охлаждения является эталонным для чистых металлов и позволяет точно определять температурные интервалы фазовых превращений, а также косвенно судить о чистоте материала и условиях проведения процесса. Понимание тепловых эффектов кристаллизации является фундаментальной основой для управления структурой и свойствами литых изделий.
Механизм кристаллизации и закономерности формирования зародышей. При достижении определённой степени переохлаждения в жидком металле начинают самопроизвольно образовываться мельчайшие кристаллики, которые в теории металловедения называются центрами кристаллизации или зародышами. Для того чтобы эти зародыши могли не только возникнуть, но и начать необратимый рост, необходимо дальнейшее уменьшение свободной энергии системы; в противном случае, если рост термодинамически невыгоден, образовавшийся зародыш неизбежно растворяется в окружающей его жидкой фазе. Минимальный размер зародыша, при котором он становится способным к самопроизвольному росту, получил название критического размера, а сам зародыш, преодолевший этот барьер, именуется устойчивым.
Переход атомов из неупорядоченного жидкого состояния в упорядоченное кристаллическое неизбежно требует затрат энергии на создание новой поверхности раздела между жидкой и твёрдой фазами. Процесс кристаллизации будет термодинамически разрешён и будет протекать самопроизвольно только в том случае, когда энергетический выигрыш от образования более устойчивой твёрдой фазы превышает потери энергии, связанные с формированием поверхности раздела «жидкость — кристалл». Графическая зависимость полной энергии системы от размера зарождающейся частицы твёрдой фазы представлена на рисунке 3.3, где наглядно показано существование энергетического барьера, который необходимо преодолеть зародышу.
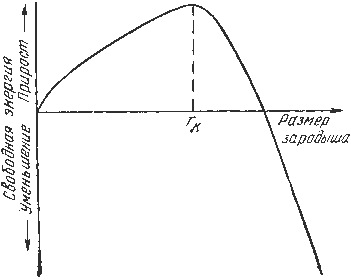
Рис.3.3. Зависимость свободной энергии системы от размера зародыша твёрдой фазы
Зародыши, размер которых меньше критического, термодинамически нестабильны, так как их рост приводит к увеличению свободной энергии системы, поэтому они растворяются. В противоположность этому, зародыши с размерами, равными критическому или превышающими его, при дальнейшем росте обеспечивают неуклонное уменьшение свободной энергии, что делает их способными к существованию и последующему развитию в макроскопические кристаллы. Преодоление критического размера является ключевым моментом зарождения новой фазы и определяет всю дальнейшую кинетику кристаллизации.
Визуализация механизма кристаллизации на микроуровне представлена на рисунке 3.4, который иллюстрирует последовательные стадии этого процесса. Центры кристаллизации возникают в исходной жидкой фазе статистически независимо друг от друга, в случайных местах, где флуктуации плотности и энергии достигают значений, достаточных для преодоления энергетического барьера зарождения. На начальном этапе образовавшиеся кристаллы имеют правильную геометрическую форму, обусловленную их внутренним кристаллическим строением, однако по мере роста и столкновения с соседними растущими кристаллами эта форма неизбежно нарушается.

Рис.3.4. Модель процесса кристаллизации, демонстрирующая зарождение и рост кристаллов
Рост кристаллов после их столкновения продолжается исключительно в тех направлениях, где сохраняется свободный доступ питающей среды, то есть жидкого металла. В результате такого ограниченного роста формируется характерная структура, состоящая из множества сросшихся между собой кристаллов неправильной формы, которые называются кристаллитами или зёрнами. После полного завершения процесса кристаллизации мы имеем дело с поликристаллическим телом, свойства которого определяются размером, формой и взаимной ориентацией составляющих его зёрен.
Качественная картина процесса кристаллизации может быть представлена в строгом количественном виде с помощью кинетической кривой, изображённой на рисунке 3.5. Данная кривая описывает изменение доли закристаллизовавшегося объёма во времени и имеет характерный S-образный вид. В начальный период процесс кристаллизации ускоряется по мере увеличения числа и размеров растущих кристаллов, однако по мере заполнения объёма твёрдой фазой столкновения между кристаллами начинают препятствовать их свободному росту.
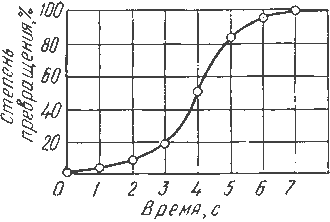
Рис.3.5. Кинетическая кривая процесса кристаллизации
Объём оставшейся жидкой фазы, в которой могут образовываться новые центры и расти существующие кристаллы, неуклонно сокращается. После того как закристаллизуется примерно 50 % общего объёма металла, скорость процесса начинает закономерно замедляться, что связано с уменьшением количества питающей среды и стеснённостью условий роста. Таким образом, с кинетической точки зрения процесс кристаллизации состоит из двух элементарных, но конкурирующих актов: образования центров кристаллизации и последующего роста кристаллов из этих центров.
Ключевым фактором, определяющим кинетику обоих процессов, является степень переохлаждения расплава. Как показано на рисунке 3.6, зависимости числа центров кристаллизации (ч.ц.) и скорости роста кристаллов (с.р.) от степени переохлаждения имеют экстремальный характер с максимумом при определённых температурах. При малых переохлаждениях оба процесса идут медленно, при увеличении переохлаждения они ускоряются, достигая максимума, а затем могут спадать, если переохлаждение становится слишком большим, затрудняя диффузионные процессы.
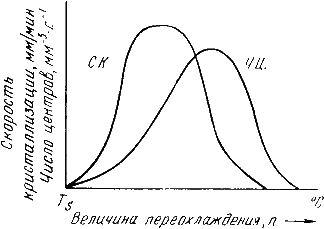
Рис.3.6. Зависимость числа центров кристаллизации (а) и скорости роста кристаллов (б) от степени переохлаждения
Конечные размеры кристаллитов (зёрен) в затвердевшем металле определяются соотношением между скоростью зарождения новых центров и линейной скоростью роста уже существующих кристаллов при фактической температуре кристаллизации. При равновесной температуре ТS оба параметра равны нулю, поэтому процесс кристаллизации вообще не происходит, несмотря на наличие термодинамической движущей силы. Если жидкость переохладить до невысокой степени, соответствующей точке «а» на графике, то формируется крупнозернистая структура, поскольку число образующихся центров невелико, а скорость их роста, напротив, высока, что позволяет немногим зародышам вырасти до значительных размеров.
При переохлаждении до более низкой температуры, соответствующей точке «в», создаются условия для получения мелкозернистой структуры: в единице объёма образуется большое число центров кристаллизации, а линейная скорость их роста относительно невелика, что не позволяет отдельным зёрнам сильно разрастаться до момента столкновения с соседями. В случае экстремально глубокого переохлаждения металла число центров кристаллизации и скорость роста могут упасть практически до нуля, в результате чего жидкость не кристаллизуется в обычном понимании, а переходит в аморфное состояние, характерное для стёкол. Для большинства металлов, обладающих малой склонностью к переохлаждению, экспериментально удаётся зафиксировать лишь восходящие ветви кривых, так как достичь глубокого переохлаждения в обычных условиях крайне сложно.
Технологические приёмы получения мелкозернистой структуры. В металлургии и литейном производстве технологи стремятся к получению мелкозернистой структуры, так как она обеспечивает более высокий комплекс механических свойств готовых изделий, включая прочность, пластичность и вязкость. Оптимальными условиями для формирования мелкого зерна являются: достижение максимально возможного числа центров кристаллизации в единице объёма в сочетании с относительно малой линейной скоростью роста кристаллов. Управление этими параметрами в процессе затвердевания отливки является основной задачей технологии литья.
Размер образующихся зёрен при кристаллизации в значительной степени зависит также от наличия в расплаве мельчайших частиц нерастворимых примесей, которые выполняют функцию готовых (внешних) центров кристаллизации. Такими частицами могут служить тугоплавкие соединения, присутствующие в расплаве, например, оксиды, нитриды или сульфиды. Чем больше в расплаве содержится таких мелкодисперсных, не растворяющихся частиц, тем мельче будет структура закристаллизовавшегося металла, так как отпадает необходимость в преодолении энергетического барьера зарождения для каждого нового кристалла.
Важную роль в формировании структуры играют также стенки изложницы (формы), в которую заливается жидкий металл. Неровности, микротрещины и шероховатости на поверхности стенок служат дополнительными центрами кристаллизации, увеличивая локальную скорость затвердевания и способствуя образованию мелкокристаллической корки по периферии отливки. Это явление широко используется в практике литья для получения качественной поверхности и мелкозернистой структуры в поверхностных слоях изделия.
Наиболее эффективным способом управления структурой является модифицирование — технологический процесс, заключающийся во введении в жидкий металл специально подобранных добавок, называемых модификаторами. По механизму воздействия на процесс кристаллизации модификаторы подразделяются на два основных типа. Первый тип — это вещества, которые практически не растворяются в жидком металле и присутствуют в расплаве в виде взвешенных мельчайших твёрдых частиц, выступающих в роли дополнительных центров кристаллизации (например, добавки тугоплавких соединений). Второй тип — это поверхностно-активные вещества (ПАВ), которые способны растворяться в жидком металле, но, обладая низким поверхностным натяжением, они концентрируются (адсорбируются) на поверхности растущих кристаллов, образуя тонкий слой, который физически или энергетически препятствует их дальнейшему росту.
Применение модификаторов второго типа позволяет эффективно подавлять рост кристаллов даже при относительно небольшом числе центров кристаллизации, что также ведёт к измельчению зерна. Выбор конкретного типа модификатора и его количество определяются природой обрабатываемого металла, требуемой степенью измельчения структуры и конечными эксплуатационными свойствами изделия. Таким образом, комбинируя температурные условия кристаллизации (степень переохлаждения) и введение специальных добавок (модификаторов), можно в широких пределах управлять микроструктурой металлических материалов, добиваясь оптимального сочетания их служебных характеристик.
Сведения об авторах и источниках:
Авторы: Третьякова Н.В.
Источник: Лекции по материаловедению
Данные публикации будут полезны студентам, изучающим материаловедение и металлургию, инженерно-техническим работникам и специалистам, занятым в области машиностроения, а также всем, кто интересуется историей науки о металлах и современными тенденциями разработки новых материалов.
Дата добавления: 2026-03-10; просмотров: 618;
