Металлические сплавы: классификация, типы, кристаллизация и диаграммы состояния
Сплавом в металловедении принято называть вещество, полученное сплавлением двух или более химических элементов, преимущественно металлических. Помимо традиционного сплавления, существуют иные способы получения сплавов: спекание (порошковая металлургия), электролиз и возгонка; материалы, полученные такими методами, часто именуют псевдосплавами. Если сплав приготовлен главным образом из металлических компонентов и сохраняет характерные металлические свойства (электропроводность, пластичность, металлический блеск), его относят к металлическим сплавам. Ключевым преимуществом сплавов перед чистыми металлами является возможность получения разнообразного комплекса свойств, которые закономерно изменяются в зависимости от химического состава и способов термической или механической обработки.
Основные понятия в теории сплавов. В металловедении под системой понимают группу тел или веществ, выделенных для наблюдения и изучения. В качестве систем могут выступать как чистые металлы, так и сплавы: чистый металл представляет собой простую однокомпонентную систему, тогда как сплав является сложной системой, состоящей из двух или более компонентов. Компоненты — это химические элементы или устойчивые химические соединения, образующие систему; при этом соединения рассматриваются как компоненты лишь в том случае, если они не диссоциируют на составные части в исследуемом интервале температур.
Фазой называют однородную часть системы, отделённую от других частей поверхностью раздела, при переходе через которую структура и свойства вещества изменяются скачкообразно. Важнейшей характеристикой равновесия фаз является вариантность (С) , или число степеней свободы, показывающее количество внутренних и внешних факторов (температура, давление, концентрация), которые можно изменять без изменения числа фаз в системе. Если вариантность равна единице (С = 1), система называется моновариантной: допустимо изменение одного из факторов (например, температуры) в некоторых пределах без исчезновения или появления новых фаз. При нонвариантной системе (С = 0) любое изменение внешних условий неизбежно приводит к изменению числа фаз.
Математическая связь между числом компонентов (К), числом фаз (Ф) и вариантностью системы выражается правилом фаз (законом Гиббса). Для большинства металлургических процессов, протекающих при постоянном давлении, правило фаз принимает упрощённый вид:
С = К – Ф + 1
где единица учитывает возможность изменения температуры. Это фундаментальное соотношение позволяет анализировать фазовые равновесия и прогнозировать поведение сплавов при нагреве или охлаждении.
Особенности строения, кристаллизации и свойств сплавов: механические смеси, твёрдые растворы, химические соединения. Строение металлического сплава определяется характером взаимодействия между компонентами, входящими в его состав. Почти все металлы в жидком состоянии неограниченно растворимы друг в друге, однако при затвердевании возможны различные варианты взаимодействия. В зависимости от типа этого взаимодействия сплавы подразделяют на три основных класса: механические смеси, химические соединения и твёрдые растворы.
Механические смеси образуются, когда компоненты не способны к взаимному растворению в твёрдом состоянии и не вступают в химическую реакцию с образованием соединения. Такие сплавы возникают между элементами, значительно различающимися по строению и свойствам, причём силы взаимодействия между однородными атомами превышают силы связи между разнородными атомами. В результате сплав состоит из кристаллов обоих компонентов, сохраняющих собственные кристаллические решётки (рис. 4.1). Микроструктура механической смеси представляет собой конгломерат зёрен исходных фаз, что хорошо видно после травления.

Рис. 4.1. Схема микроструктуры механической смеси
Химические соединения формируются между элементами, также существенно различающимися по природе, но в этом случае энергия взаимодействия разнородных атомов выше, чем однородных. Для химических соединений характерны следующие признаки:
1. постоянство состава, выражаемое формулой АₙВₘ (стехиометрическое соотношение);
2. образование новой, специфической кристаллической решётки, отличной от решёток исходных компонентов и имеющей упорядоченное расположение атомов (рис. 4.2);
3. ярко выраженные индивидуальные свойства (обычно повышенная твёрдость, хрупкость);
4. постоянство температуры кристаллизации, подобно чистым металлам.
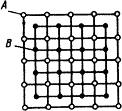
Рис. 4.2. Кристаллическая решётка химического соединения
Твёрдые растворы представляют собой фазы переменного состава, в которых соотношение компонентов может изменяться в широких пределах. Они являются кристаллическими веществами, причём их характерная особенность — наличие в кристаллической решётке атомов обоих компонентов при сохранении типа решётки растворителя. Твёрдый раствор состоит из однородных зёрен (рис. 4.3), что отличает его от механической смеси, где зёрна имеют разную природу.
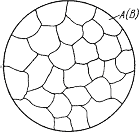
Рис.4.3. Схема микроструктуры твёрдого раствора
Классификация твёрдых растворов. По степени растворимости компонентов различают твёрдые растворы с неограниченной и ограниченной растворимостью. Неограниченная растворимость возможна при выполнении трёх условий:
1. изоморфность (однотипность) кристаллических решёток компонентов;
2. близость атомных радиусов (различие не более 8–13 %);
3. сходство физико-химических свойств и строения валентных электронных оболочек.
В таких растворах кристаллическая решётка растворителя по мере увеличения концентрации растворённого компонента плавно переходит в решётку второго компонента. При ограниченной растворимости существует предел насыщения; превышение этого предела приводит к распаду однородного твёрдого раствора с образованием двухфазной смеси.
По характеру распределения атомов растворённого вещества в решётке растворителя выделяют:
- твёрдые растворы замещения — часть атомов растворителя замещается атомами растворённого элемента (рис. 4.4 а). Замещение происходит статистически, поэтому такие растворы называют неупорядоченными. Периоды решётки изменяются пропорционально концентрации и разности атомных диаметров: если атом растворённого элемента крупнее атома растворителя, параметры решётки возрастают, и наоборот. Изменение параметров существенно влияет на свойства, причём уменьшение параметра ведёт к большему упрочнению, чем его увеличение.
- твёрдые растворы внедрения — атомы растворённого компонента располагаются в порах (междоузлиях) кристаллической решётки растворителя (рис. 4.4 б). Такой тип растворов возможен лишь для элементов с малыми атомными радиусами — углерода, водорода, азота, бора. Поскольку размеры этих атомов обычно превышают размеры межатомных промежутков, решётка искажается, возникают внутренние напряжения, а концентрация таких растворов редко превышает 2–2,5 %.
- твёрдые растворы вычитания (растворы с дефектной решёткой) образуются на базе химических соединений. В этом случае возможна не только замена одних атомов другими в узлах решётки, но и появление вакансий — узлов, не занятых атомами. Обычно это происходит при добавлении одного из компонентов сверх стехиометрического состава: атомы избыточного элемента занимают свои законные места, а часть узлов, принадлежавших другому элементу, остаётся пустой.
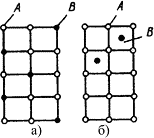
Рис.4.4. Кристаллическая решётка твёрдых растворов замещения (а) и внедрения (б)
Кристаллизация сплавов. Процесс кристаллизации сплавов подчиняется тем же термодинамическим закономерностям, что и кристаллизация чистых металлов: необходимым условием является стремление системы к состоянию с минимумом свободной энергии. Однако в сплавах существенно возрастает роль диффузионных процессов, так как для образования кристаллической фазы требуется перераспределение разнородных атомов между жидкостью и твёрдой фазой. Диффузия в жидкой и твёрдой фазах обеспечивает выравнивание концентраций и возможность роста кристаллов переменного состава.
В твёрдом состоянии в сплавах часто происходят фазовые превращения, обусловленные аллотропическими изменениями компонентов, распадом пересыщенных твёрдых растворов или выделением вторичных фаз при изменении растворимости с температурой. Эти процессы называют фазовыми превращениями в твёрдом состоянии. Они также включают стадии образования центров новой фазы и их роста. Центры кристаллизации обычно возникают на границах зёрен исходной фазы, где решётка наиболее дефектна и присутствуют примеси. Между старой и новой фазами первоначально может существовать когерентная связь — общие кристаллографические плоскости. При достижении определённого размера кристаллов когерентность нарушается, и фазы обособляются. Если структуры фаз сильно различаются, превращение может идти через образование промежуточных метастабильных фаз. Основным инструментом изучения кристаллизации и фазовых равновесий в сплавах служат диаграммы состояния.
Диаграмма состояния. Диаграмма состояния (фазовая диаграмма) представляет собой графическое изображение фазового состава сплавов изучаемой системы в зависимости от температуры и концентрации компонентов (рис. 4.5). Она показывает устойчивые (равновесные) состояния, то есть те фазы, которые при данных условиях обладают минимальной свободной энергией. Поэтому диаграмму состояния также называют диаграммой равновесия.

Рис. 4.5. Общий вид диаграммы состояния двойной системы
Построение диаграмм состояния чаще всего осуществляется с помощью термического анализа. Для серии сплавов различного состава снимают кривые охлаждения, на которых при температурах фазовых превращений наблюдаются точки перегиба или температурные остановки (площадки). Эти температуры называют критическими точками. Некоторые из них имеют специальные названия: температуры начала кристаллизации образуют линию ликвидус, а конца кристаллизации — линию солидус. На диаграмме по оси абсцисс откладывают концентрацию компонентов (обычно в массовых или атомных процентах), по оси ординат — температуру. Основными линиями являются линии ликвидус (1) и солидус (2), а также линии, соответствующие фазовым превращениям в твёрдом состоянии (3, 4).
По диаграмме состояния можно определить:
- температуры фазовых превращений для сплава любого состава;
- фазовый состав при заданной температуре (правило отрезков);
- тип и количество фаз;
- приблизительные свойства сплава (например, по правилу аддитивности);
- возможные виды термической и химико-термической обработки.
Существуют различные типы диаграмм состояния для систем с неограниченной растворимостью в жидком и твёрдом состояниях, с эвтектикой, с перитектикой, с образованием химических соединений и др. Каждый тип диаграммы отражает определённый характер взаимодействия компонентов и позволяет прогнозировать структуру и свойства сплавов. Например, сплавы-механические смеси на диаграмме характеризуются наличием горизонтальной линии (эвтектическое или эвтектоидное превращение), а твёрдые растворы — областями гомогенности, расширяющимися с повышением температуры.
Таким образом, знание основных понятий теории сплавов, типов взаимодействия компонентов и умение читать диаграммы состояния является фундаментом для разработки новых материалов с заданными свойствами и выбора оптимальных режимов их обработки.
Сведения об авторах и источниках:
Авторы: Третьякова Н.В.
Источник: Лекции по материаловедению
Данные публикации будут полезны студентам, изучающим материаловедение и металлургию, инженерно-техническим работникам и специалистам, занятым в области машиностроения, а также всем, кто интересуется историей науки о металлах и современными тенденциями разработки новых материалов.
Дата добавления: 2026-03-10; просмотров: 606;
