Получения хлористого водорода путем пропускания паров воды и хлора над раскаленным углем
На рис. 11 А изображена схема установки для получения хлористого водорода путем пропускания паров воды и хлора над раскаленным углем. Конструирование и испытание подобной установки следует провести на внеклассных занятиях, так как соответствующие реакции посредственно в школьном курсе химии не рассматриваются. Выполнение данного опыта требует особой осторожности, так как исходные, конечные и промежуточные вещества ядовиты (Сl2, СО, а также СОСl2, гидролизующийся до СO2 и НСl).
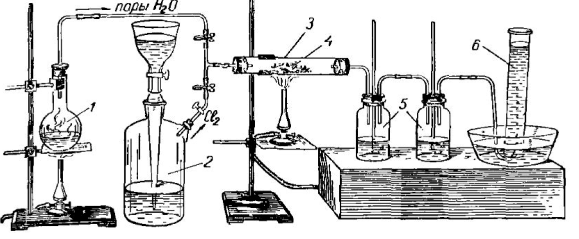
Рис. 11 А. Установка для получения соляной кислоты путем взаимодействия хлора, паров воды и угля при нагревании. Вариант I: 1 — колба с водой; 2 -газометр, наполненный хлором; 3 — трубка стеклянная или фарфоровая; 4 — кусочки древесного угля, перемешанные с порошком окиси железа (катализатор); 5 — склянки с водой для поглощения хлористого водорода; 6 — цилиндр для собирания окиси углерода
Аналогичный опыт был описан также П. Н. Федосеевым в несколько ином конструктивном оформлении (рис. 11 Б). Особенность предлагаемой названным автором установки состоит в том, что в реакционную трубку с древесным или активированным углем (например, от старого противогаза) пропускается только хлор, предварительно увлажненный пропусканием его через промывную склянку 3 с водой. Таким образом, исключается необходимость вводить в реакционную трубку водяные пары, как это имело место в предыдущем варианте.
Вторая особенность предложенного П. Н. Федосеевым прибора состоит в использовании клапана Бунзена 5 для предотвращения засасывания жидкости в трубку. Вместо клапана можно воспользоваться стеклянной воронкой, края которой подходят к поверхности жидкости (рис. 11 Б, 7).
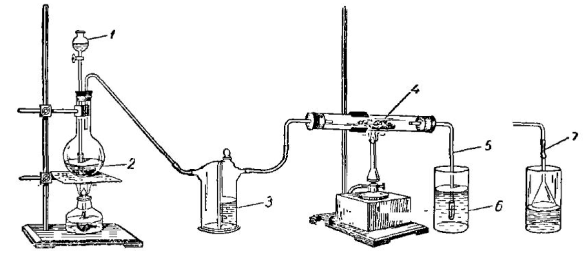
Рис. 11 Б. Установка для получения соляной кислоты путем взаимодействия -хлора, паров воды и угля при нагревании. Вариант II: 1 — капельная воронка с концентрированной соляной кислотой; 2—марганцевокислый калий; 3 — промывная склянка с водой; 4 — реакционная трубка с кусочками древесного угля; 5—газоотводная трубка с клапаном Бунзена на конце; 6 — стакан с водой; 7 — вариант газоотводной трубки с воронкой на конце
В обоих случаях хлористый водород можно определить по образованию тумана соляной кислоты, белого дыма из хлористого аммония (при поднесении к газоотводной трубке стеклянной палочки, смоченной раствором аммиака), а также по окрашиванию синей лакмусовой бумажки в красный цвет. Водный раствор соляной кислоты испытывают, как и в предыдущем случае, азотнокислым серебром, металлическим магнием и т. д.
Реакция между углем, водяными парами и хлором протекает с выделением тепла. При быстром пропускании хлора уголь остается в накаленном состоянии даже в том случае, если нагрев реакционной смеси прекратить.
Учащиеся могут собрать на кружковых занятиях комбинированную установку, аналогичную описанной С. В. Васильевым. Получаемые электролитическим путем хлор и водород пропускают над нагретым активированным углем, причем газы спокойно соединяются друг с другом с образованием хлористого водорода, который затем поглощается водой.
Этот интересный опыт можно видоизменить так, что получаемые электролитическим путем хлор и водород сначала собираются в газометре, откуда они поступают в горелку для сжигания. Но нужно иметь в виду, что водород должен быть чистым, не содержащим кислорода и хлора, во избежание образований взрывчатой смеси, чего при работе с самодельными электролизёрами не всегда удается достичь.
Демонстрация действия основной установки, изображенной на рис. 10, происходит на уроке химии в VIII классе когда учитель излагает материал о производстве соляной кислоты синтетическим способом. После этого разбирается схема промышленной установки, в которой протекают те же химические процессы в сходном техническом оформлении. Но следует отметить различие в способах получения водорода и хлора в промышленности и школьном опыте.
В самом деле, в промышленности сырьем служит раствор хлористого натрия, а в школьном опыте одним из исходных веществ служит соляная кислота. Правда, она может быть заменена серной кислотой (для этого берется смесь хлористого натрия и двуокиси марганца или хлорная известь). Но ближе к техническим условиям находится опыт с получением электролитического хлора и водорода, что рассматривается в курсе химии X класса.
На этом примере учащиеся наглядно видят, как происходит комбинирование (Производства соляной кислоты с производством хлора, водорода, едкого натра, гипохлоритов и хлоратов. Однако материал этот выходит за рамки курса химии VIII класса, но может служить темой внеклассной работы.
Дата добавления: 2023-01-03; просмотров: 8764;
