Второе начало термодинамики (устанавливает определённое направление течения процессов в природе – стрела времени).
Первая часть: Каждая термодинамическая система обладает функцией состояния, называемой энтропией (энтропия – изменение). Энтропия вычисляется следующим образом. Система переводится из произвольно выбранного начального состояния через последовательность состояний равновесия, вычисляются все подводимые при этом к системе порции тепла 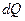 , делится каждая на соответствующую ей абсолютную температуру
, делится каждая на соответствующую ей абсолютную температуру 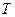 , и все полученные таким образом значения суммируются.
, и все полученные таким образом значения суммируются.
Вторая часть: При реальных (неидеальных) процессах энтропия изолированной системы возрастает 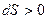 .
.
Если обозначить энтропию через 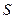 , то
, то
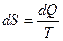 (2)
(2)
и получим соотношение Гиббса:
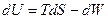 (3)
(3)
Это фундаментальное уравнение, объединяющее первое и второе начала, и в нём по существу заключена вся равновесная термодинамика.
Второе начало термодинамики позволяет судить о направлении процесса и имеет различные формулировки.
Томсона: «Невозможно построить периодически действующую машину, единственным результатом которой было бы поднятие груза за счёт охлаждения теплового резервуара».
Клаузиуса: «Теплота не может самопроизвольно переходить от тела менее нагретого к телу более нагретому».
Из второго постулата следует:
- существование энтропии как функции состояния системы;
- принцип возрастания энтропии.
В гигантской фабрике естественных процессов принцип энтропии занимает место директора, который предписывает вид и течение всех сделок. Закон сохранения энергии играет лишь роль бухгалтера, который приводит в равновесие дебет и кредит.
Третье начало термодинамики (тепловая теорема Нернста)
При абсолютном нуле температуры энтропия принимает значение 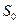 , не зависящее от давления, агрегатного состояния и других характеристик вещества. Эту величину можно положить равной рулю.
, не зависящее от давления, агрегатного состояния и других характеристик вещества. Эту величину можно положить равной рулю.
Теорема Нернста не вытекает из первых двух начал, поэтому в силу своей общности может рассматриваться как новый закон природы - третье начало термодинамики.
В отличие от нулевого, первого и второго начал теоремы Нернста не вводит в термодинамику новой функции состояния, однако именно она делает функции состояния численно определёнными и практически полезными.
Содержание тепловой теоремы Нернста сводится к двум утверждениям.
Первое утверждение состоит в том, что при приближении к абсолютному нулю энтропия стремится к определённому конечному пределу. Поэтому имеет смысл говорить об энтропии тела при абсолютном нуле температур. То есть интеграл
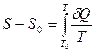
сходится.
Вторая часть теоремы Нернста утверждает, что все процессы при абсолютном нуле температур, переводящие систему из одного равновесного состояния в другое равновесное состояние, происходят без изменения энтропии.
В 1906 году немецкий физикохимик В.Г.Нернст сформулировал свою знаменитую тепловую теорему, ставшую третьим началом термодинамики. Тем самым было завершено аксиоматическое построение классической термодинамики.
Этот этап термодинамики сыграл выдающуюся роль в истории науки.
Логическая стройность равновесной термодинамики, основанной на четырёх началах, породила мнение, что термодинамика уже доведена до своего окончательного завершения. Эту точку зрения целиком поддерживал Нернст, считавший, что развитие термодинамики закончилось.
Такой взгляд не выдержал испытания временем. История науки свидетельствует, что всякая глубокая научная идея не может быть исчерпана до конца. Более того, сама идея развивается и обогащается по мере углубления наших знаний. Именно так обстоит дело с термодинамикой.
Теорема Нернста подвела итог развитию классической равновесной термодинамики.
Классическая термодинамика – это область физики, которая занимается изучением общих свойств макроскопических систем в равновесии, а также общих закономерностей при установлении равновесия.
Из всего многообразия макроскопических объектов, которые нас окружают или которые мы используем в повседневной жизни или работе, термодинамика изучает объекты только в состоянии термодинамического равновесия.
Под состоянием термодинамического равновесия подразумевается состояние, в которое с течением времени рано или поздно приходит система, находящаяся при определённых внешних условиях и определённой постоянной температуре окружающих тел.
При достижении термодинамического равновесия система забывает свою предысторию.
Она помнит только то, что сохраняется в силу законов сохранения (в изолированной системе это суммарные энергия, импульс и масса).
С этой точки зрения окружающий нас мир: мир животных, мир растений, мир неживой природы – представляют собой системы, не находящиеся в состоянии термодинамического равновесия.
Термодинамическое равновесие есть некая абстракция. По отношению к окружающему нас миру это упрощённая модель. Тем не менее, в огромном большинстве практически важных случаев она приводит к правильным результатам.
Термодинамика, как уже говорилось, изучает свойства равновесных состояний. А для равновесных состояний понятия времени не существует. Поэтому время в явном виде в термодинамику не входит (термодинамика не знает времени). В этом смысле об обычной термодинамике говорят как о термостатике (термин введён в 1854 г. В.Томсоном взамен «механической теории тепла»).
Термодинамика позволяет также сделать выводы об общих закономерностях процессов, происходящих при установлении равновесия. Эти выводы касаются направления необратимых процессов и их возможностей при данных условиях. Однако все выводы классической равновесной термодинамики о неравновесных процессах или неравновесных состояниях по-прежнему не включают времени. Утверждение о направлении процесса или запрета процесса не даёт никакой информации о скорости процесса.
Классический этап развития термодинамики кроме формулировки основных начал и анализа вытекающих из них следствий оставил нам в наследство программу действий, связанную прежде всего с необходимостью описания неравновесных процессов.
Классическая термодинамика является мощным средством исследования обратимых процессов. Могущество термодинамического метода состоит в том, что он позволяет получить основные закономерности квазистатических процессов, не вскрывая их молекулярного механизма.
Вполне естественно возникает идея о необходимости создания аналогичного метода для исследования необратимых процессов. В настоящее время такой метод создан и получил своё окончательное оформление под названием термодинамики необратимых процессов.
Сегодня закончена разработка основ линейной теории неравновесных процессов, завершившейся созданием линейной неравновесной термодинамики.
Одно из направлений завтрашнего дня - создание нелинейной феноменологической теории неравновесных процессов.
Разработка общих методов термодинамического анализа неравновесных процессов и неравновесных состояний – это главная задача и содержание неравновесной термодинамики.
Термодинамика неравновесных необратимых процессов – это физическая теория макроскопического описания неравновесных процессов.
Дата добавления: 2014-12-09; просмотров: 1495;
