Методы получения. 14.1.1.1. Гидролиз галогенпроизводных аренов
14.1.1.1. Гидролиз галогенпроизводных аренов. Гидролиз самого хлорбензола протекает с большим трудом из-за –I-эффекта атома хлора по механизму «элиминирование – присоединение». Условия гидролиза: 10-15%-ный водный раствор NaOH, 3500С, 315 атм., время реакции – 20 мин
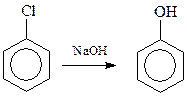
Хлорбензолы, содержащие в кольце и другие заместители электроноакцепторного типа, гидролизуются значительно легче по бимолекулярному механизму. Интересно, что в качестве таких облегчающих гидролиз заместителей могут выступать и атомы галогена. На этом основано получение хлорфенолов: 2,4,5-трихлорфенола и пентахлорфенола
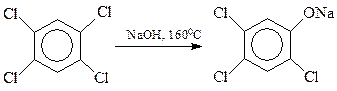
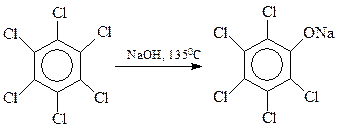
С сожалением приходиться отмечать, что процесс гидролиза тетрахлорбензола часто выходит из-под контроля. При этом быстро и самопроизвольно температура реакции повышается со 1600С до 2300С и выше, происходит соответствующее повышение давления. При таком развитии событий (Севезо, 1976 г.) две молекулы фенолята натрия трихлорфенола вступают между собой в реакцию Вильямсона с образованием 2,3,7,8-тетрахлордибензо-п-диоксина
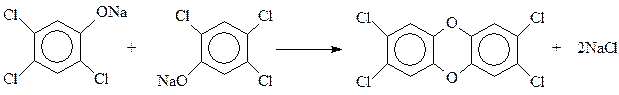
Диоксин – один из наиболее ядовитых органических соединений, созданных когда-либо руками человека. Среднесмертельная доза для человека, полученная расчетным путем, составляет при однократном оральном поступлении 0,05-0,07 микрограммов (миллионных долей грамма).
14.1.1.2. Щелочной плав солей сульфоновых кислот. Этот метод раньше, до разработки кумольного метода, широко применялся для получения фенола и крезолов. Замещение сульфогруппы на гидроксил осуществляется при нагревании солей сульфоновых кислот с едкими щелочами при 3000С и выше
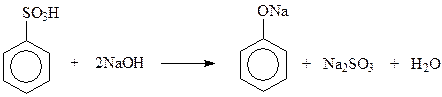
14.1.1.3. Замещение диазогруппы на гидроксил. Эта реакция протекает легко даже в водном растворе соли диазония при 5 – 100С
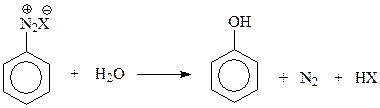
Гидролиз солей диазония – удобный и универсальный лабораторный метод получения разнообразных фенолов.
14.1.1.4. Кумольный метод. Такое название получил метод синтеза фенола разложением гидроперекисей алкилбензолов, чаще всего кумола (Сергеев, Удрис, Кружалов)
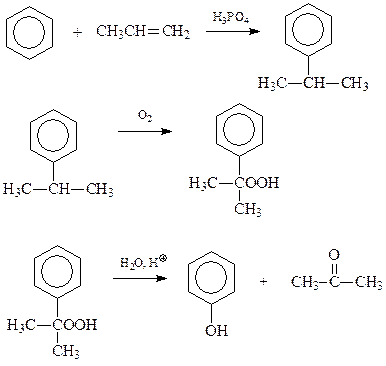
В приведенной схеме ключевым является превращение гидроперекиси кумола в фенол и ацетон.
Предложен следующий механизм кислотного разложения гидроперекиси.
В начальной стадии происходит протонирование гидроксильного кислорода гидроперекиси, который далее отщепляет молекулу воды и превращается в окисный катион
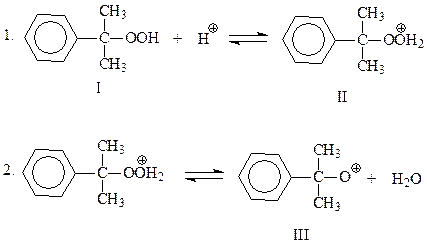
Эта промежуточная частица претерпевает перегруппировку по механизму 1,2-фенильного сдвига. Сам факт этой перегруппировки свидетельствует, что резонансный гибрид канонических структур IV и V устойчивее, чем окисный катион III. Полагают, что движущая сила перегруппировки достаточно велика и, возможно, 2 и 3 стадии рассматриваемого механизма протекают одновременно
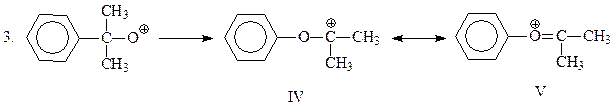
Электрофильная частица, представленная формулами IV и V, присоединяет воду и отщепляет протон. В результате получается гемикеталь VII, образованный фенолом и ацетоном
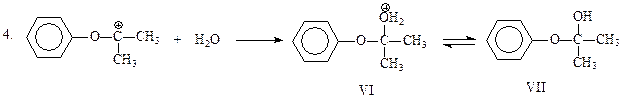
На финальной стадии имеет место гидролиз неустойчивого полукеталя
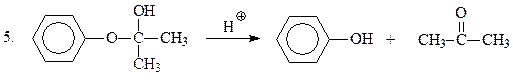
В настоящее время по кумольному методу получают основное количество фенола.
14.1.1.5. Разные реакции. В основу синтеза сложных фенолов, особенно находящих практическое применение, положены самые обычные реакции алкилирования, галогенирования и конденсации самого фенола.
Ниже приводятся примеры таких специальных синтезов.
Как известно, необходимый для синтеза гербицида 2,4-Д дихлорфенол получают хлорированием фенола
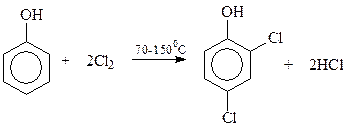
Одним из эффективных антиоксидантов, ингибирующих окисление многих веществ кислородом воздуха, оказались так называемые экранированные фенолы, особенно 4-метил-2,6-ди-трет-бутилфенол (ионол). Его можно получить алкилированием п-крезола изобутиленом
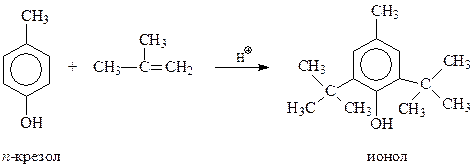
Так же с использованием реакции Фриделя-Крафтса осуществляется синтез алкилфенолов исходя из фенола и тримеров и тетрамеров пропилена и изобутилена
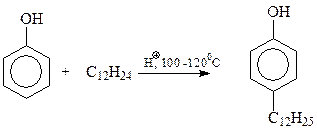
Еще один пример – синтез так называемого бис-фенола, на основе которого производится ценнейший полимер – поликарбонат, относящийся к сложным эфирам угольной кислоты
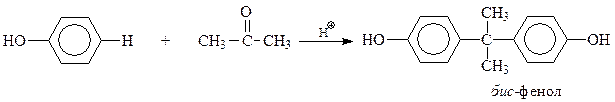
В бензольное кольцо в фенолах могут быть введены и функциональные группы. Одним из интересных примеров может послужить синтез салициловой кислоты по реакции Кольбе-Шмидта
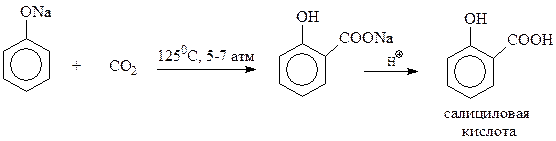
Дата добавления: 2014-12-24; просмотров: 5300;
