Внутренняя энергия реального газа
Внутренняя энергия реального газа складывается из кинетической энергии теплового движения его молекул (она определяет внутреннюю энергию идеального газа, и равна CVT)и потенциальной энергии межмолекулярного взаимодействия. Потенциальная энергия реального газа обусловлена только силами притяжения между молекулами. Наличие сил притяжения приводит к возникновению внутреннего давления на газ:
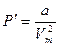 .
.
Работа, которая затрачивается для преодоления сил притяжения, действующих между молекулами газа, как известно из механики, идет на увеличение потенциальной энергии системы, т. е. 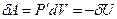 , или
, или 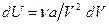 , откуда
, откуда 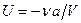
(постоянная интегрирования принята равной нулю). Знак минус означает, что молекулярные силы, создающие внутреннее давление 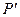 , являются силами притяжения .
, являются силами притяжения .
Учитывая оба слагаемых, получим, что внутренняя энергия моля реального газа растет с повышением температуры и увеличением объема:
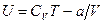 (4.1)
(4.1)
Если газ расширяется без теплообмена с окружающей средой (адиабатический процесс, т. е. 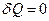 ) и не совершает внешней работы (расширение газа в вакуум, т. е.
) и не совершает внешней работы (расширение газа в вакуум, т. е. 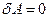 ), то на основании первого начала термодинамики
), то на основании первого начала термодинамики 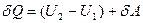 получим, что
получим, что
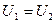 . (4.2)
. (4.2)
Следовательно, при адиабатическом расширении без совершения внешней работы внутренняя энергия газа не изменяется.
Равенство (4.2) формально справедливо как для идеального, так и для реального газов, но физически для обоих случаев совершенно различно. Для идеального газа равенство 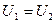 означает равенство температур
означает равенство температур 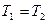 , т. е. при адиабатическом расширении идеального газа в вакуум его температура не изменяется. Для реального газа из равенства (4.2) для моля газа, получается
, т. е. при адиабатическом расширении идеального газа в вакуум его температура не изменяется. Для реального газа из равенства (4.2) для моля газа, получается 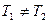
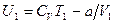 ,
,
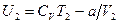 , и отсюда получаем изменение температуры реального газа при его расширении в пустоту
, и отсюда получаем изменение температуры реального газа при его расширении в пустоту
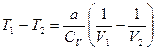 . (4.3)
. (4.3)
Так как при расширении 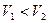 , тогда
, тогда 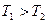 , т. е. реальный газ при адиабатическом расширении в вакуум охлаждается. При адиабатическом сжатии реальный газ нагревается.
, т. е. реальный газ при адиабатическом расширении в вакуум охлаждается. При адиабатическом сжатии реальный газ нагревается.
Дата добавления: 2019-10-16; просмотров: 2160;
