СВОЙСТВА АМИНОКИСЛОТ
І. Кислотно-основные свойства. Амфотерность
Аминокислоты имеют 2 функциональные группы с противоположными свойствами: кислую карбоксильную и основную аминогруппу. Поэтому в водном растворе аминокислоты существуют в виде биполярного иона (рис. 1).
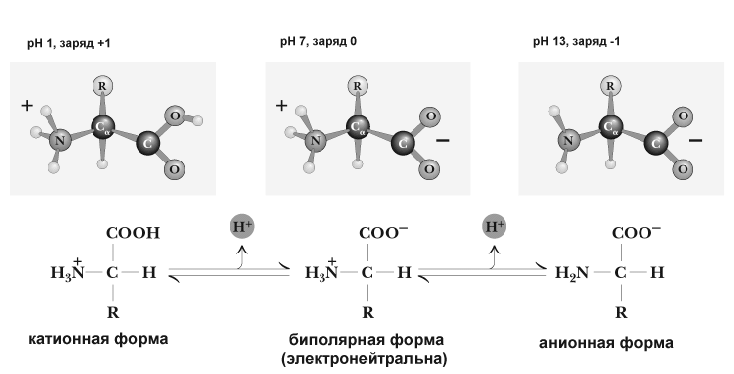
Рис. 1. Анионная, биполярная и катионная форма аминокислот в водных растворителях.
При добавлении в раствор аминокислот дополнительного количества протонов (кислоты) подавляется диссоциация карбоксильных групп и увеличивается количество NH3+-групп. Аминокислоты при этом переходят в катионную форму (приобретают положительный заряд). При добавлении щелочи, наоборот, увеличивается диссоциация карбоксильных групп. Аминокислоты переходят в анионную форму (приобретают отрицательный заряд). Изменяя, таким образом, pH раствора, можно изменять заряд молекул аминокислот.
Нейтральные аминокислоты в воде не имеют заряда. Дикарбоновые аминокислоты имеют две карбоксильные группы, которые диссоциируют, отдавая 2 протона, но поскольку у них только одна аминогруппа, принимающая один протон, то такие аминокислоты ведут себя как кислоты и раствор их имеет кислую реакцию. Сам ион аминокислоты заряжается отрицательно.
Диаминомонокарбоновые аминокислоты реагируют в водном растворе как слабые основания, так как один протон, который освобождается при диссоциации карбоксильной группы таких аминокислот, связывается с одной из аминогрупп, а вторая аминогруппа связывает протон из водного окружения, в результате увеличивается количество OH– групп и повышается pH. Заряд иона таких аминокислот будет положительным.
Добавляя к раствору аминокислоты определенное количество кислоты или щелочи, можно изменить их заряд. При определенном значении pH наступает такое состояние, при котором заряд аминокислоты становится нейтральным. Такое значение pH получило название изоэлектрической точки (ИЭТ),концентрация АК при этом не влияет на величину ИЭТ. При значении pH, равном изоэлектрической точке, аминокислоты не перемещаются в электрическом поле. Если pH ниже изоэлектрической точки, катион аминокислоты движется к катоду, а при pH выше ИЭТ анион аминокислоты — к аноду. На этих свойствах аминокислот основана возможность разделения их в электрическом поле (электрофорез). Кислые аминокислоты имеют ИЭТ в слабокислой среде, основные — в слабоосновной, а нейтральные — в нейтральной.
ІІ. Стереоизомерия
Обусловлена наличием у аминокислоты ассиметричного атома углерода (называется хиральный центр) (рис. 2).
По абсолютной конфигурации (эталон — глицериновый альдегид) АК могут быть L- или D-стереоизомеры (рис. 3). В состав белков организма входят только L-стереоизомеры аминокислот.
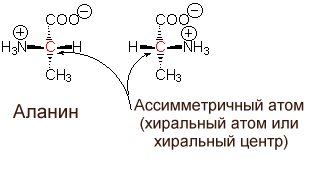
Рис. 2. Ассиметрический атом углерода у аминокислот.
Рис. 3. L- и D-стереоизомеры АК.
Дата добавления: 2017-09-19; просмотров: 1079;
