II. Окисление алкенов.
В зависимости от условий проведения реакции различают окисление алкенов без разрыва по двойной связи, с разрывом молекулы по двойной связи,
и по аллильному положению.
А. Окисление алкенов без разрыва по двойной связи
а) Окисление OsO4 (реакция Криге) или разбавленным раствором КMnO4 при 5-10 0С (реакция Вагнера).
Обесцвечивание фиолетового 3%-ного раствора КMnO4 используется для идентификации кратных связей в непредельных соединениях (проба Байера)
3% р-р KMnO4 ; 50C СH3–CH–CH2
СH3–CH=CH2 ¾¾¾¾¾¾¾¾® | |
или OsO4 OH OH
пропандиол-1,2
Циклоалкены образуют цис-диолы.
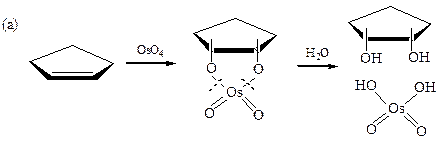
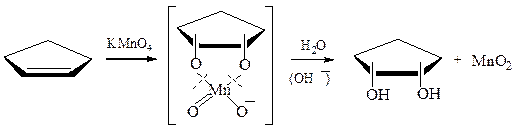
Оба атома кислорода в образующемся цис-гликоле (мезо-соединение) при использовании иона MnO4- происходят из перманганата.
б) Окисление кислородом (Ag; 350 0C) или надкислотами

транс-циклопентандиол-1,2
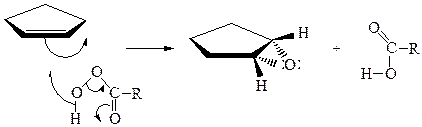
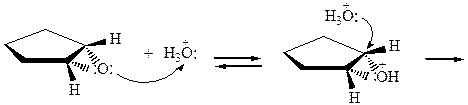
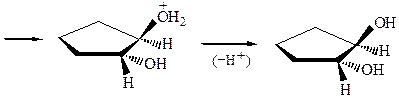
Атака циклического эпоксида осуществляется «сзади», происходит обращение конфигурации атакуемого атома углерода и образование транс-диола-1,2. Возможна атака и другого углеродного атома, приводящая к образованию энантиомера.
Дата добавления: 2017-09-19; просмотров: 1774;
