II. Возбуждающие и тормозящие синапсы и их нейромедиаторы. Пресинаптическое торможение.
Глутамат и аспартат. Функцию медиаторов выполняют некоторые аминокислоты. Важнейшие представители этой группы медиаторов – глутаминовая кислота (глутамат) и близка к ней аспарагиновая кислота (аспартат). Они высвобождаются из окончаний некоторых интернейронов и оказывают кратковременное возбуждающее действие (75% возбуждения в головном мозгу). Рецепторы глутамата (NMDA) способны к так называемой долговременной потенциации, которая является основой памяти.
Гамма-аминомасляная кислота (ГАМК). У млекопитающих ГАМК содержится почти исключительно в головном мозге. Большая часть таких нейронов образует лишь внутренние связи в таких отделах, как кора большого мозга, гиппокамп, мозжечок. Рецепторы ГАМК делятся на три вида: ГАМКа, ГАМКв, ГАМКс (а и с – ионотропные, в – метаботропные). Основной эффект ГАМК – это постсинатическое торможение, обусловленное повышением хлоридной проводимости (развивается ТПСП). Вещества, блокирующие рецепторы ГАМК (например, пикротоксин и бикукуллин), вызывают судороги; это навело на мысль, что решающую роль в развитии эпилепсии играет нарушение функции ГАМК-эргических интернейронов коры мозга. Рецепторы ГАМК исключительно сложные – полисайтные. На них действуют как агонисты бензодиазепины и барбитураты.
Пресинаптическое торможение локализуется в пресинаптических терминалях перед синаптической бляшкой. На пресинаптических терминалях располагаются окончания аксонов других нервных клеток, образующих здесь аксо-аксональные синапсы. ГАМК открывает ионные каналы для Cl–, и гиперполяризуют или деполяризуют мембрану терминалей (зависит от баланса ионов Cl– внутри и вне клетки). Это обусловливает частичную или полную блокаду проведения по нервным волокнам возбуждающих импульсов, идущих к нервным окончаниям.
Глицин обнаружен главным образом в стволе головного мозга и спинном мозге. Полагают, что в спинном мозге он обусловливает тормозные влияния интернейронов (клеток Реншоу) на мотонейроны. Однако в головном мозгу действует как активирующий медиатор и модулирует NMDA-рецепторы глютамата.
III. Медиаторы моноамины.
Ацетилхолин (АЦХ) встречается в лимбической системе и стриатуме. АЦХ может действовать либо на никотиновые (ионотропные, возбуждение быстрое, но нестойкое), либо на мускариновые рецепторы (метаботропные, возбуждение возникает медленнее, но сохраняется дольше). АЦХ-нейроны лежат в конечном мозгу, особенно их много в базальном ядре Мейнерта. Дегенерация этих клеток приводит к ускоренному психическому старению. Причина – накопление белка-амилоида на поверхности АЦХ-нейронов.
Ущерб – около 100 млрд. долларов. Расходы в мире на исследования и лечение – около 10 млрд. долларов.
Дофаминергическая (ДА-) система головного мозга представлена телами ДА-нейронов в области черной субстанции среднего мозга, разветвлениями их аксонов и рецепторами дофамина (ДА). ДА-нейроны, как и другие аминергические клетки отличаются исключительно разветвленными аксонами и обилием разнообразных синаптических терминалей. Так, проецируясь в стриатум, ДА-нейрон способен образовывать до одного миллиона синаптических контактов. Рост и ветвление ДА аксонов продолжается вплоть до достижения человеком взрослого возраста. Помимо классических синапсов ДА-клетки образуют варикозеты, что позволяет им оказывать модулирующее действие сразу на большое количество нейронов. Основными мишенями проекций ДА-нейронов являются неостриатум и различные отделы неокортекса.
На сегодняшний день описаны пять типов рецепторов ДА (Д1-Д5), обладающих значительным генетическим полиморфизмом. Рецепторы ДА являются метаботропными – они не связаны непосредственно с ионными каналами, а ассоциированы с регуляторными G-белками, находящимися на внутренней стороне постсинаптической мембраны. Связывание ДА с рецептором побуждает G-белки активировать или тормозить фермент аденилатциклазу, которая в свою очередь управляет синтезом вторичного мессенджера – цАМФ. цАМФ действует на многие процессы в клетке, в том числе на работу натрий-калиевой АТФ-азы. Действие ДА на Д1- и Д5-рецепторы за счет повышения внутриклеточной концентрации цАМФ и активации протеинкиназы А в основном приводит к развитию в нейронах-мишенях медленного возбуждения. Второе семейство представлено Д2- Д3-Д4-рецепторами. Эти рецепторы отрицательно сопряжены с аденилатциклазой и угнетают синтез цАМФ. Активация Д2- Д3-Д4-рецепторов основном приводит к развитию гиперполяризации клеток мишеней за счет увеличения проводимости для ионов калия. В целом воздействие ДА на нейроны уникально в том плане, что оно обеспечивает увеличение соотношения сигнал/шум в нервных клетках за счет подавления их фоновой активности, без снижения вызванных реакций.
Предполагают, что ДА-нейроны играют важную роль в мозговой системе вознаграждения. ДА-систему расценивают как детектор благоприятности среды: они активируются событиями, которые лучше, чем ожидаемые; не реагируют – при совпадении с ожиданием; тормозятся – если события хуже, чем ожидалось. Если вслед за активацией корковостриатного синапса, происходит выброс ДА из варикозного расширения, то проведение в синапсе облегчается. Таким образом, ДА-система контролирует корково-стриато-таламо-корковые цепи в процессе формирования целенаправленного поведения.
ДА играет ключевую роль в системе так называемого «приближающего поведения». Деятельность системы приближающего поведения лежит в основе состояний приятного предвосхищения, надежды и дает основной вклад в генерацию положительных эмоций.
ДА-система связана с организацией движений и когнитивными процессами. При избыточной активности ДА-системы у человека развивается шизофрения. Считают, что гиперфункция ДА-системы может приводить к чрезмерному усилению сигнал/шум в нейронных цепях Генетическая предрасположенность к шизофрении обусловлена индивидуальными особенностями в наборе изоформ рецепторов Д3 и, возможно, Д4, что приводит к их гиперчувствительности. Предполагается, что развитие шизофрении может быть также связано с нарушениями баланса активности ДА- и глутаминергической систем. Имеются многочисленные данные о субоптимальной активности ДА-системы при эндогенной депрессии.
В последнее время К. Блумом и коллегами (Blum et al., 2000) высказывается предположение, что определенные генетически предопределенные варианты рецепторов ДА-системы могут лежать в основе «синдрома дефицита подкрепления». Синдром проявляется при сочетании ряда наследуемых черт с неблагоприятными воздействиями среды (ранние стрессы, родительский алкоголизм и т.д.). Главной особенностью является пониженная активность ДА-системы. Синдром приводит к повышенному риску возникновения импульсивных и компульсивных расстройств: алкогольной, никотиновой, кокаиновой, героиновой и иных зависимостей, аутизма, насильственного и асоциального поведения, СДВГ.
Норадренергическая (НА-) система головного мозга берет начало главным образом в голубом пятне (ГП). ГП расположено билатерально на границе между мостом и средним мозгом. В ядре у человека находится очень небольшое число нервных клеток – до 50.000 (в расчете на одну – левую или правую сторону мозга). ГП образует настолько широкие эфферентные проекции, что фактически иннервирует большее количество мозговых областей, чем любое иное ядро ЦНС. НА-волокна входят во фронтальный регион коры и затем образуют «паутину» волокон, пронизывающую с промежутками в 30-40 мкм на уровне III-IV слоев все области коры в рострокаудальном направлении. Имеются многочисленные варикозные расширения по ходу волокон, диффузно выделяющие НА во внеклеточное пространство коры.
Во время медленного сна активность НА-клеток снижается и полностью исчезает в стадии парадоксального сна. Выдвинуто предположение, что одной из функций парадоксального сна как раз и является снижение активности НА-клеток, что приводит к восстановлению чувствительности рецепторов НА головного мозга.
НА вызывает в клетках-мишенях как возбудительные, так и тормозные эффекты. Характер воздействия на конкретную клетку определяется концентрацией медиатора, наличием и соотношением типов рецепторов, с которыми связывается НА. В ЦНС это метаботропные α1-, α2-, β1- и β2-адренорецепторы. Регуляция адренорецепторами ионных каналов, как и у рецепторов ДА, опосредована G-белками и вторичными внутриклеточными посредниками. Считают, что в центральных нервных сетях активация α1-рецепторов приводит к возбудительным эффектам. Что касается эффектов активации α2-рецепторов, то они в общем тормозные благодаря возрастанию калиевой проводимости в клетках-мишенях. Считают, что β1-рецепторы могут опосредовать тормозные, а β2-рецепторы – возбудительные эффекты.
При активации ГП наблюдается поведенческое возбуждение, что связано с повышением эффективности воздействия внутренних и внешних стимулов. В неокортексе усиливаются как возбудительные ответы, связанные с активацией глутаматергических входов (через α1-адренорецепторы), так и тормозные. Афферентный приток может становиться более эффективным благодаря большему подавлению фоновой, чем вызванной активности клеток-мишеней. В результате этого реакции нейронов по отношению к фону усиливаются, т.е. увеличивается соотношение «сигнал-шум» клетки
Стимуляция ГП электрическим током у кошек вызывает тревогу и страх.
Обнаружена тесная связь между активностью нейронов ГП обезьян, с одной стороны, и уровнем исполнения оперантной задачи, отражающим внимание животного, с другой. Взаимоотношения между ними напоминают классическую кривую Йеркса-Додсона (рис. 1,3). Низкий активности не обеспечивает выполнения задач, очевидно в связи с пониженным уровнем внимания и arousal. Средний уровень активности и хорошо выраженные фазные реакции НА-клеток лежат в основе состояния фокусированного внимания и оптимального исполнения поведенческой задачи. Высокий уровень тонической активности сочетается со слабой выраженностью фазических реакций. Такая активность лежит в основе лабильного внимания и частых ошибок.
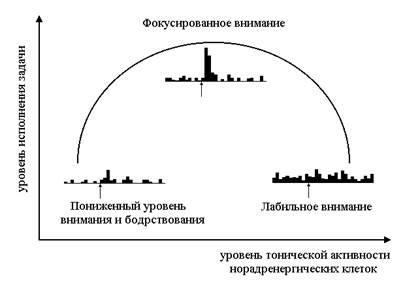 |
Рис. 1.3. Инвертированная U-образная зависимость между тонической активностью норадренергических клеток голубого пятна и уровнем выполнения поведенческой задачи, требующей выделения целевого стимула (по Aston-Jones, 2000).
Хроническая гиперактивность НА-системы может приводить к развитию некоторых симптомов маниакально-депрессивных расстройств, включая приступы паники, импульсивность и бессонницу (для лечения применяют анксиолитики). В то же время, недостаточная активность НА-клеток является вероятной причиной депрессии, развивающейся вслед за стрессом, при переходе его в дистресс.
Роль НА-системы головного мозга в регуляции внимания и ответоспособности указывает на ее возможную вовлеченность в развитие синдрома дефицита внимания с гиперактивностью (СДВГ). СДВГ может быть связан с чрезмерной тонической активностью НА-нейронов ГП. Результатом является чрезмерная лабильность внимания и неспособность к его фокусированию, гиперактивность. Наоборот, некоторые типы аутизма могут быть связаны с чрезмерной выраженностью фазических ответов. Такая активность может продуцировать чрезмерно фиксированный вид взаимодействия, когда поведение становится «застревающим» на внутренних драйвах и неспособным к изменению при изменении ситуации (Aston-Jones et al., 2000).
Серотонинергическая (СТ-) система образована скоплениями нейронов, в пределах ядер шва (ЯШ). СТ-система отличается высокой степенью разветвленности. Вся неокортикальная мантия пронизана тонкими, извилистыми СТ-волокнами с варикозными расширениями.
В ЦНС в настоящее время выделяют по крайней мере семь различных типов рецепторов СТ (5-гидропситриптамина) или, как их чаще называют, 5-НТ-рецепторов с 15 подтипами. Большинство 5-НТ-рецепторов являются метаботропными и только 5-НТ3-рецепторы относятся к ионотропным. 5-НТ1-рецепторы оказывают преимущественно тормозящее действие на клетки-мишени, другие типы рецепторов – преимущественно возбуждающее, быстрое у 5-НТ3-рецепторов и более медленное, у остальных.
СТ, в противоположность ДА и НА, в сенсорных и ассоциативных регионах мозга ослабляет ответы нейронов, уменьшая соотношение сигнал/шум в процессах переработки информации. В то же время он преимущественно усиливает реакции нейронов в структурах мозга связанных с моторными функциями (Jacobs, Fornal, 1995; Саченко, Хоревин, 2001).
При недостатке СТ возникают тревожность, депрессивные состояния, сопровождающиеся мигренью и вегето-сосудистой дистонией. Количество СТ резко падает зимой (сезонная депрессия), на обмен его влияет и питание (синтезируется из триптофана). Длительное воздействие стресса, с переходом в дистресс, приводит к истощению СТ-передачи, которое сопровождается психическими нарушениями, выражающимися не только в усилении чувства тревоги, но и в агрессивности и попытках суицида. Пациенты с депрессиями обычно демонстрируют компульсивные действия, например, повторяющиеся стереотипные моторные акты. Вероятно такое поведение может рассматриваться как своего рода самолечение, т.к. подобная двигательная активность активирует СТ-систему и стимулирует повышенное выделение СТ (Jacobs, Fornal,1995). Подобный эффект вызывают и другие движения (ходьба, жевание резинки).
Гистаминергические нейроны лежат в задних отделах гипоталамуса. Их функция окончательно не выяснена, но считается, что они учавствуют в процессах мотивации и полового поведения, контролируют выделение гормонов.
Исходя из понимания роли моноаминов, применяют соответствующие антидепрессанты – ингибиторы обратного всасывания ДА, НА и СТ (амитриптилин) или СТ (флуоксетин, прозак, сертралин). Индивидуальные особенности аминергических систем лежат в основе формирования темперамента человека.
Дата добавления: 2017-09-19; просмотров: 2063;
