ОСНОВНЫЕ ПУТИ КАТАБОЛИЗМА УГЛЕВОДОВ
Распад углеводов в организме человека и животных начинается еще в ротовой полости. Полисахариды и олигосахариды распадаются на простые соединения посредством реакций двух типов: гидролиза и фосфоролиза.
Гидролиз (или расщепление макромолекулы в присутсвии воды) крахмала ускоряется специфическими ферментами — амилазами, относящимися к классу гидролаз. В зависимости от характера фермента гидролитический разрыв эфирных связей между остатками a-D-глюкопиранозы в молекуле крахмала может происходить до глюкозы, мальтозы или олигосахаридов.
В природе найдено несколько амилаз: a-амилаза, b-амилаза, g-амилаза (глюкоамилаза) и амило-1,6-глюкозидаза.
a-Амилаза (a-1,4-глюкан-4-глюканогидролаза) ускоряет гидролиз внутренних a-1,4-гликозидных связей в молекуле крахмала. В качестве основного конечного продукта гидролиза крахмала при участии a-амилазы образуется мальтоза в a-форме. a-Амилаза найдена у всех видов растений и животных.
b-Амилаза (a-1,4-глюкан-мальтогидролаза) ускоряет гидролиз a-1,4-гликозидных связей, начиная с невосстанавливающего конца молекулы крахмала, последовательно отщепляя остатки мальтозы. Мальтоза, освобождающаяся при гидролизе крахмала под действием b-амилазы, получается в b-форме. Образование последней происходит в момент гидролиза a-гликозидной связи вследствие изменения пространственной конфигурации образующегося гликозидного гидроксила при первом углеродном атоме остатка глюкозы. b-Амилаза найдена лишь у высших растений.
g-Амилаза (a-1,4-глюкан-глюкогидролаза, глюкоамилаза) ускоряет гидролиз a-1,4-гликозидных связей в молекуле крахмала или олигосахаридов, последовательно отщепляя остатки глюкозы от невосстанавливающего конца молекулы.
Амило-1,6-глюкозидаза (амило-6-глюканогидролаза) ускоряет реакцию гидролиза 1,6-связей в молекуле крахмала (амилопектина), т.е. в точках разветвления полиглюкозидной цепи, и образует олигосахариды с тем или иным числом остатков a-D-глюкозы и зависимости от длины отщепляемой боковой цепи. Фермент характерен для животных тканей, но встречается также у растений и микроорганизмов. Характерной особенностью всех амилаз является отсутствие абсолютной специфичности действия. Они ускоряют гидролиз различных соединений: амилозы, амилопектина, гликогена и олигосахаридов.
Аналогично крахмалу и гликогену гидролизуются и другие природные полисахариды: целлюлоза — при участии фермента целлюлазы, хитин — хитиназы, гепарин — гепариназы и др. Дисахариды, возникающие в ряде случаев при гидролизе полисахаридов (например, мальтоза и целлобиоза) или существующие в организме в свободном виде (лактоза, сахароза, трегалоза и др.), гидролизуются при каталитическом воздействии a- и b-гликозидаз до индивидуальных моносахаридов.
Другой путь распада полисахаридов и олигосахаридов — фосфоролиз — наиболее характерен для гликогена. Реакция фосфоролиза заключается в присоединении фосфорной кислоты по месту разрыва гликозидной связи между остатками моносахаридов в молекулах олиго- или полисахаридов.
Реакции фосфоролиза ускоряются специфическими ферментами — фосфорилазами (гликозилтрансферазами), причем фосфоролитическому расщеплению подвергаются лишь 1,4-гликозидные связи. Поэтому в случае фосфоролиза, например, амидопектина распад прекращается в точках разветвления молекулы, где имеются 1,6-связи. Дальнейший фосфоролиз будет происходить лишь после расщепления 1,6-связей в остаточном декстрине при посредстве амило-1,6-гликозидазы.
Таким образом, при распаде олиго- и полисахаридов возникают свободные моносахариды или их фосфорные эфиры. В дальнейшем обмене моносахаридов участвуют только их фосфорные эфиры, свободные же монозы фосфорилируются, превращаясь в фосфорные эфиры, представляющие собой гораздо более реакционноспособные соединения по сравнению со свободными моносахаридами.
Фосфорилирование моносахаридов осуществляется при их взаимодействии с АТФ и ускоряется ферментами — фосфотрансферазами, носящими название киназ. Фосфорилирование глюкозы, например, идет по схеме: глюкокиназа
Глюкоза + АТФ ¾¾¾¾¾¾® Глюкозо-6-фосфат + АДФ.
В природе обнаружено около двух десятков индивидуальных фосфотрансфераз, переносящих остатки фосфорной кислоты от АТФ. Процесс обмена углеводов протекает через некоторые их формы, занимающие ключевые позиции (например, глюкозо-6-фосфат и рибулозо-5-фосфат).
Глюкозо-6-фосфат образуется в организме разными путями, в том числе при фосфорилировании глюкозы, и, за счет изомеризации (при участии фермента фосфоглюкомутазы) глюкозо-1-фосфата, который образуется в свою очередь в процессе фосфоролиза олиго- и полисахаридов.
Глюкозо-6-фосфат подвергается разнообразным превращениям. В процессе его окислительного распада запасается энергия в мак-роэргических связях АТФ. Кроме того, многие из промежуточных продуктов, образующихся при обмене глюкозо-6-фосфата, используются для синтеза аминокислот, нуклеотидов, глицерина, высших жирных кислот и т. п.
Катаболизм глюкозо-6-фосфата осуществляется преимущественно двумя путями: дихотомическим (гликолиз), когда на определенной стадии молекула распадается пополам, и апотомическим (пентозофосфатный путь), когда молекула теряет первый углеродный атом.
На рисунке 4.6 показана схема, обобщающая основные пути распада углеводов.

Рисунок 4.6 - Схематическое изображение путей катаболизма
Полисахаридов
Взаимосвязи между путями распада углеводов сложны и определяются как видовыми особенностями, так и условиями жизнедеятельности организмов. Даже в различных тканях и органах одного и того же организма соотношения путей распада углеводов могут быть различными. У подавляющего большинства организмов аэробный путь распада углеводов в целом превалирует над анаэробным, а дыхание подавляет гликолиз и брожение.
Дихотомический путь распада глюкозы (гликолиз)
Основным катаболическим процессом деструкции глюкозы в клетках животных и человека является последовательность ряда реакций ее окисления, в результате которых в анаэробных (без участия кислорода) условиях глюкоза превращается в лактат (молочную кислоту), а в аэробных (в присутствии кислорода) – в конечные продукты распада - СО2 и Н2О.
Гликолиз (от «glycys» - сладкий и «lysis» - растворение, распад) – это последовательность ферментативных рекций, в процессе которых глюкоза расщепляется на две молекулы пирувата (аэробный гликолиз), или лактата (анаэробный гликолиз), сопровождаясь выделением энергии АТФ. Ниже приведены реакции анаэробного (1) и аэробного (2) гликолиза с учетом всех стехиометрических коэффициентов:
С6Н12О6 + 2АДФ + 2Н3РО4 ¾¾¾¾® 2СН3СНОНСООН + 2АТФ + 2Н2О (1)
С6Н12О6 + 2АДФ + 2Н3РО4 + НАД+ ¾¾¾¾® 2СН3СОСООН + 2АТФ +
2Н2О + 2НАДН.Н+ (2)
Разделение на анаэробный и аэробный гликолиз носит чисто условный характер, поскольку первые реакции гликолиза в присутствии кислорода и без него одни и те же, отличия касаются лишь их скорости и конечных продуктов. При недостатке кислорода реокисление НАДН.Н+, образовавшегося в ходе гликолиза, осуществляется путем сопряжения с восстановлением пирувата в лактат, а в аэробных условиях НАДН.Н+ окисляется в ходе кислородзависимого фосфорилирования, результатом которого является образование большого количества АТФ.
В анаэробных условиях гликолиз – единственный процесс в организме животных, растений и микроорганизмов, приводящий к образованию АТФ.
В аэробных условиях реакции гликолиза, остановившиеся на стадии образования пирувата, составляют первую, начальную стадию деструкции углеводов, связанную с циклом трикарбоновых кислот (см. далее).
Весь этап гликолиза протекает в две стадии.
Первая стадия – подготовительная, или стадия активации глюкозы, которая включает пять реакций и завершается расщеплением глюкозы на две молекулы триозы – глицеральдегидфосфата (рисунок 4.7).
На первой стадии гликолиза глюкозо-6-фосфат претерпевает изомеризацию и превращается в b-D-фруктозо-6-фосфат (на схеме реакция 2), который далее фосфорилируется по первому углеродному атому с образованием фруктозо-1,6-дифосфата (реакция 3). Это ключевая реакция процесса гликолиза, от которой зависит скорость всего гликолиза в целом.
Фруктозо-1,6-дифосфат подвергается далее дихотомическому распаду на две фосфотриозы (фосфоглицеральдегид и дигидроксиацетонфосфат) (реакция 4), превращающиеся друг в друга (на схеме реакция 5).
В дальнейший обмен вступает только 3-фосфоглицериновый альдегид. По мере расходования убыль этого соединения восполняется за счет фосфодиоксиацетона, который практически полностью в него превращается. Поэтому из каждой молекулы фруктозо-1,6-дифосфата возникают две молекулы 3-фосфоглицеринового альдегида. Все последующие реакции и их продукты удваиваются!
Вторая стадия – стадия генерации АТФ, в которой энергия окислительных реакций трансформируется в энергию химической связи АТФ по механизму реакции субстратного фосфорилирования.
Процесс синтеза богатой энергией АТФ при непосредственном участии окисляемого субстрата (в данном случае, 3-фосфоглицеринового альдегида) называетсяокислительным фосфорилированием на уровне субстрата.

 
 


 



            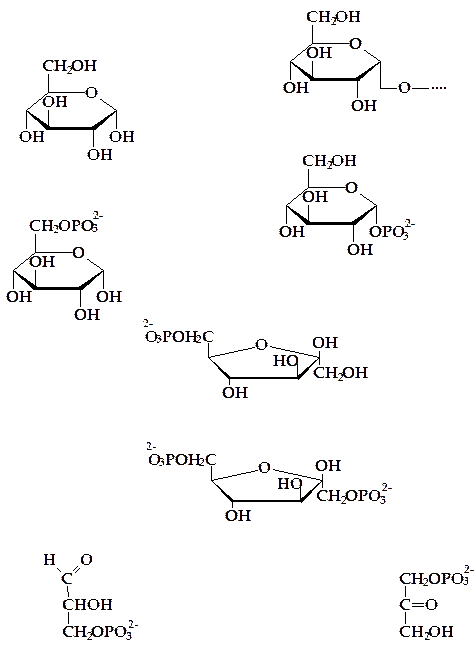
ф е р м е н т ы: 1 – гексокиназа (глюкокиназа); 1а – гликогенфосфорилаза; 1б – фосфоглюкомутаза; 2 – глюкозофосфатизомераза; 3 – фосфофруктокиназа; 4 – фруктозодифосфатальдолаза (альдолаза); 5 – триозофосфатизомераза. Рисунок 4.7 - Реакции гликолиза, гликогенолиза |
Дата добавления: 2017-08-01; просмотров: 3094;
