Тангенциальная составляющая ускорения 8 страница
В молекулярно-кинетической теории пользуются идеализированной модельюидеального газа, согласно которой считают, что:
1) собственный объем молекул газа пренебрежимо мал по сравнению с объемом сосуда;
2) между молекулами газа отсутствуют силы взаимодействия;
3) столкновения молекул газа между собой и со стенками сосуда абсолютно упругие.
Модель идеального газа можно использовать при изучении реальных газов, так как они в условиях, близких к нормальным (например, кислород и гелий), а также при низких давления» и высоких температурах близки по своим свойствам к идеальному газу. Кроме того, внеся поправки, учитывающие собственный объем молекул газа и действующие молекулярные силы, можно перейти к теории реальных газов.
Рассмотрим законы, описывающие поведение идеальных газов.
Закон Бойля—Мариотта*: для данной массы газа при постоянной температуре произведение давления газа на его объем есть величина постоянная:
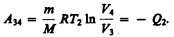 (41.1)
(41.1)
* Р. Бойль (1627—1691)—английский ученый; Э. Мариотт (1620—1684) — французский физик.
Кривая, изображающая зависимость между величинами р и V, характеризующими свойства вещества при постоянной температуре, называетсяизотермой. Изотермы представляют собой гиперболы, расположенные на графикетем выше, чем выше температура, при которой происходит процесс (рис. 60).
Законы Гей-Люссака*:1) объем данной массы газа при постоянном давлении изменяется линейно с температурой:
(41.2)
2) давление данной массы газа при постоянном объеме изменяется линейно с температурой:
(41.3)
* Ж. Гей-Люссак (1778—1850) — французский ученый.
В этих уравнениях t — температура по шкале Цельсия, р0 и V0 — давление и объем при 0°С, коэффициент a = 1/273,15 К–1.
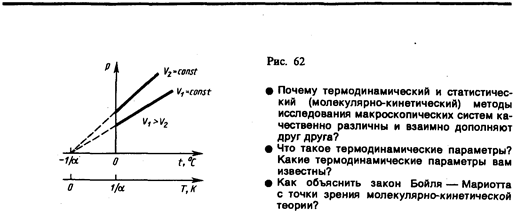
Процесс, протекающий при постоянном давлении, называетсяизобарным. На диаграмме в координатах V, t (рис. 61) этот процесс изображается прямой, называемой изобарой. Процесс, протекающий при постоянном объеме, называетсяизохорным. На диаграмме в координатах р, t (рис. 62) он изображается прямой, называемойизохорой.
Из (41.2) и (41.3) следует, что изобары и изохоры пересекают ось температур в точке t=–1/a=–273,15°С, определяемой из условия 1+at = 0. Если перенести начало отсчета в эту точку, то происходит переход к шкале Кельвина (рис. 62), откуда
Вводя в формулы (41.2) и (41.3) термодинамическую температуру, законам Гей-Люссака можно придать более удобный вид:
(41.4)
(41.5)
где индексы 1 и 2 относятся к произвольным состояниям, лежащим на одной изобаре или изохоре.
Закон Авогадро*: моли любых газов при одинаковых температуре и давлении занимают одинаковые объемы. При нормальных условиях этот объем равен 22,41×10–3 м3/моль.
* А. Авогадро (1776—1856) — итальянский физики химик.
По определению, в одном моле различных веществ содержится одно и то же число молекул, называемое постоянной Авогадро:
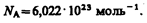
Закон Дальтона*: давление смеси идеальных газов равно сумме парциальных давлений p1, p2 ,..., рn входящих в нее газов:
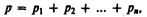
Парциальное давление — давление, которое производил бы газ, входящий в состав газовой смеси, если бы он один занимал объем, равный объему смеси при той же температуре.
* Дж. Дальтон (1766—1844) — английский химик и физик.
§ 42. Уравнение Клапейрона — Менделеева
Как уже указывалось, состояние некоторой массы газа определяется тремя термодинамическими параметрами: давлением р, объемом V и температурой Т. Между этими параметрами существует определенная связь, называемаяуравнением состояния, которое в общем виде дается выражением
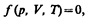
где каждая из переменных является функцией двух других.
Французский физик и инженер Б. Клапейрон (1799—1864) вывел уравнение состояния идеального газа, объединив законы Бойля — Мариотта и Гей-Люссака. Пусть некоторая масса газа занимает объем V1, имеет давление р1 и находится при температуре T1. Эта же масса газа в другом произвольном состоянии характеризуется параметрами р2, V2, T2 (рис. 63). Переход из состояния 1 в состояние 2 осуществляется в виде двух процессов: 1) изотермического (изотерма 1–1'), 2) изохорного (изохора 1'–2).
В соответствии с законами Бойля — Мариотта (41.1) и Гей-Люссака (41.5) запишем:
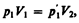 (42.1)
(42.1)
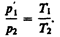 (42.2)
(42.2)
Исключив из уравнений (42.1) и (42.2) 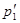 получим
получим
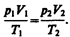
Так как состояния 1 и 2 были выбраны произвольно, то для данной массы газа величина pV/T остается постоянной, т. е.
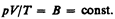 (42.3)
(42.3)
Выражение (42.3) являетсяуравнением Клапейрона, в котором В — газовая постоянная, различная для разных газов.
Русский ученый Д. И. Менделеев (1834—1907) объединил уравнение Клапейрона с законом Авогадро, отнеся уравнение (42.3) к одному молю, использовав молярный объем Vm. Согласно закону Авогадро, при одинаковых р и Т моли всех газов занимают одинаковый молярный объем Vm, поэтому постоянная В будет одинаковой для всех газов. Эта общая для всех газов постоянная обозначается R и называетсямолярном газовой постоянной. Уравнению
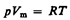 (42.4)
(42.4)
удовлетворяет лишь идеальный газ, и оно являетсяуравнением состояния идеального газа, называемым такжеуравнением Клапейрона — Менделеева.
Числовое значение молярной газовой постоянной определим из формулы (42.4), полагая, что моль газа находится при нормальных условиях (р0= 1,013×105 Па, T0=273,15 К, Vm=22,41×10–3 м3/моль): R=8,31 Дж/(моль×К).
От уравнения (42.4) для моля газа можно перейти к уравнению Клапейрона — Менделеева для произвольной массы газа. Если при некоторых заданных давлении и температуре один моль газа занимает молярный объем Vm, то при тех же условиях масса т газа займет объем V= (т/М)Vm, где М —молярная масса (масса одного моля вещества). Единица молярной массы — килограмм на моль (кг/моль). Уравнение Клапейрона — Менделеева для массы т газа
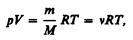 (42.5)
(42.5)
где n =m/M—количество вещества.

Часто пользуются несколько иной формой уравнения состояния идеального газа, вводя постоянную Больцмана:
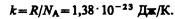
Исходя из этого уравнение состояния (42.4) запишем в виде
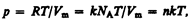
где NA/Vm = n — концентрация молекул (число молекул в единице объема). Таким образом, из уравнения
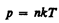 (42.6)
(42.6)
следует, что давление идеального газа при данной температуре прямо пропорционально концентрации его молекул (или плотности газа). При одинаковых температуре и давлении все газы содержат в единице объема одинаковое число молекул. Число молекул, содержащихся в 1 м3 газа при нормальных условиях, называется числом Лошмидта*:
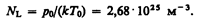
* И. Лошмидт (1821—1895) —австрийский химик и физик.
§ 43. Основное уравнение молекулярно-кинетической теории идеальных газов
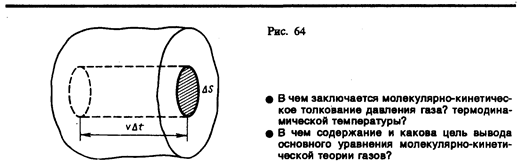
Для вывода основного уравнения молекулярно-кинетической теории рассмотрим одноатомный идеальный газ. Предположим, что молекулы газа движутся хаотически, число взаимных столкновений между молекулами газа пренебрежимо мало по сравнению с числом ударов о стенки сосуда, а соударения молекул со стенками сосуда абсолютно упругие. Выделим на стенке сосуда некоторую элементарную площадку DS (рис. 64) и вычислим давление, оказываемое на эту площадку. При каждом соударении молекула, движущаяся перпендикулярно площадке, передает ей импульс m0v – (– m0v) = 2m0v, где m0 — масса молекулы, v — ее скорость. За время Dt площадки DS достигнут только те молекулы, которые заключены в объеме цилиндра с основанием DS и высотой vDt (рис. 64). Число этих молекул равно nDSvDt (n — концентрация молекул).
Необходимо, однако, учитывать, что реально молекулы движутся к площадке DS под разными углами и имеют различные скорости, причем скорость молекул при каждом соударении меняется. Для упрощения расчетов хаотическое движение молекул заменяют движением вдоль трех взаимно перпендикулярных направлений, так что в любой момент времени вдоль каждого из них движется 1/3 молекул, причем половина молекул 1/6 движется вдоль данного направления в одну сторону, половина — в противоположную. Тогда число ударов молекул, движущихся в заданном направлении, о площадку DS будет 1/6nDSvDt. При столкновении с площадкой эти молекулы передадут ей импульс
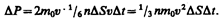
Тогда давление газа, оказываемое им на стенку сосуда,
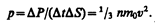 (43.1)
(43.1)
Если газ в объеме V содержит N молекул, движущихся со скоростями v1, v2, ..., vN, то целесообразно рассматриватьсреднюю квадратную скорость
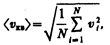 (43.2)
(43.2)
характеризующую всю совокупность молекул газа.
Уравнение (43.1) с учетом (43.2) примет вид
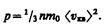 (43.3)
(43.3)
Выражение (43.3) называетсяосновным уравнением молекулярно-кинетической теории идеальных газов. Точный расчет с учетом движения молекул по всевозможным направлениям дает ту же формулу.
Учитывая, что n =N / V, получим
 (43.4)
(43.4)
или
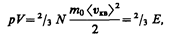 (43.5)
(43.5)
где Е — суммарная кинетическая энергия поступательного движения всех молекул газа.
Так как масса газа m=Nm0, то уравнение (43.4) можно переписать в виде
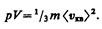
Для одного моля газа т=М (М — молярная масса), поэтому
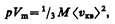
где Vm — молярный объем. С другой стороны, по уравнению Клапейрона — Менделеева, pVm=RT. Таким образом,
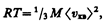
откуда
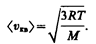 (43.6)
(43.6)
Так как M=m0NА, где т0 — масса одной молекулы, a NА — постоянная Авогадро, то из уравнения (43.6) следует, что
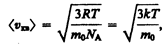 (43.7)
(43.7)
где k=R/NА — постоянная Больцмана. Отсюда найдем, что при комнатной температуре молекулы кислорода имеют среднюю квадратичную скорость 480 м/с, водорода — 1900 м/с. При температуре жидкого гелия те же скорости будут соответственно 40 и 160 м/с.
Средняя кинетическая энергия поступательного движения одной молекулы идеального газа
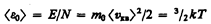 (43.8)
(43.8)
(использовали формулы (43.5) и (43.7)) пропорциональна термодинамической температуре и зависит только от нее. Из этого уравнения следует, что при Т=0 <e0>=0, т. е. при 0К прекращается поступательное движение молекул газа, а следовательно, его давление равно нулю. Таким образом, термодинамическая температура является мерой средней кинетической энергии поступательного движения молекул идеального газа, и формула (43.8) раскрывает молекулярно-кинетическое толкование температуры.
§ 44. Закон Максвелла о распределении молекул идеального газа по скоростям и энергиям теплового движения
При выводе основного уравнения молекулярно-кинетической теории молекулам задавали различные скорости. В результате многократных соударений скорость каждой молекулы изменяется по модулю и направлению. Однако из-за хаотического движения молекул все направления движения являются равновероятными, т. е. в любом направлении в среднем движется одинаковое число молекул.
По молекулярно-кинетической теории, как бы ни изменялись скорости молекул при столкновениях, средняя квадратичная скорость молекул массой т0 в газе, находящемся в состоянии равновесия при Т= const. остается постоянной и равной 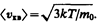
Это объясняется тем, что в газе, находящемся в состоянии равновесия, устанавливается некоторое стационарное, не меняющееся со временем распределение молекул по скоростям, которое подчиняется вполне определенному статистическому закону. Этот закон теоретически выведен Дж. Максвеллом.
При выводе закона распределения молекул по скоростям Максвелл предполагал, что газ состоит из очень большого числа N тождественных молекул, находящихся в состоянии беспорядочного теплового движения при одинаковой температуре. Предполагалось также, что силовые поля на газ не действуют.
Закон Максвелла описывается некоторой функцией f(v), называемой функцией распределения молекул по скоростям. Если разбить диапазон скоростей молекул на малые интервалы, равные dv, то на каждый интервал скорости будет приходиться некоторое число молекул dN(v), имеющих скорость, заключенную в этом интервале. Функция f(v) определяет относительное число молекул dN(v)/N, скорости которых лежат в интервале от v до v+dv, т. е.
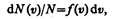
откуда
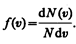
Применяя методы теории вероятностей. Максвелл нашел функцию f(v) — закон о распределеня молекул идеального газа по скоростям:
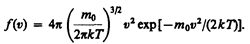 (44.1)
(44.1)
Из (44.1) видно, что конкретный вид функции зависит от рода газа (от массы молекулы) и от параметра состояния (от температуры Т).
График функции (44.1) приведен на рис. 65. Так как при возрастании v множитель exp[–m0v2/(2kT)] уменьшается быстрее, чем растет множитель v2, то функция f(v), начинаясь от нуля, достигает максимума при vB, и затем асимптотически стремится к нулю. Кривая несимметрична относительно vB.
Относительное число молекул dN(v)/N, скорости которых лежат в интервале от v до v+dv, находится как площадь заштрихованной полоски на рис. 65. Площадь, ограниченная кривой распределения и осью абсцисс, равна единице. Это означает, что функция f(v) удовлетворяет условию нормировки
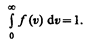
Скорость, при которой функция распределения молекул идеального газа по скоростям максимальна, называется наиболее вероятной скоростью. Значение наиболее вероятной скорости можно найти продифференцировав выражение (44.1) (постоянные множители опускаем) по аргументу v, приравняв результат нулю и используя условие для максимума выражения f(v):
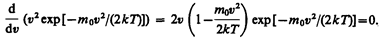
Значения v=0 и v=¥ соответствуют минимумам выражения (44.1), а значение v, при котором выражение в скобках становится равным нулю, и есть искомая наиболее вероятная скорость vB:
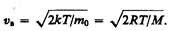 (44.2)
(44.2)

Из формулы (44.2) следует, что при повышении температуры максимум функции распределения молекул по скоростям (рис. 66) сместится вправо (значение наиболее вероятной скорости становится больше). Однако площадь, ограниченная кривой, остается неизменной, поэтому при повышении температуры кривая распределения молекул по скоростям будет растягиваться и понижаться.
Средняя скорость молекулы <v> (средняя арифметическая скорость) определяется по формуле
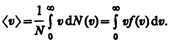
Подставляя сюда f(v) и интегрируя, получаем
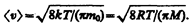 (44.3)
(44.3)
Скорости, характеризующие состояние газа: 1) наиболее вероятная 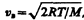 2) средняя
2) средняя 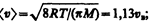 3) средняя квадратичная
3) средняя квадратичная 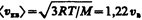 (рис. 65). Исходя из распределения молекул по скоростям
(рис. 65). Исходя из распределения молекул по скоростям
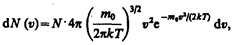 (44.4)
(44.4)
можно найти распределение молекул газа по значениям кинетической энергии e. Для этого перейдем от переменной v к переменной e=m0v2/2. Подставив в (44.4) v= 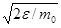 и dv=
и dv= 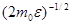 de , получим
de , получим
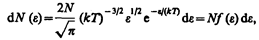
где dN(e) — число молекул, имеющих кинетическую энергию поступательного движения, заключенную в интервале от e до e + de.
Таким образом, функция распределения молекул по энергиям теплового движения
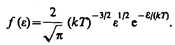
Средняя кинетическая энергия <e> молекулы идеального газа
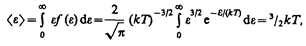
т. е. получили результат, совпадающий с формулой (43.8).

§ 45. Барометрическая формула. Распределение Больцмана
При выводе основного уравнения молекулярно-кинетической теории газов и максвелловского распределения молекул по скоростям предполагалось, что на молекулы газа внешние силы не действуют, поэтому молекулы равномерно распределены по объему. Однако молекулы любого газа находятся в потенциальном поле тяготения Земли. Тяготение, с одной стороны, и тепловое движение молекул — с другой, приводят к некоторому стационарному состоянию газа, при котором давление газа с высотой убывает.
Выведем закон изменения давления с высотой, предполагая, что поле тяготения однородно, температура постоянна и масса всех молекул одинакова. Если атмосферное давление на высоте h равно р (рис. 67), то на высоте h+dh оно равно p+dp (при dh>0 dp<0, так как давление с высотой убывает). Разность давлений р и p+dp равна весу газа, заключенного в объеме цилиндра высотой dh с основанием площадью 1 м2:

где r — плотность газа на высоте h (dh настолько мало, что при изменении высоты в этом пределе плотность газа можно считать постоянной). Следовательно,
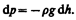 (45.1)
(45.1)
Воспользовавшись уравнением состояния идеального газа pV=(m/M) RT (т — масса газа, М — молярная масса газа), находим, что
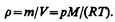
Подставив это выражение в (45.1), получим
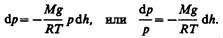
С изменением высоты от h1 до h2 давление изменяется от р1 до р2 (рис. 67), т. е.
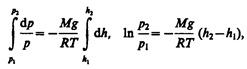
или
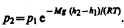 (45.2)
(45.2)
Выражение (45.2) называетсябарометрической формулой. Она позволяет найти атмосферное давление в зависимости от высоты или, измерив давление, найти высоту: Так как высоты обозначаются относительно уровня моря, где давление считается нормальным, то выражение (45.2) может быть записано в виде
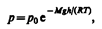 (45.3)
(45.3)
где р — давление на высоте h.
Прибор для определения высоты над земной поверхностью называетсявысотомером (илиальтиметром). Его работа основана на использовании формулы (45.3). Из этой формулы следует, что давление с высотой убывает тем быстрее, чем тяжелее газ.
Барометрическую формулу (45.3) можно преобразовать, если воспользоваться выражением (42.6) p=nkT:
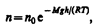
где n – концентрация молекул на высоте h, n0 – то же, на высоте h=0. Так как M=m0NA (NA – постоянная Авогадро, т0 – масса одной молекулы), a R=kNA, то
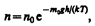 (45.4)
(45.4)
где m0gh=П — потенциальная энергия молекулы в поле тяготения, т. е.
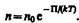 (45.5)
(45.5)
Выражение (45.5) называется распределением Больцмана для внешнего потенциального поля. Из вето следует, что при постоянной температуре плотность газа больше там, где меньше потенциальная энергия его молекул.
Если частицы имеют одинаковую массу и находятся в состоянии хаотического теплового движения, то распределение Больцмана (45.5) справедливо в любом внешнем потенциальном поле, а не только в поле сил тяжести.
§ 46. Среднее число столкновений и средняя длина свободного пробега молекул
Молекулы газа, находясь в состоянии хаотического движения, непрерывно сталкиваются друг с другом. Между двумя последовательными столкновениями молекулы проходят некоторый путь l, который называетсядлиной свободного пробега. В общем случае длина пути между последовательными столкновениями различна, но так какмы имеемдело с огромным числом молекул и они находятся в беспорядочном движении, то можно говорить осредней длине свободного пробега молекул <l>.
Минимальное расстояние, на которое сближаются при столкновении центры двух молекул, называетсяэффективным диаметром молекулы d (рис. 68). Он зависит от скорости сталкивающихся молекул, т. е. от температуры газа (несколько уменьшается с ростом температуры).
Так как за 1 с молекула проходит в среднем путь, равный средней арифметической скорости <v>, и если <z> — среднее число столкновений, испытываемых одной молекулой газа за 1 с, то средняя длина свободного пробега
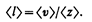
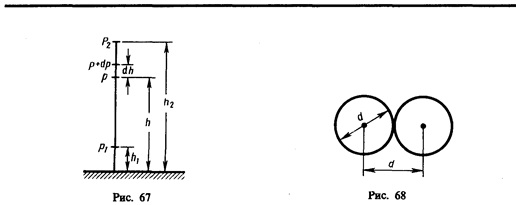
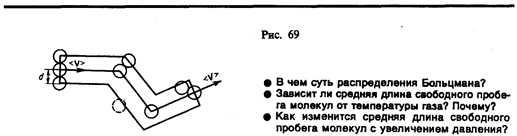
Для определения <z> представим себе молекулу в виде шарика диаметром d, которая движется среди других «застывших» молекул. Эта молекула столкнется только с теми молекулами, центры которых находятся на расстояниях, равных или меньших d, т. е. лежат внутри «ломаного» цилиндра радиусом d (рис. 69).
Среднее число столкновений за 1 с равно числу молекул в объеме «ломаного» цилиндра:
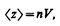
где п — концентрация молекул, V = pd2 <v> <v> — средняя скорость молекулы или путь, пройденным ею за 1 с). Таким образом,среднее число столкновений
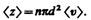
Расчеты показывают, что при учете движения других молекул
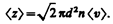
Тогда средняя длина свободного пробега
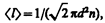
т. е. <l> обратно пропорциональна концентрации n молекул. С другой стороны, из (42.6) следует, что при постоянной температуре n пропорциональна давлению р. Следовательно,
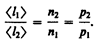
§ 47. Опытное обоснование молекулярно-кинетической теории
Рассмотрим некоторые явления, экспериментально подтверждающие основные положения и выводы молекулярно-кинетической теории.
1. Броуновское движение. Шотландский ботаник Р. Броун (1773—1858), наблюдая под микроскопом взвесь цветочной пыльцы в воде, обнаружил, что частицы пыльцы оживленно и беспорядочно двигались, то вращаясь, то перемещаясь с места на место, подобно пылинкам в солнечном луче. Впоследствии оказалось, что подобное сложное зигзагообразное движение характерно для любых частиц малых размеров (»1 мкм), взвешенных в газе или жидкости. Интенсивность этого движения, называемого броуновским, повышается с ростом температуры среды, с уменьшением вязкости и размеров частиц (независимо от их химической природы). Причина броуновского движения долго оставалась неясной. Лишь через 80 лет после обнаружения этого эффекта ему было дано объяснение: броуновское движение взвешенных частиц вызывается ударами молекул среды, в которой частицы взвешены. Так как молекулы движутся хаотически, то броуновские частицы получают толчки с разных сторон, поэтому и совершают движение столь причудливой формы. Таким образом, броуновское движение является подтверждением выводов молекулярно-кинетической теории о хаотическом (тепловом) движении атомов и молекул.
2. Опыт Штерна. Первое экспериментальное определение скоростей молекул выполнено немецким физиком О. Штерном (1888—1970). Его опыты позволили также оценить распределение молекул по скоростям. Схема установки Штерна представлена на рис. 70. Вдоль оси внутреннего цилиндра с щелью натянута платиновая проволока, покрытая слоем серебра, которая нагревается током при откачанном воздухе. При нагревании серебро испаряется. Атомы серебра, вылетая через щель, попадают на внутреннюю поверхность второго цилиндра, давая изображение щели О. Если прибор привести во вращение вокруг общей оси цилиндров, то атомы серебра осядут не против щели, а сместятся от точки О на некоторое расстояние s. Изображение щели получается размытым. Исследуя толщину осажденного слоя, можно оценить распределение молекул по скоростям, которое соответствует максвелловскому распределению.
Дата добавления: 2017-04-20; просмотров: 747;
