Сухие марганцево-цинковые (МЦ) элементы
Первичные сухие ХИТ выпускаются промышленностью с не проливающимся электролитом (загущенным крахмалом, мукой, карбоксиметилцеллюлозой (КМЦ)), отсюда и название «сухие». Типичным представителем сухих ХИТ являются МЦ элементы стаканчиковой и галетной конструкций, в которых используют солевые (NH4Cl) и щелочные (NaOH, KOH) электролиты. Схематически их можно представить так:
 Zn|NH4Cl|MnO2(C)
Zn|NH4Cl|MnO2(C) 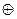 и
и  Zn|KOH|MnO2(C)
Zn|KOH|MnO2(C) 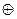
Токообразующие реакции на положительном электроде зависят от рН электролита. При рН ≤ 4,5…5 происходит восстановление MnO2 по реакциям:
2MnO2 + 2H+ + 2 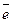 → 2MnOOH (4.а)
→ 2MnOOH (4.а)
2MnOOH + 2H+ → Mn2+ + 2H2O + MnO2 (4.б)
 MnO2 +4Н++ 2
MnO2 +4Н++ 2 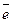 → Mn2+ + 2H2O
→ Mn2+ + 2H2O
Равновесный потенциал суммарной реакции снижается на 0,118 В при повышении рН среды на единицу. Так как подкисление раствора возможно только за счет гидролиза, образующегося в небольшом количестве хлорида цинка (ZnCl2 + H2O → ZnOHCl + HCl), электролит в процессе разряда элемента подщелачивается, что приводит к довольно крутому падению кривой (рис. 4.1, кривая 1) МЦ элемента, которая определяется, в основном, изменением потенциала положительного электрода.
В случае слабощелачных электролитов восстановление MnO2 до манганита по реакции MnO2 + H2O + 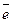 → MnOOH + OH-; приводит к более плавному уменьшению потенциала при разряде (рис. 4.1, кривая 2) – всегда на 0,059 В при увеличении рН на единицу.
→ MnOOH + OH-; приводит к более плавному уменьшению потенциала при разряде (рис. 4.1, кривая 2) – всегда на 0,059 В при увеличении рН на единицу.
При этом восстановление MnO2 происходит в твердой фазе с участием ионов раствора на границе раздела фаз, поэтому потенциал электрода зависит также и от активностей MnО2 и MnOOH.

Рис. 4.1 Кривая разряда МЦ элемента
На поверхности зерна положительной активной массы, в которую для повышения ее электрической проводимости добавляют графит (рис. 4.2), образуется фаза переменного состава хMnOOH(1-x)MnO2 по типу твердого раствора без искажения кристаллической решетки. После насыщения ею поверхностного слоя активной массы система становится неравновесной, идет диффузия протонов вглубь зерна, постепенно восстанавливаются глубинные слои активной массы.
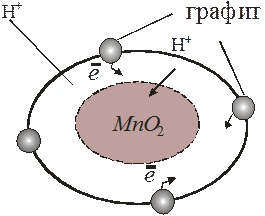
Рис. 4.2 Активная масса положительного электрода МЦ элемента
Так как диффузия в твердой фазе замедлена, полностью концентрация манганита в поверхностном и в глубинном слоях активной массы может выровняться только после включения нагрузки, во время “отдыха” элемента.
Таким образом, МЦ элементы выгоднее эксплуатировать в прерывистом, а не в непрерывном режиме разряда. Достигаемое после “отдыха” напряжение разомкнутой цепи будет тем меньше, чем дольше разряжался элемент.
Качество МЦ элементов (срок службы, разрядные характеристики, саморазряд) во многом определяется составом и качеством активной массы положительного электрода (степенью активации пиролюзита или электролитической двуокиси марганца, отсутствием вредных примесей и т.п.)
На отрицательном электроде в солевой и слабощелочной средах при разряде элемента идут реакции
Zn + H2O → ZnO + 2H+ + 2 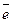 (4.в)
(4.в)
Zn + 2H2O → Zn(OH)2 + 2H+ + 2 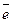 (4.г)
(4.г)
Из-за вторичных процессов в порах электродов и сепаратора образуются осадки малорастворимых аммиакатов [Zn(NH3)2]Cl2 и [Zn(NH3)4]Cl2.
Суммарные токообразующие реакции в этих электролитах
2MnO2 + 2NH4Cl + Zn → 2MnOOH + [Zn(NH3)2]Cl2 (4.д)
и
2MnO2 + Zn + 2H2O + 2OH- → 2MnOOH + [Zn(OH)4]2- (4.е)
Анодный процесс на цинковом электроде в избытке щелочного электролита идет по так называемому первичному механизму с образованием цинкатов:
Zn + 4OH- → [Zn(OH)4]2- + 2 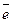 . (4.ж)
. (4.ж)
Повышение анодной плотности тока в этом случае приводит к пассивации монолитных гладких электродов. Применение пористых прессованных цинковых электродов, истинная поверхность которых в сотни раз превышает геометрическую, позволяет получать большие (габаритные) плотности тока – от 1 кА/м2 (0,1 А/см2) и выше. Такие электроды в отличие от монолитных не пассивируются, и при пониженных температурах, возможен также частичный их подзаряд. Прессованные цинковые электроды механически непрочны и поэтому применяются в элементах матричного типа и аккумуляторах. Расход раствора электролита при вторичном механизме очень мал (1,5 – 2 мл/А·ч). Им только пропитывают сепарацию и электроды.
Саморазряд МЦ элементов (~ 30% в год) происходит вследствие коррозии цинка по реакциям:
Zn + 2NH4Cl → [Zn(NH3)2]Cl2 + H2;
Zn + 2H2O → Zn(OH)2 + H2; (4.з)
2Zn + O2 + 2H2O → 2Zn(OH)2,
а также вследствие химического окисления хлорида аммония. Быстрому саморазряду способствуют примеси веществ, легко подвергающихся окислению и восстановлению (например, ионов Fe2+ и Fe3+), а также образование мостиков из-за вытекания или высыхания электролита, вызывающих короткое замыкание в элементе. Для уменьшения коррозии применяют цинк, легированный свинцом, или очень чистый цинк (99,9%), амальгамируют его (добавками в электролит сулемы), или используют ингибиторы коррозии.
Дата добавления: 2017-01-29; просмотров: 1471;
