Диффузионные процессы в металле.
Диффузия – перемещение атомов в кристаллическом теле на расстояния, превышающие средние межатомные данного вещества.
Диффузия, сопровождающаяся изменением концентрации, происходит в сплавах или в металлах с повышенным содержанием примесей и называется диффузией или гетеродиффузией.
Перемещения атомов, не связанных с изменением концентрации в различных объемах, называется самодиффузией.
В основе процесса диффузии в кристаллах лежит атомный механизм, при котором каждый атом совершает ряд перемещений между различными равновесными положениями в кристаллической решетке. Для описания процесса диффузии в твердом кристаллическом теле предложено несколько возможных механизмов:
циклический;
объемный,
вакансионный;
межузельный.
При циклической диффузии (рис. 1.7, а) совместно перемещаются группы атомов (атомы 1-4). Такая диффузия не требует больших затрат энергии, но маловероятна.
При обменном механизме диффузия (рис. 1.7, б) атомы меняются местами (атомы 1-2).
В металлах и сплавах диффузия преимущественно осуществляется по вакансионному механизму (рис. 1.7, в), при этом происходит замещение вакансий и их перемещений вглубь металла.
При диффузии в металле элементов с малым атомным радиусом (углерод, азот, водород, кислород) происходит диффузии по межузельному механизму (рис. 1.7, г).
Рис. 1.7. Перемещение атомов в кристаллической решетке металлов:
а - циклическая диффузия;
б - обменный механизм диффузии;
в - вакансионная диффузия;
г - межузельная диффузия;
1, 2, 3, 4 – перемещающиеся атомы.
Наиболее легко диффузия протекает по поверхности и границам зерен, где сосредоточены дефекты кристаллического строения (вакансии, дислокации).
Скорость диффузии – количество вещества, продиффундировавшего через единицу площади поверхности раздела за единицу времени.
Количество диффундирующего вещества в единицу времени «m», зависит от градиента концентраций «dc/dx» элемента в направлении, нормальном к поверхности раздела и пропорционально коэффициенту диффузии «D» м2/сек:
m = - D dc/dx,
где dc – концентрация;
dx – расстояние в выбранном направлении.
Знак «минус» указывает, что диффузия (самодиффузия) протекает в направлении от объемов с большей концентрацией к объемам с меньшей концентрацией.
Коэффициент диффузии D– количество вещества, продиффундировавшего через единицу времени при перепаде концентраций, равной единице.
Он зависит то природы сплава, размеров зерна и особенно сильно от температуры.
Температурная зависимость коэффициента диффузии описывается экспоненциальным уравнением:
D=Do e -Q/RT,
где Do –множитель, величина которого определяется типом кристаллической решетки;
R – газовая постоянная;
T – температура,
Q – энергия активации диффузии. Энергия активации диффузии характеризует энергию связи атомов в кристаллической решетке и очень сильно влияет на коэффициент диффузии.
Диффузия лежит в основе большинства фундаментальных процессов, протекающих в металлах и сплавах, таких как кристаллизация, фазовые превращения, рекристаллизация, деформация, химико-термическая обработка и других.
Лекция 2. Формирование структуры металлов и сплавов при кристаллизации –2 часа
Первичная кристаллизация, степень переохлаждения. Механизм и закономерности кристаллизации металлов. Самопроизвольное (спонтанное) и гетерогенное образование центров кристаллизации. Модифицирование. Влияние размера зерна на свойства металла. Строение металлического слитка. Ликвация дендритная и зональная.
Построение диаграммы состояния двойных сплавов методом термического анализа
Любое вещество может находиться в четырех агрегатных состояниях: твердом, жидком, газообразном и плазменном. Переход из одного состояния в другое возможен при условии, если новое состояние является более устойчивым, т.е. обладает наименьшим запасом свободной энергии.
Свободная энергия изменяется по сложному закону различно для жидкого и кристаллического состояний. Характер изменения свободной энергии жидкого и твердого состояний с изменением температуры показан на рис. 2.1.
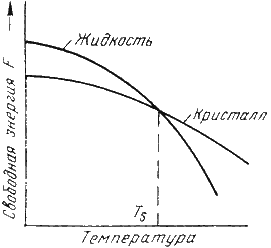
Рис.2.1. Изменение свободной энергии в зависимости от температуры
В соответствии с этой схемой выше температуры ТS вещество должно находиться в жидком состоянии, а ниже ТS – в твердом.
При температуре равной ТS жидкая и твердая фаза обладают одинаковой энергией, металл в обоих состояниях находится в равновесии, поэтому две фазы могут существовать одновременно бесконечно долго.
Температура ТS – равновесная или теоретическая температура кристаллизации.
Для начала процесса кристаллизации необходимо, чтобы процесс был термодинамически выгоден системе и сопровождался уменьшением свободной энергии системы. Это возможно при охлаждении жидкости ниже температуры ТS.
Температура, при которой практически начинается кристаллизация называется фактической температурой кристаллизации.
Охлаждение жидкости ниже равновесной температуры кристаллизации называется переохлаждением, которое характеризуется степенью переохлаждения( 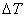 ):
):
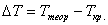
Степень переохлаждения зависит от природы металла, от степени его загрязненности (чем чище металл, тем больше степень переохлаждения), от скорости охлаждения (чем выше скорость охлаждения, тем больше степень переохлаждения).
Рассмотрим переход металла из жидкого состояния в твердое.
При нагреве всех кристаллических тел наблюдается четкая граница перехода из твердого состояния в жидкое. Такая же граница существует при переходе из жидкого состояния в твердое.
Первичная кристаллизация– это процесс перехода сплава из жидкого состояния в твердое.
Кристаллизация протекает в условиях, когда система переходит к термодинамически более устойчивому состоянию с минимумом свободной энергии.
Процесс перехода металла из жидкого состояния в кристаллическое можно изобразить кривыми в координатах время – температура. Кривая охлаждения чистого металла представлена на рис. 2.2

Рис.2.2. Кривая охлаждения чистого металла
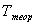 – теоретическая температура кристаллизации;
– теоретическая температура кристаллизации;
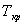 . – фактическая температура кристаллизации.
. – фактическая температура кристаллизации.
Процесс кристаллизации чистого металла:
До точки 1 охлаждается металл в жидком состоянии, процесс сопровождается плавным понижением температуры. На участке 1 – 2 идет процесс кристаллизации, сопровождающийся выделением тепла, которое называется скрытой теплотой кристаллизации. Оно компенсирует рассеивание теплоты в пространство, и поэтому температура остается постоянной. После окончания кристаллизации в точке 2 температура снова начинает снижаться, металл охлаждается в твердом состоянии.
Дата добавления: 2017-01-13; просмотров: 6809;
