Металлическое состояние, основные типы кристаллических решеток металлов.
Вклад ученых в развитие металловедения.
Создание научных основ металловедения принадлежит Чернову Д.К., который установил критические температуры фазовых превращений в сталях и их связь с количеством углерода в сталях. Этим были заложены основы для создания диаграммы состояния железоуглеродистых сплавов.
Чернов Д.К. открыл аллотропические превращения в стали и заложил фундамент термической обработки стали.
Он изучил кристаллизацию стали и основы теории литья.
Великий русский металлург Аносов П.П. впервые применил микроскоп для исследования структуры металлов. Ему принадлежит приоритет в создании легированных сталей.
Он разработал теорию и технологию изготовления клинков из булатной стали.
В настоящее время для структурного анализа, кроме рентгеновских лучей, используют электроны. Электронная оптика позволила усовершенствовать микроскопию. В настоящее время на электронных микроскопах полезное максимальное увеличение доведено до 100000 раз.
Особенно интенсивно развивается металловедение в последние десятилетия. Это объясняется потребностью в новых материалах для исследования космоса, развития электроники, атомной энергетики.
Основными направлениями в развитии металловедения являются:
1. разработка способов производства чистых и сверхчистых металлов, свойства которых сильно отличаются от свойств металлов технической чистоты
2. создание материалов с заранее рассчитанными свойствами применительно к заданным параметрам и условиям работы. Большое внимание уделяется изучению металлов в экстремальных условиях (низкие и высокие температуры и давление).
3. создание неметаллических материалов (пластмасс, керамики, материалов порошковой металлургии) и композиционных материалов.
4. разработка «умных материалов».
Атомно-кристаллическое строение металлов
Металл состоит из атомов, которые представляют собой положительно заряженные ядра, вокруг которых по орбитам вращаются электроны. На последнем уровне число электронов невелико, и они слабо связаны с ядром. Эти электроны имеют возможность перемещаться по всему объему металла и называются свободными электронами. Они являются носителями электрических зарядов и представляют собой «электронный газ», определяющий пластичность, теплопроводность и электропроводность металла.
Атомы в металлах расположены упорядоченно и образуют кристалл, т.е. металлы имеют кристаллическое строение.
Металлическое состояние, основные типы кристаллических решеток металлов.
Металлическое состояние характеризуется следующими признаками:
· высокая отражательная способность (металлический блеск);
· высокая пластичность;
· высокая теплопроводность и электропроводность;
· положительный температурный коэффициент линейного расширения.
Из большого числа упорядоченно расположенных атомов всегда можно выделить элементарный объем, который многократно повторяется и образует элементарную ячейку, которую называют кристаллической решеткой (к.р.).
Кристаллическая решетка (элементарная ячейка) – этовоображаемая пространственная решетка из минимального числа атомов, которая многократно повторяясь, образует кристалл
Основными параметрами кристаллической решетки являются:
· период решётки – расстояния между центрами ближайших атомов;
· координационное число (К) – число атомов, расположенных на ближайшем одинаковом расстоянии от любого атома в решетке;
·базис решетки – количество атомов, приходящихся на одну элементарную ячейку решетки.
Основные типы кристаллических решеток (рисунок 1.1):
1. Объемно - центрированная кубическая (ОЦК), атомы располагаются в вершинах куба и в его центре (V, W, Ti, Feα) (рисунок 1.1,а)
2. Гранецентрированная кубическая (ГЦК), атомы рассполагаются в вершинах куба и в центре каждой грани (Ag, Au, Feγ) (рисунок 1.1,б)
3. Гексагональная плотноупакованная (ГПУ), в основании которой лежит шестиугольник, в вершинах которого и в центре располагаются атомы и три атома в центре боковых граней через одну (Zn,Al,Mg) (рис. 1.1,в).
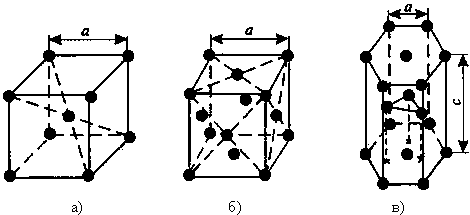
Рис.1.1. Основные типы кристаллических решеток:
а – объемно-центрированная кубическая; б – гранецентрированная кубическая; в – гексагональная плотноупакованная.
Аморфные вещества
Аморфные вещества – вещества, в которых атомы располагаются хаотично (произвольно).
Эти материалы не имеют определенной температуры плавления, как у металлов. При нагревании плавно переходят в вязко-текучее состояние. Например, силикатное стекло.
В металлических сплавах можно получить аморфную структуру при условии сверхбыстрого охлаждения из жидкого состояния (104…106 °С/с). Такие сплавы обладают очень высокой износостойкостью и отсутствием магнитных потерь при перемагничивании. Достаточно широко применяются в технике. Сплавы называются «металлическими стеклами».
Дата добавления: 2017-01-13; просмотров: 2823;
