Ионное произведение воды. Водородный показатель
Вода – слабый электролит – диссоциирует, образуя ионы Н+ и OH¯. Эти ионы гидратированы, т. е. соединены с несколькими молекулами воды, но для простоты их записывают в негидратированной форме
Н2O ↔ Н+ + OH¯.
На основании закона действия масс, для этого равновесия:
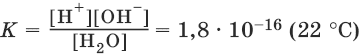
Концентрацию молекул воды [Н2O], т. е. число молей в 1 л воды, можно считать постоянной и равной [Н2O] = 1000 г/л : 18 г/моль = 55,6 моль/л. Отсюда:
К • [Н2O] = К (Н2O) = [Н+] • [OH¯] = 10-14 (22°C).
Ионное произведение воды– произведение концентраций [Н+] и [OH¯] – есть величина постоянная при постоянной температуре и равная 10-14 при 22°C.
Ионное произведение воды увеличивается с увеличением температуры.
Водородный показатель рН– отрицательный логарифм концентрации ионов водорода: рН = – lg[H+]. Аналогично: pOH = – lg[OH¯].
Логарифмирование ионного произведения воды дает: рН + рOH = 14.
Величина рН характеризует реакцию среды.
Если рН = 7, то [Н+] = [OH¯] – нейтральная среда.
Если рН < 7, то [Н+] > [OH¯] – кислотная среда.
Если рН > 7, то [Н+] < [OH¯] – щелочная среда.
Буферные растворы
Буферные растворы – растворы, имеющие определенную концентрацию ионов водорода. рН этих растворов не меняется при разбавлении и мало меняется при добавлении небольших количеств кислот и щелочей.
I. Раствор слабой кислоты НА, концентрация – скисл, и ее соли с сильным основанием ВА, концентрация – ссоли. Например, ацетатный буфер – раствор уксусной кислоты и ацетата натрия: CH3COOH + CHgCOONa.
рН = рКкисл + lg(ссоли/скисл).
II. Раствор слабого основания ВOH, концентрация – сосн, и его соли с сильной кислотой ВА, концентрация – ссоли. Например, аммиачный буфер – раствор гидроксида аммония и хлорида аммония NH4OH + NH4Cl.
рН = 14 – рКосн – lg(ссоли/сосн).
Гидролиз солей
Гидролиз солей – взаимодействие ионов соли с водой с образованием слабого электролита.
Примеры уравнений реакций гидролиза.
I. Соль образована сильным основанием и слабой кислотой:
Na2CO3 + H2O ↔ NaHCO3 + NaOH
2Na+ + CO32- + H2O ↔ 2Na+ + HCO3¯ + OH¯
CO32- + H2O ↔ HCO3¯ + OH¯, pH > 7, щелочная среда.
По второй ступени гидролиз практически не идет.
II. Соль образована слабым основанием и сильной кислотой:
AlCl3 + H2O ↔ (AlOH)Cl2 + HCl
Al3+ + ЗCl¯ + H2O ↔ AlOH2+ + 2Cl¯ + Н+ + Cl¯
Al3+ + H2O ↔ AlOH2+ + Н+, рН < 7.
По второй ступени гидролиз идет меньше, а по третьей ступени практически не идет.
III. Соль образована сильным основанием и сильной кислотой:
KNO3 + H2O ≠
К+ + NO3¯ + Н2O ≠ нет гидролиза, рН ≈ 7.
IV. Соль образована слабым основанием и слабой кислотой:
CH3COONH4 + H2O ↔ CH3COOH + NH4OH
CH3COO¯ + NH4+ + H2O ↔ CH3COOH + NH4OH, рН = 7.
В ряде случаев, когда соль образована очень слабыми основаниями и кислотами, идет полный гидролиз. В таблице растворимости у таких солей символ – «разлагаются водой»:
Al2S3 + 6Н2O = 2Al(OH)3↓ + 3H2S↑
Возможность полного гидролиза следует учитывать в обменных реакциях:
Al2(SO4)3 + 3Na2CO3 + 3H2O = 2Al(OH)3↓ + 3Na2SO4 + 3CO2↑
Степень гидролиза h– отношение концентрации гидролизованных молекул к общей концентрации растворенных молекул.
Для солей, образованных сильным основанием и слабой кислотой:
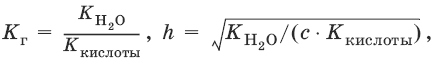
[OH¯] = ch, рOH = – lg[OH¯], рН = 14 – рOH.
Из выражения следует, что степень гидролиза h (т. е. гидролиз) увеличивается:
а) с увеличением температуры, так как увеличивается K(H2O);
б) с уменьшением диссоциации кислоты, образующей соль: чем слабее кислота, тем больше гидролиз;
в) с разбавлением: чем меньше с, тем больше гидролиз.
Для солей, образованных слабым основанием и сильной кислотой
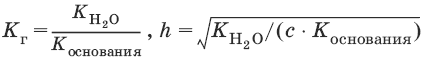
[Н+] = ch, рН = – lg[H+].
Для солей, образованных слабым основанием и слабой кислотой
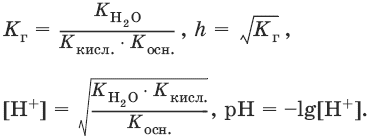
Дата добавления: 2016-04-23; просмотров: 1169;
