СИСТЕМНАЯ ПРОГРЕССИРУЮЩАЯ ДЕЗОРГАНИЗАЦИЯ СОЕДИНИТЕЛЬНОЙ ТКАНИ КАК СЛЕДСТВИЕ ЕЕ ДЕСТРУКЦИИ
СТРОМАЛЬНО-СОСУДИСТЫЕ ДИСТРОФИИ: МОРФОЛОГИЯ СИСТЕМНОЙ ПРОГРЕССИРУЮЩЕЙ ДЕЗОРГАНИЗАЦИИ СОЕДИНИТЕЛЬНОЙ ТКАНИ
Стромально-сосудистые (мезенхимальные) дистрофии развиваются в результате нарушений обмена в соединительной ткани и выявляются в строме органов и стенках сосудов. Стромально-сосудистые дистрофии развиваются на территории гистиона, который, как известно, образован отрезком микроциркуляторного русла с окружающими его элементами соединительной ткани (основное вещество, волокнистые структуры, клетки) и нервными волокнами. Понятным становится в связи с этим преобладание среди механизмов развития стромально-сосудистых дистрофий нарушений транспортных систем трофики, общности морфогенеза, возможности не только сочетания различных видов дистрофий, но и перехода одного вида в другой.
Эти особенности стромально-сосудистых дистрофий ярко выражены при диспротеинозах. Они-то и составляют сущность системной прогрессирующей дезорганизации соединительной ткани.
В одних случаях в основе этой дезорганизации лежит прогрессирующая деструкция соединительной ткани — прогрессирующая дезорганизация как следствие деструкции соединительной ткани, в других — синтез аномального белка — прогрессирующая дезорганизация как следствие синтеза аномального белка в соединительной ткани.
СИСТЕМНАЯ ПРОГРЕССИРУЮЩАЯ ДЕЗОРГАНИЗАЦИЯ СОЕДИНИТЕЛЬНОЙ ТКАНИ КАК СЛЕДСТВИЕ ЕЕ ДЕСТРУКЦИИ
Этот вид системной дезорганизации обусловлен в большинстве случаев инфекцией, чаще стрептококковой, и тяжелыми иммунными (аутоиммунными) нарушениями, которые наиболее яр-
ко выражены при ревматических заболеваниях. Определенное значение в их возникновении имеют и наследственные факторы.
Начальные изменения системной дезорганизации соединительной ткани находят впарапластической субстанции (основное вещество соединительной ткани), где накапливаются гликозаминогликаны (хромотропные вещества), главным образом за счет гидрофильных гиалуроновых структур, а также плазменные белки, преимущественно глобулины. Накопление гликозаминогликанов связано с активной деятельностью фиб-робластов, а глобулинов — как с усиливающейся гидрофильно-стью соединительной ткани, так и с нарастающей плазморраги-ей. Коллагеновые фибриллы практически не страдают, если не считать некоторого их разволокнения; однако "упаковка" колла-геновых фибрилл в волокне становится более рыхлой.
В 1961 г. А.И.Струков назвал эти изменения мукоидным набуханием, поверхностной фазой дезорганизации соединительной ткани. По существу он дал новое толкование миксоматозного (хромотропного) отека соединительной ткани, описанного В.Т.Талалаевым при ревматизме (1923). Однако термин "мукоидное набухание" за рубежом не прижился; обычно говорят о талалаевском мукоидном или хромотропном отеке.
При мукоидном набухании часто развиваются клеточные реакции в виде лимфоцитарно-макрофагальных скоплений (полиморфно-ядерные лейкоциты редки), что свидетельствует об участии иммунных реакций при этой поверхностной и обратимой дезорганизации соединительной ткани.
Если учесть, что при ревматических заболеваниях (особенно ревматизме и ревматоидном артрите) иммунные реакции индуцированы стрептококком, с чем связано резкое повышение активности гиалуронидаз, то накопление гиалуроновых структур в соединительной ткани в этой ситуации можно рассматривать как проявление адаптации.
Несмотря на общие пато- и морфогенетические механизмы мукоидного набухания при ревматических заболеваниях, оно имеет определенное своеобразие в зависимости от особенностей этиологии и патогенеза каждого из заболеваний; следует учитывать также и структурно-функциональные особенности органов, что показано при ревматизме, системной красной волчанке, ревматоидном артрите.
Поверхностная дезорганизация соединительной ткани обычно прогрессирует, становится глубокой, захватывающей как ин-терстициальное (межуточное) вещество, так и коллагеновые структуры — развиваются фибриноидиые изменения, или фибриноидное набухание. Это уже необратимый процесс, завершающийся фибриноидным некрозом, ги-алинозом, склерозом.
E.Neumann, впервые описавший фибриноидное набухание (1896) считал, что в его основе лежат повреждение коллагеновых нолокон и приобретение ими свойств фибрина. Так появилось понятие о фибриноиде — веществе, которое возникает при фибриноидном набухании и отличается по многим свойствам от коллагена и фибрина.
В дальнейшем было показано, что в формировании фибрино-ида, помимо деструкции коллагеновых волокон, большую роль играет состояние основного вещества, прежде всего его гликоз-аминогликанов, которые способны осаждаться щелочными белками, высвобождающимися при повреждении волокнистых и клеточных структур соединительной ткани. Было установлено, что в построении фибриноида принимают участие и белки плазмы, в первую очередь фибриноген с последующим превращением его в фибрин.
Деление фибриноида на два вида — с фибрином и без фибрина, было опровергнуто результатами как биохимических, имму-ногистохимических, так и поляризационно-микроскопических и электронно-микроскопических исследований. Фибрин — обязательный компонент фибриноида, что лишний раз свидетельствует о важной роли плазморрагии в его развитии. Обнаружение же в фибриноиде иммунных комплексов подтверждает важную роль не только плазморрагии, но и нарушений иммунологического го-меостаза при фибриноидных изменениях. Становится понятной клеточная реакция при фибриноидных изменениях, преимущественно плазмоцитарная и лимфоцитарно-макрофагальная (в случаях фибриноидного некроза и нейтрофильная). В ответ на деструкцию возникает воспаление по сути своей иммунное [Стру-ков А.И., 1979].
При нарушениях иммунологического гомеостаза образование фибриноида обусловлено главным образом иммунокомплексным повреждением соединительной ткани с последующей абсорбцией фибрина — "фибриноид иммунных комплексов", "фибриноид деструкции". Однако при различных ревматических болезнях, патогенез которых связан с нарушением иммунологического гомеостаза, образуется разный фибриноид. Так, анализ фибриноидных изменений сердца при ревматизме показал, что расщепление коллагеновых фибрилл, как и изменения склеивающего вещества коллагеновых волокон, может быть причиной последующей инсудации плазменных белков, прежде всего фибриногена, при этом поврежденные коллагеновые волокна приобретают тинкториальные свойства фибрина. В очагах фибриноида обнаруживают фибрин, иммуноглобулины, комплемент. Подобную характеристику имеет и фибриноид при ревматоидном артрите. При системной красной волчанке — классической иммунокомп-псксной болезни — фибриноид имеет свою особенность. В фиб-
риноиде определяется ядерный материал, что связано со своеобразием иммунных комплексов — высокая комплементсвязываю-щая активность комплексов, их лизирующие, лейкотаксические и хемотаксические свойства, а главное, антинуклеарная направленность комплексов.
Системный гиалиноз как сосудов, особенно микроциркуляции, так и собственно соединительной ткани завершает процессы системной ее дезорганизации.
Сложный гиалин, среди микрофибрилл которого видны разрушенные элементы соединительной ткани, — это "гиалин деструкции", так как основой его является обычно "фибриноид". Поэтому сложный гиалин отличает высокое содержание фибрина, наличие в нем иммунных комплексов. Сложный галин и "старый" фибриноид имеют много общих черт. Это понятно, так как к их образованию причастны одни и те же иммунопатологические механизмы.
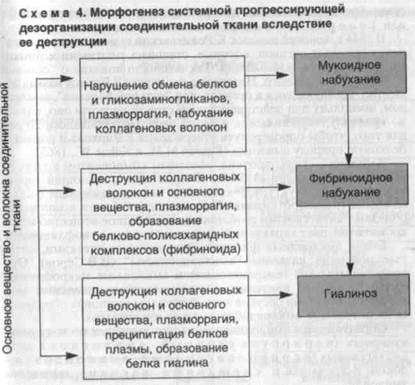
■ Итак, системная дезорганизация соединительной ткани как следствие ее прогрессирующей деструкции представлена следующими последовательно сменяющими друг друга процессами, составляющими сущность стромально-сосудистых (мезенхималь-ных) диспротеинозов:
▲ мукоидным набуханием (нарушение обмена белков и гликоза-миногликанов основного вещества, плазморрагия, набухание коллагеновых волокон);
▲ фибриноидным набуханием с образованием фибриноида (деструкция коллагеновых волокон и основного вещества, плазморрагия, образование белково-полисахаридных комплексов);
▲ гиалинозом (деструкция коллагеновых волокон и основного вещества, плазморрагия, преципитация белков плазмы, образование белка гиалина) (схема 4).
На основании приведенных материалов можно убедиться в том, что ревматические болезни отличаются от других системных заболеваний прежде всего двумя признаками — особенностью патогенеза и своеобразием морфогенеза. Особенность патогенеза заключается в ведущей роли при этих заболеваниях иммунопатологических механизмов. Морфогенетическое своеобразие заключается в системной дезорганизации соединительной ткани в результате прогрессирующей ее деструкции. При этом выявляется одна особенность — преимущественное поражение при том или ином ревматическом заболевании определенных, характерных только для этого заболевания, органов. При ревматизме такими органами-мишенями становятся сердце и сосуды, при ревматоидном артрите — суставы, при системной красной волчанке — микроциркуляторное русло и почки, при склеродермии (прогрессирующий системный склероз) — кожа и соединительная ткань ряда органов, при узелковом периартериите — артерии, при дерматомиозите — кожа и мышцы.
Эти шесть болезней, дополненные в последнее время болезнью Шегрена, образуют группу ревматических (бывших коллаге-новых) заболеваний. Эта группа, как видно, четко очерчена патогенезом и морфогенезом.
К сожалению, в последние годы морфогенез — основа патогенеза ревматических болезней — был перечеркнут, что привело к "разрастанию" и безликости группы ревматических болезней. Отрицание морфогенетических (морфологических) признаков заболеваний перечеркивает и признанный общей патологией постулат Н.Н.Аничкова : "Морфогенез — основа патогенеза". Отказ от этого принципа ведет к необоснованным заключениям, которые, как говорили великие энциклопедисты прошлого, хуже, чем заблуждение.
Дата добавления: 2016-11-02; просмотров: 1239;
