Нарушения сердечного ритма и проводимости (с указанием формы). 21 страница
Следует помнить, что при развитии междолевого плеврита физикальные изменения в легких могут быть очень скудными. Диагноз подтверждается только при рентгенологическом исследовании.
Аутоиммунный пневмонит при постинфарктном синдроме выявляется несколько реже, чем перикардит и плеврит. Субъективно пневмонит проявляется усугублением одышки, что нередко расценивается как признак левожелудочковой недостаточности. Однако назначение диуретиков или инотропных лекарственных средств не приносит облегчения.
При объективном исследовании в легких выявляется ограниченный участок, в котором на фоне несколько ослабленного дыхания на высоте вдоха выслушивается крепитация. Иногда могут появляться мелкопузырчатые влажные хрипы. Лишь изредка, если очаг иммунного воспаления достаточно велик, можно выявить небольшое притупление перкуторного звука. В остальных случаях над легкими определяется ясный легочный звук.
 Запомните
Одним из важнейших диагностических признаков постинфарктного синдрома является быстрый положительный эффект при назначении глюкокортикоидов: уменьшение болевого синдрома, снижение лихорадки, исчезновение крепитации, шума трения перикарда и плевры. Запомните
Одним из важнейших диагностических признаков постинфарктного синдрома является быстрый положительный эффект при назначении глюкокортикоидов: уменьшение болевого синдрома, снижение лихорадки, исчезновение крепитации, шума трения перикарда и плевры.
|
Лечение постинфарктного синдрома заключается в назначении нестероидных противовоспалительных средств, а в более тяжелых случаях — глюкокортикоидов.
1. Глюкокортикоиды оказывают наиболее выраженный и быстрый эффект в связи с аутоиммунным генезом данного осложнения. Преднизолон назначают внутрь в дозе 20–30 мг в сутки, постепенно снижая дозу, примерно на 2,5–5 мг в неделю. При необходимости (например, при рецидивирующем течении постинфарктного синдрома) лечение продолжают в течение нескольких недель.
2. Нестероидные противовоспалительные средства (НПВС) также достаточно эффективны при постинфарктном синдроме, особенно при нетяжелых клинических проявлениях синдрома Дресслера. Назначают ацетилсалициловую кислоту, индометацин, ибупрофен, диклофенак, мовалис в обычных терапевтических дозах.
При назначении глюкокортикоидов и НПВС в остром и подостром периодах ИМ следует учитывать, что эти препараты могут нарушать процессы рубцевания инфаркта, повышая риск разрывов сердца. Кроме того, необходимо помнить, что при синдроме Дресслера антикоагулянты должны быть отменены. По понятным причинам антибиотики не эффективны при постинфарктном синдроме.
 Запомните
1. Наиболее характерными клиническими проявлениями постинфарктного синдрома Дресслера является триада: перикардит, плеврит, пневмонит. Эти патологические состояния развиваются обычно на 2–6-й неделе от начала ИМ. 2. Лечение постинфарктного синдрома заключается в назначении НПВС, а в более тяжелых случаях — глюкокортикоидов. 3. Антибиотики не эффективны при постинфарктном синдроме. 4. При подтверждении диагноза синдрома Дресслера антикоагулянты должны быть отменены. Запомните
1. Наиболее характерными клиническими проявлениями постинфарктного синдрома Дресслера является триада: перикардит, плеврит, пневмонит. Эти патологические состояния развиваются обычно на 2–6-й неделе от начала ИМ. 2. Лечение постинфарктного синдрома заключается в назначении НПВС, а в более тяжелых случаях — глюкокортикоидов. 3. Антибиотики не эффективны при постинфарктном синдроме. 4. При подтверждении диагноза синдрома Дресслера антикоагулянты должны быть отменены.
| ||
| 6.6. Инфаркт миокарда правого желудочка | ||

| ||
До недавнего времени считалось, что ИМ правого желудочка встречается очень редко. Однако в последние годы доказано, что примерно у 1/4 больных с заднедиафрагмальным (нижним) трансмуральным ИМ ЛЖ некроз распространяется и на область ПЖ, чаще его задней стенки. Поражение ПЖ в этих случаях определяет некоторые важные особенности нарушения гемодинамики, которые обязательно должны учитываться при лечении больных ИМ.
Особенности клинической картины.Начальные клинические проявления ИМ ПЖ (в частности, болевой синдром), динамика гиперферментемии и признаков резорбционно-некротического синдрома в целом соответствуют таковым, характерным для инфаркта задней стенки ЛЖ.
Некроз миокарда ПЖ быстро приводит к снижению его сократимости и появлению отдельных признаков или развернутой клинической картины острой правожелудочковой недостаточности, как правило, сопровождающейся также артериальной гипотонией.
При физикальном исследовании можно обнаружить следующие клинические симптомы:
1. Набухание шейных вен, обусловленное застойными явлениями в венозном русле большого круга кровообращения. Нередко набухание вен увеличивается на вдохе (симптом Куссмауля) в результате инспираторного увеличения притока крови в центральные вены и правые отделы сердца, обусловленного присасывающим действием отрицательного давления грудной клетки во время вдоха. У здорового человека такое инспираторное увеличение притока крови к правому сердцу (увеличение преднагрузки на ПЖ) сопровождается адекватным увеличением УО ПЖ (механизм Старлинга), и весь объем крови поступает в систему легочной артерии. Поэтому в норме во время вдоха шейные вены не набухают, а спадаются. При резком снижении систолической функции ПЖ его инспираторная объемная перегрузка сопровождается не увеличением, а заметным уменьшением УО ПЖ, связанным с неспособностью ПЖ “протолкнуть” этот дополнительный объем в легочную артерию. В результате происходит инспираторное набухание шейных вен.
2. Гепатомегалия, быстрое развитие которой при острой правожелудочковой недостаточности сопровождается болями в правом подреберье и болезненностью при пальпации печени.
3. Перкуторные признаки расширения полости ПЖ (смещение правой границы сердца вправо и расширение абсолютной тупости сердца), что подтверждается при рентгенографии и эхокардиографическом исследовании.
4. Правожелудочковый протодиастолический ритм галопа (патологический III тон сердца) выслушивается в нижней трети грудины или у ее левого края. Здесь же иногда можно выслушать систолический шум относительной недостаточности трехстворчатого клапана.
5. Отсутствие клинических признаков острой левожелудочковой недостаточности и застоя крови в малом круге кровообращения (одышки, удушья, влажных хрипов в легких и др.), что связано с уменьшением количества крови, выбрасываемой ПЖ в легочную артерию, и, соответственно, со снижением ДЗЛА и давления наполнения ЛЖ.
6. Артериальная гипотония связана не с угнетением насосной функции ЛЖ, а со снижением систолической функции ПЖ и уменьшением количества крови, поступающей в левые отделы сердца из малого круга кровообращения (уменьшение преднагрузки ЛЖ). Другой причиной артериальной гипотензии могут служить различные брадиаритмии (СССУ, АВ-блокады и др.), характерные для ишемического поражения ПЖ, что связано с окклюзией ПКА, участвующей в кровоснабжении СА-узла и АВ-соединения.
7. Парадоксальный артериальный пульс — снижение во время вдоха систолического АД больше 10–12 мм рт. ст. и инспираторное уменьшение наполнения пульсовой волны. Этот признак, по сути, обусловлен теми же причинами, что и увеличение набухания вен шеи на вдохе (симптом Куссмауля): снижением УО ПЖ и, соответственно, наполнения левых отделов сердца. Имеет значение также инспираторное парадоксальное движение МЖП в сторону ЛЖ (подробнее см. главу 12).
8. Клинические признаки нарушений сердечного ритма и проводимости, наиболее частыми из которых являются фибрилляция предсердий и АВ-блокады.
Эти и некоторые другие, остро развивающиеся клинические признаки обычно позволяют заподозрить наличие у больного ИМ ПЖ. Классической триадой, характерной для инфаркта миокарда правого желудочка, считают:
- артериальную гипотензию;
- увеличение давления в яремных венах и правом предсердии;
- отсутствие хрипов при аускультации легких.
Диагноз инфаркта ПЖ подтверждается с помощью следующих инструментальных методов исследования.
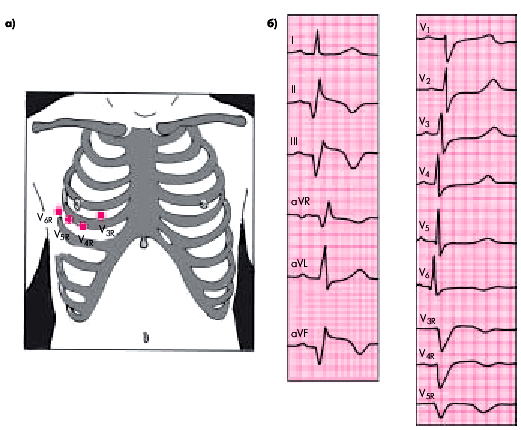
Электрокардиография. ИМ правого желудочка, как правило, сочетается с заднедиафрагмальным (нижним) ИМ левого желудочка. При этом чаще поражается задняя стенка ПЖ, реже — его боковая или передняя стенки. При обычной регистрации ЭКГ в 12 отведениях ИМ задней стенки ПЖ лишь иногда проявляется подъемом сегмента RS–Т в правых грудных отведениях (V1–V2), что не является специфическим признаком ИМ ПЖ. Большей информативностью обладают дополнительные отведения с правой половины грудной клетки V3R — V4R (рис. 6.65). При ИМ ПЖ в этих отведениях появляется патологический зубец Q или комплекс QS и подъем сегмента RS–Т (в острейшей и острой стадиях заболевания). Иногда изменения ограничиваются только подъемом сегмента RS–Т и формированием отрицательного зубца Т.
|
| Рис. 6.65. Локализация электродов дополнительных отведений V3r-V6r (а) и изменения ЭКГ при заднедиафрагмальном (нижнем) ИМ с переходом на залнюю стенку правого желудочка (б) |
Таким образом, для ИМ задней стенки ПЖ (наиболее частая локализация инфаркта ПЖ) характерны наличие патологического зубца Q и/или подъем сегмента RS–Т в дополнительных отведениях с правой половины грудной клетки V3R и V4R при отсутствии этих изменений в отведениях V1 и V2. Нередко на ЭКГ выявляются также фибрилляция предсердий и АВ-блокады.
Эхокардиография. Эхокардиограмма, зарегистрированная в двухмерном и допплеровском режимах, позволяет выявить ряд признаков поражения ПЖ и снижение его систолической функции.
- Расширение полости ПЖ.
- Признаки гипокинезии или акинезии задней, боковой или передней стенки ПЖ.
- Парадоксальное движение МЖП в сторону ЛЖ, что объясняется выраженной объемной перегрузкой ПЖ и его неспособностью “протолкнуть” кровь в систему малого круга кровообращения.
- Расширение нижней полой вены с ее недостаточным спадением (коллабированием) на высоте глубокого вдоха, что указывает на повышение ЦВД (давления в полости ПП).
- Исследование транстрикуспидального диастолического потока крови в допплеровском режиме иногда позволяет выявить признаки трикуспидальной регургитации крови из ПЖ в ПП, обусловленной дисфункцией клапанного аппарата, возникающей в результате дилатации и снижения сократимости ПЖ.
Катетеризацию правых отделов сердца и легочной артерии катетером Свана–Ганца у больных ИМ ПЖ проводят для подтверждения диагноза и разработки адекватной тактики лечения больных. Наиболее типичными изменениями гемодинамики, выявляемыми у больных ИМ ПЖ с помощью катетеризации правых отделов сердца и легочной артерии, являются:
- увеличение среднего давления в ПП (выше 10 мм рт. ст.), которое иногда достигает уровня диастолического давления в легочной артерии или ДЗЛА. Это объясняет наличие застоя крови в венах большого круга кровообращения и отсутствие застоя крови в легких;
- систолическое давление в легочной артерии нормально или даже несколько снижено, что частично объясняет сравнительно низкие значения давления наполнения ЛЖ и системного АД.
Коронароангиография, как правило, позволяет выявить окклюзию или критическое сужение ПКА, кровоснабжающей заднюю стенку как левого, так и правого желудочков. Реже встречается поражение ОВ ЛКА (обычно при левом типе кровоснабжения сердца).
 Запомните
Классической триадой, характерной для инфаркта миокарда ПЖ (помимо болевого синдрома), считают: Запомните
Классической триадой, характерной для инфаркта миокарда ПЖ (помимо болевого синдрома), считают:
|
Лечение
Ниже приведены основные принципы лечения больных ИМ ПЖ.
1. При наличии артериальной гипотонии, вызванной недостаточностью насосной функции ПЖ и уменьшением ОЦК, необходимо внутривенное капельное введение растворов, способствующих увеличению циркулирующего объема крови: 0,9% раствора натрия хлорида (1–1,5 л со скоростью 200 мл/ч), декстрана, коллоидных растворов, реополиглюкина. Введение жидкости проводится под постоянным контролем гемодинамических показателей до тех пор, пока ЦВД (давление в ПП) не достигнет уровня 14–15 мм рт. ст. (D. Alpert, G. Frensis) или несколько выше.
2. Если после введения жидкостей сохраняется артериальная гипотония, целесообразно прибегнуть к введению инотропных лекарственных средств (добутамина или/и допaмина) (см. выше).
3. При отсутствии эффекта показана коронарная баллонная ангиопластика (см. выше).
4. Тромболитическая терапия (см. выше) достаточно успешно устраняет основные клинические проявления ИМ ПЖ.
5. При возникновении фибрилляции предсердий необходимо купирование ее по схемам, описанным выше.
6. При появлении синусовой брадикардии и других проявлений СССУ и АВ-блокады II степени II типа Мобитца показана временная ЭКС.
 Запомните
В большинстве случаев при ИМ ПЖ, особенно при развитии артериальной гипотонии, необходимо обеспечить восстановление ОЦК и создание достаточно высокого давления наполнения ПЖ (или давления в ПП), достигающего 14–15 мм рт. ст. и выше. 2. Следует по возможности избегать введения лекарственных средств, уменьшающих преднагрузку на ПЖ: нитратов, диуретиков, ингибиторов АПФ, морфина. 3. Введение раствора нитроглицерина возможно только при нормализации системного АД и одновременно с инфузионной терапией, контролируемой по ЦВД и ДЗЛА (или диастолическому давлению в легочной артерии). Запомните
В большинстве случаев при ИМ ПЖ, особенно при развитии артериальной гипотонии, необходимо обеспечить восстановление ОЦК и создание достаточно высокого давления наполнения ПЖ (или давления в ПП), достигающего 14–15 мм рт. ст. и выше. 2. Следует по возможности избегать введения лекарственных средств, уменьшающих преднагрузку на ПЖ: нитратов, диуретиков, ингибиторов АПФ, морфина. 3. Введение раствора нитроглицерина возможно только при нормализации системного АД и одновременно с инфузионной терапией, контролируемой по ЦВД и ДЗЛА (или диастолическому давлению в легочной артерии).
| ||
| 6.7. Внезапная сердечная смерть | ||

| ||
Внезапная сердечная смерть (ВСС) — это наиболее тяжелый, молниеносно протекающий клинический вариант ИБС. К внезапной сердечной смерти относят только те случаи внезапного прекращения сердечной деятельности, которые характеризуются следующими признаками:
1. Смерть наступила в присутствии свидетелей в пределах 1 ч после возникновения первых угрожающих симптомов (в недавнем прошлом этот период ограничивали 6 часами).
2. Перед наступлением смерти состояние больных оценивалось окружающими как стабильное и не вызывающее серьезных опасений.
3. Смерть произошла при обстоятельствах, исключающих другие ее причины (насильственная смерть, травмы, другие смертельные заболевания).
В подавляющем большинстве случаев (около 85–90%) причиной внезапной сердечной смерти является ИБС, причем любые ее клинические варианты, включая бессимптомное течение, когда внезапная смерть является первым и последним клиническим проявлением болезни. В целом примерно  больных верифицированной ИБС умирает внезапно. Наибольшему риску внезапной сердечной смерти подвержены:
больных верифицированной ИБС умирает внезапно. Наибольшему риску внезапной сердечной смерти подвержены:
- больные острым ИМ (особенно в первый час развития инфаркта);
- больные НС;
- пациенты, перенесшие в прошлом ИМ, особенно лица с кардиомегалией и застойной сердечной недостаточностью;
- больные ИБС с желудочковыми аритмиями высоких градаций;
- больные ИБС, имеющие несколько основных факторов риска (АГ, ГЛП, курение, нарушения углеводного и жирового обменов и др.).
Следует заметить, что внезапная смерть, наступившая в ранней (острейшей) фазе ИМ, верифицированного клинически или на аутопсии, расценивается как “смерть от инфаркта”. Тем не менее по своим механизмам, клинической картине и комплексу необходимых реанимационных мероприятий она полностью соответствует внезапной сердечной смерти, развивающейся при других формах ИБС, и поэтому рассматривается в данном разделе.
К другим причинам внезапной сердечной смерти (помимо ИБС) относятся:
- любые заболевания сердца, сопровождающиеся выраженной гипертрофией миокарда (например, ГКМП, стеноз устья аорты и т.п.);
- застойная сердечная недостаточность любого генеза;
- кардиогенный шок любого генеза (помимо острого ИМ);
- тампонада сердца любого генеза (например, при экссудативном перикардите и т.п.);
- тромбоэмболия легочной артерии;
- синдром удлиненного интервала Q–Т
Особенности патогенеза
У большинства больных ИБС (85–90%), умерших внезапно, в том числе у пациентов с бессимптомным течением заболевания, на аутопсии обнаруживают значительные атеросклеротические изменения КА: сужение их просвета более чем на 75% и многососудистое поражение коронарного русла. Только у 10–15% внезапно умерших эти изменения отсутствуют. Атеросклеротические бляшки, расположенные преимущественно в проксимальных участках КА, как правило, бывают осложненными, с признаками повреждения эндотелия и образованием пристеночных или (сравнительно редко) полностью окклюзирующих просвет сосуда тромбов.
Эти изменения вместе с возможной в этих условиях динамической окклюзией (выраженным спазмом) венечных сосудов и увеличением потребности миокарда в кислороде являются причиной развития острого очагового ишемического повреждения сердечной мышцы, лежащего в основе внезапной сердечной смерти.
Правда, на аутопсии только у 10–15% больных ИБС, умерших внезапно, выявляются макроскопические и/или гистологические признаки острого ИМ. Это объясняется тем, что для формирования таких признаков требуется не менее 18–24 ч (В.В. Серов с соавт, 1997). Тем не менее результаты электронной микроскопии показывают, что уже через 20–30 мин после прекращения коронарного кровотока начинается процесс необратимых изменений клеточных структур миокарда, который завершается уже через 2–3 ч коронарной окклюзии. Возникают выраженные необратимые нарушения метаболизма миокарда, ведущие к электрической нестабильности сердечной мышцы и фатальным нарушениям ритма.
Основными непосредственными причинами внезапной сердечной смерти являются: 1) фибрилляция желудочков и 2) асистолия сердца, электрофизиологические механизмы которых подробно разбираются в главе 3.
Фибрилляция желудочков — это частое (до 200–500 в мин), но беспорядочное, нерегулярное возбуждение и сокращение отдельных мышечных волокон. В результате такой хаотической активации отдельных групп кардиомиоцитов одномоментное синхронное их сокращение становится невозможным. Наступает асистолия желудочков, и кровоток прекращается.
Асистолия сердца — это полное прекращение деятельности сердца, его остановка. Первичная асистолия обусловлена нарушением функции автоматизма СА-узла, а также водителей ритма II и III порядка (АВ-соединения и волокон Пуркинье). В этих случаях асистолии предшествует так называемая электромеханическая диссоциация сердца, при которой еще сохраняются признаки минимальной электрической активности сердца в виде быстро истощающегося синусового, узлового или редкого идиовентрикулярного ритма, но критически снижается сердечный выброс. Электромеханическая диссоциация достаточно быстро переходит в асистолию сердца.
Понятно, что асистолии сердца часто предшествует также фибрилляция и трепетание желудочков.
Клиническая картина
Около 1/4 случаев внезапной сердечной смерти наступает молниеносно и без видимых предвестников. Однако, как показывает опрос родственников умерших, у остальных больных за 1–2 недели до внезапной смерти отмечаются разнообразные, не всегда специфичные, продромальные симптомы, свидетельствующие об обострении заболевания: учащение болей в сердце (иногда атипичной локализации), одышка, общая слабость и значительное снижение работоспособности и переносимости физической нагрузки, сердцебиения и перебои в работе сердца и т.п.
Внезапная сердечная смерть может быть спровоцирована чрезмерным физическим или нервно-психическим напряжением, но может возникнуть в покое, например, во сне. Непосредственно перед наступлением внезапной сердечной смерти примерно у половины больных отмечается болевой ангинозный приступ, нередко сопровождающийся страхом близкой смерти.
Бульшая часть случаев внезапной сердечной смерти (около 90%) происходит во внебольничных условиях — дома, на работе, в транспорте, что и определяет наиболее частый фатальный исход этой формы ИБС. Если же больной находится в стационаре, в частности в блоке интенсивной терапии, диагноз внезапной сердечной смерти должен быть поставлен в считанные секунды и незамедлительно начаты реанимационные мероприятия.
Сразу во время внезапно развивающейся фибрилляции желудочков или асистолии сердца у больного появляются резкая слабость, головокружение. Через несколько секунд в результате полного прекращения мозгового кровотока больной теряет сознание, появляется тоническое сокращение скелетных мышц, шумное дыхание.
При осмотре кожные покровы бледные с сероватым оттенком, холодные на ощупь. Начинают быстро расширяться зрачки. Пульс на сонных артериях не определяется, тоны сердца не выслушиваются. Примерно через 1,5 мин зрачки максимально расширены. Отмечается отсутствие зрачковых и роговичных рефлексов. Дыхание быстро урежается, становится агональным, появляются очень редкие отдельные “судорожные дыхательные движения”. Через 2,5–3 мин дыхание прекращается совсем. Следует помнить, что примерно через 3 мин от момента наступления фибрилляции желудочков или асистолии в клетках коры головного мозга происходят необратимые изменения.
 Запомните
Диагноз клинической смерти ставится на основании следующих клинических признаков: 1. Отсутствие сознания. 2. Отсутствие дыхания (или очень редкое дыхание агонального типа). 3. Отсутствие пульса на сонных артериях. 4. Отсутствие тонов сердца при аускультации. 5. Максимальное расширение зрачков и отсутствие роговичного и зрачкового рефлексов. 6. Холодные кожные покровы бледно-серого цвета. Запомните
Диагноз клинической смерти ставится на основании следующих клинических признаков: 1. Отсутствие сознания. 2. Отсутствие дыхания (или очень редкое дыхание агонального типа). 3. Отсутствие пульса на сонных артериях. 4. Отсутствие тонов сердца при аускультации. 5. Максимальное расширение зрачков и отсутствие роговичного и зрачкового рефлексов. 6. Холодные кожные покровы бледно-серого цвета.
|
Если больной находится на ЭКГ-мониторном наблюдении,в момент наступления внезапной сердечной смерти можно обнаружить следующие изменения:
1. Фибрилляция желудочков — частые (до 200–500 в мин) и нерегулярные беспорядочные волны, отличающиеся друг от друга различной формой и амплитудой. Постепенно волны фибрилляции становятся низкоамплитудными и переходят в прямую изолинию (асистолия).
2. Трепетание желудочков (иногда предшествует фибрилляции желудочков) — частые относительно регулярные и почти одинаковые по форме и амплитуде волны трепетания, напоминающие синусоидальную кривую. Выделить на этой кривой комплексы QRS, сегмент RS–Т и зубец Т не представляется возможным. Вскоре амплитуда волн уменьшается, они становятся нерегулярными и разной амплитуды — трепетание переходит в фибрилляцию желудочков.
3. Асистолия сердца — полное отсутствие электрической активности сердца. На ЭКГ при этом определяется изолиния.
4. Электромеханическая диссоциация — на ЭКГ регистрируется редкий синусовый или узловой ритм, переходящий в oчень редкий идиовентрикулярный ритм, а затем в асистолию.
Лечение
При возникновении внезапной сердечной смерти немедленно осуществляют сердечно-легочную реанимацию, которая включает восстановление проходимости дыхательных путей, искусственную вентиляцию легких, непрямой массаж сердца, электрическую дефибрилляцию и медикаментозную терапию.
Методы сердечно-легочной реанимации подробно изложены в последующих главах руководства.
Профилактика
В многочисленных специальных исследованиях, посвященных внезапной сердечной смерти, было показано, что к числу наиболее значимых предикторов внезапной смерти у больных ИБС относятся:
1. Возникновение желудочковых аритмий высоких градаций у больных с низкой толерантностью к физической нагрузке и положительной велоэргометрической пробой.
2. Выраженная депрессия сегмента RS–Т (более 2,0 мм), патологическое повышение АД и раннее достижение максимальной ЧСС во время нагрузочного теста.
3. Наличие на ЭКГ патологических зубцов Q или комплекса QS в сочетании с блокадой левой ножки пучка Гиса и желудочковой экстрасистолией.
4. Наличие у больного основных факторов риска (АГ, ГЛП, курение и сахарный диабет) в сочетании со снижением толерантности к физической нагрузке и положительной велоэргометрической пробой.
| Глава 7. Эссенциальная артериальная гипертензия (гипертоническая болезнь) |

|
Артериальная гипертензия (АГ) — это стойкое повышение АД (систолического АД і 140 мм рт. ст. и/или диастолического АД і 90 мм рт. ст.), зарегистрированное не менее чем при 2-х врачебных осмотрах, при каждом из которых АД измеряется по крайней мере дважды. Понятно, что это определение справедливо только при условии, что пациент не принимал в это время лекарственные средства, влияющие на уровень АД.
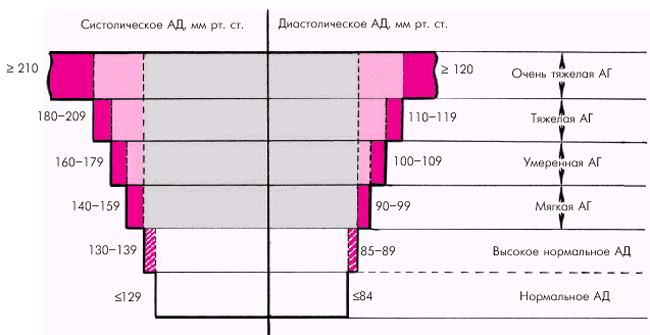
В норме систолическое АД на плечевой артерии не превышает 139 мм рт. ст., а диастолическое — 89 мм рт. ст. Согласно рекомендациям Национального комитета США по артериальным гипертензиям (1993 г.), к нормальному уровню АД на плечевой артерии следует относить цифры систолического АД, не превышающие 129 мм рт. ст. и диастолического АД — 84 мм рт. ст. (рис. 7.1). Уровень систолического АД от 130 до 139 мм рт. ст. и диастолического АД от 85 до 89 мм рт. ст. оценивается как “высокое нормальное АД”. Таким образом, превышение этих нормативов является основанием для диагностики АГ.
|
| Рис. 7.1. Классификация артериальных гипертензий в зависимости от уровня АД. Объяснение в тексте |
В клинической практике чаще встречается систоло-диастолическая АГ, при которой отмечается повышение как систолического АД (САД і 140 мм рт. ст.), так и диастолического АД (ДАД і 90 мм рт. ст.). Если имеет место преимущественное повышение систолического АД (і 140 мм рт. ст.), а диастолическое АД не превышает 90 мм рт. ст., говорят о так называемой изолированной систолической АГ, больше свойственной больным пожилого и старческого возраста.
Многочисленные эпидемиологические исследования доказали значительную распространенность АГ среди взрослого населения. В экономически развитых странах число больных с повышенными цифрами АД достигает в настоящее время 20–30%. Имеется прямая зависимость заболеваемости АГ от возраста. Например, у лиц старше 65 лет АГ встречается в 50% случаев. Мужчины молодого и среднего возраста заболевают АГ чаще, чем женщины, хотя в возрасте старше 50 лет частота возникновения АГ у женщин несколько выше, чем у мужчин.
АГ является одним из главных факторов риска развития ИБС, мозгового инсульта и сердечной недостаточности. Среди лиц, страдающих АГ, ИБС встречается в 4,5 раза, ИМ — в 2,6 раза, НС — в 2,3 раза, а нарушения мозгового кровообращения — в 9,8 раза чаще, чем у нормотоников (Е.Е. Гогин, 1997).
В зависимости от этиологии все случаи АГ делят на две группы:
1. Первичная (эссенциальная или идиопатическая) АГ (гипертоническая болезнь — ГБ).
2. Вторичные (симптоматические) АГ.
Симптоматические (вторичные) АГ не являются самостоятельными заболеваниями. Их рассматривают лишь как одно из проявлений другой патологии, например, заболеваний почек (пиелонефрита, гломерулонефрита, стеноза почечных артерий и др.), эндокринной системы (гипертиреоза и др.), заболеваний ЦНС (посттравматической энцефалопатии и др.), сосудистой патологии (коарктации аорты, атеросклероза аорты и т.п.). Таким образом, в случае симптоматических АГ причина повышения АД всегда известна.
К эссенциальной (первичной) АГ относят те случаи заболевания, когда невозможно установить связь между повышением АД и той или иной органной или эндокринной патологией, предшествующей возникновению АГ.
Дата добавления: 2016-04-22; просмотров: 581;
