Электронные конфигурации атомов
Электроны в атоме занимают уровни, подуровни и орбитали согласно следующим правилам.
Правило Паули. В одном атоме два электрона не могут иметь четыре одинаковых квантовых числа. Они должны отличаться, по меньшей мере, одним квантовым числом.
Орбиталь содержит электроны с определенными числами n, l, ml и электроны на ней могут отличаться только квантовым числом ms, имеющим два значения +1/2 и -1/2. Поэтому на орбитали могут располагаться не более двух электронов.
На подуровне электроны имеют определенные n и l и различаются числами ml и ms. Поскольку ml может принимать 2l+1 значение, а ms - 2 значения, то на подуровне может содержаться не более 2(2l+1) электронов. Отсюда максимальные числа электронов на s-, p-, d-, f-подуровнях равны соответственно 2, 6, 10, 14 электронов.
Аналогично на уровне содержится не более 2n2 электронов и максимальное число электронов на четырех первых уровнях не должно превышать 2, 8, 18 и 32 электронов соответственно.
Правило наименьшей энергии. Последовательное заполнение уровней должно происходить так, чтобы обеспечить минимальную энергию атома. Каждый электрон занимает свободную орбиталь с наименьшей энергией.
Правило Клечковского. Заполнение электронных подуровней осуществляется в порядке возрастания суммы (n+l), а в случае одинаковой суммы (n+l) - в порядке возрастания числа n.
Графическая форма правила Клечковского.
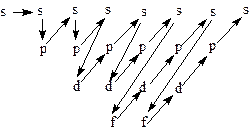
 Cогласно правилу Клечковского заполнение подуровней осуществляется в следующем порядке: 1s, 2s, 2p, 3s, 3p, 4s, 3d, 4p, 5s, 4d, 5p, 6s, 4f, 5d, 6p, 7s, 5f, 6d, 7p, 8s,...
Cогласно правилу Клечковского заполнение подуровней осуществляется в следующем порядке: 1s, 2s, 2p, 3s, 3p, 4s, 3d, 4p, 5s, 4d, 5p, 6s, 4f, 5d, 6p, 7s, 5f, 6d, 7p, 8s,...
Хотя заполнение подуровней происходит по правилу Клечковского, в электронной формуле подуровни записываются последовательно по уровням: 1s, 2s, 2p, 3s, 3p, 3d, 4s, 4p, 4d, 4f и т.д. Это связано с тем, что энергия заполненных уровней определяется квантовым числом n: чем больше n, тем больше энергия и для полностью заполненных уровней мы имеем Е3d<E4s, а не наоборот, как это следует из правила Клечковского. Таким образом, электронная формула атома брома записывается следующим образом: Br(35e) 1s22s22p63s23p63d104s24p5. Подобная формула правильно передает свойства атома брома - участие валентных 4s и 4p электронов и неучастие внутренних 3d электронов в образовании химических связей.
Уменьшение энергии подуровней с меньшими n и большими l в случае, если они заполнены полностью или наполовину, приводит для ряда атомов к электронным конфигурациям, отличающимся от предсказанных по правилу Клечковского. Так для Cr и Cu мы имеем на валентном уровне распределение:
Cr(24e) 1s22s22p63s23p63d54s1 и Cu(29e) 1s22s22p63s23p63d104s1, а не
Cr(24e) 1s22s22p63s23p63d44s2 и Cu(29e) 1s22s22p63s23p63d94s2.
Правило Гунда. Заполнение орбиталей данного подуровня осуществляется так, чтобы суммарный спин был максимален. Орбитали данного подуровня заполняются сначала по одному электрону. Например, для конфигурации р2 заполнение px1py1 с суммарным спином s = 1/2 + 1/2 = 1 предпочтительнее (т.е. ему соответствует меньшая энергия), чем заполнение px2 с суммарным спином s = 1/2 - 1/2 = 0.





 - более выгодно, ¯ - менее выгодно.
- более выгодно, ¯ - менее выгодно.
Электронные конфигурации атомов можно записать по уровням, подуровням, орбиталям. В последнем случае орбиталь обычно обозначают квантовой ячейкой, а электроны - стрелками, имеющими то или иное направление в зависимости от величины ms.
Например, электронная формула Р(15е) может быть записана:
а) по уровням )2 )8 )5
б) по подуровням 1s22s22p63s23p3
в) по орбиталям 1s22s22px22py22pz23s23px13py13pz1 или








 ¯ ¯ ¯ ¯ ¯ ¯
¯ ¯ ¯ ¯ ¯ ¯
Пример. Записать электронные формулы Ti(22e) и As(33e) по подуровням. Титан находится в 4 периоде, поэтому записываем подуровни до 4р: 1s2s2p3s3p3d4s4p и заполняем их электронами до их общего числа 22, при этом незаполненные подуровни в окончательную формулу не включаем. Получаем:
Ti(22e) 1s22s22p63s23p63d24s2.
Аналогично, для мышьяка имеем электронную формулу:
As(33e) 1s22s22p63s23p63d104s24p3.
Формулы ионов Ti2+ и As3- записываются следующим образом:
Ti2+(20e) 1s22s22p63s23p63d24s0
As3-(36e) 1s22s22p63s23p63d104s24p6
Дата добавления: 2016-04-11; просмотров: 1050;
