Роль контактных состояний.
Роль электронно-конформационных взаимодействий в разделении зарядов в реакционном центре; механизмы окисления цитохрома в реакционном центре.
Роль электронно-конформационных взаимодействий в разделении зарядов в реакционном центре
Электронные переходы должны быть сопряжены с внутримолекулярной подвижностью белка РЦ, которая обеспечивает, во-первых, процессы электронно-колебательной релаксации по акцептирующей моде и фиксации электрона в акте туннельного переноса, и во-вторых, индуцированные вследствие изменения зарядового состояния акцептора последующие конформационные перестройки в макромолекулярном комплексе:
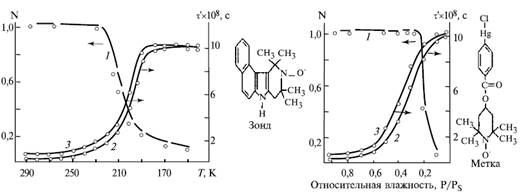
а) б)
(1) Функциональная активность и конформационная динамика (2,3) РЦ в зависимости от температуры А) и влажности Б).
Роль контактных состояний.
Для реализации контактного состояния необходима определенная конформационная свобода или набор внутримолекулярных степеней свободы молекулы цитохрома. Речь идет о структурном туннелировании между донорно-акцепторными группами, где белковая цепь, видимо, выступает как медиатор электронного переноса.
(Для бактериохлорофилла, в учебнике только такой пример)
В последнее время существование специфической электронной тропы с участием аминокислотных остатков было показано для цитохрома Сн между донорной группой гема и поверхностью глобулы. В белке РЦ такая менее специфическая тропа идет от поверхности глобулы к фотоактивному димеру Р. В контактной позиции существует перекрытие волновых функций групп И и А (электронных облаков так понимаю), и поэтому расстояние между ними составляет около 0,1 нм. В неконтактной позиции расстояние между группами И и А увеличивается до 0,3-0,5. Поскольку на расстояниях 0,3 - 0,5 нм перекрытие волновых функций практически равно нулю, между группами возникает барьер, а это сразу же снижает скорость туннелирования в неконтактной позиции в 10^6 раз, т. е. делает практически невозможным перенос электрона.
По расчетам, в условиях обезвоживания расстояние между Сн и Р должно было бы возрасти до 20 A, что явно нереально. Очевидно, при изменении состояния воды изменяется структура всего комплекса вследствие модификации взаимного расположения донорно-акцепторных пар в белковой матрице. Это обстоятельство влияет на образование контактного состояния между ними, в пределах которого возможен межбелковый перенос электрона от цитохрома к бактериохлорофиллу. Роль воды в этом процессе перестройки мембран велика, поскольку нативная конформация комплекса цитохрома с РЦ зависит от гидрофобных взаимодействий. Характер и направленность структурных перестроек в мембранах определяется соотношением фактов упорядоченности водного окружения (энтропийный фактор) и образованием водородных связей между молекулами воды и гидрофобных связей между молекулярными группами (энтальпийный фактор).
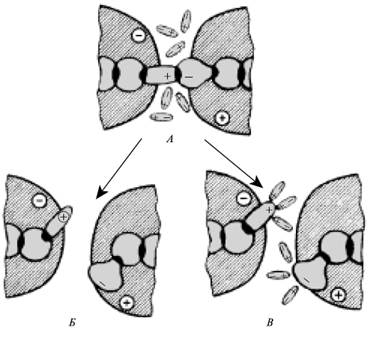
Поведение молекулярных групп в области контакта между макромолекулами высокопотенциального цитохрома (донор) и реакционного центра (акцептор) в фотосинтетических мембранах пурпурных бактерий при понижении степени гидратации и температуры.
А - контактная позиция;
Б, В - неконтактные позиции
Т е баланс сил, обусловливающий стабилизацию контактного состояния, определяется полярным взаимодействием контактирующих групп и гидрофобными силами, которые зависят от наличия молекул воды в системе. В присутствии воды при низких температурах неконтактная позиция (В) сохраняется вследствие слабой подвижности структурных групп и молекул воды в области контакта. Однако при повышении температуры подвижность отдельных молекулярных групп и, главное, молекул воды растет. Следовательно, возрастает и энтропия системы. Именно это обстоятельство делает энергетически более выгодной и устойчивой при комнатной температуре позицию А, несмотря на то, что энтальпия в этом состоянии увеличивается. В пределах позиции А происходит формирование собственно контактного состояния между подвижными группами 1 и 2. Снижение энтропии, сопровождающее образование комплекса, не может существенно уменьшить общую величину энтропии конформационно «расторможенной» позиции А. Таким образом, роль воды здесь заключается в одновременном обеспечении конформационной подвижности и «энтропийной» устойчивости контактного состояния. Аналогичную роль может играть вода и в акте первичного разделения зарядов. Как оказалось, удаление воды ингибирует процесс разделения зарядов в РЦ пурпурных фотосинтезирующих бактерий, нарушая образование контактных состояний, либо препятствует стабилизации электрона на бактериофеофитине за счет изменения характера водородных связей. Надеюсь, все это не очень путано.
Дата добавления: 2016-04-11; просмотров: 451;
