Молекулярная организация биологических мембран. Состав, строение, образование. Белок-липидные взаимодействия.
Молекулярная организация биологических мембран. Состав, строение, образование. Термодинамика процессов формирования и устойчивости мембран. Белок-липидные взаимодействия. Фазовый переход
Получилось очень много. Читать по диагонали. Зато можно составить более менее полное впечатление.
Молекулярная организация биологических мембран. Состав, строение, образование. Белок-липидные взаимодействия.
Биологическая мембрана ограничивает цитоплазму и большинство внутриклеточных структур, а также образует единую внутриклеточную систему канальцев, складок и замкнутых полостей. Толщина мембран редко больше 10,0 нм, однако из-за плотной упаковки белков и липидов, а также большой общей площади составляют обычно больше половины массы сухих клеток.
Построены в основном из белков, липидов и углеводов. Доля углеводов 10-15 %, они связаны либо с молекулами белка (гликопротеины), либо с молекулами липидов (гликолипиды). В мембранах различного происхождения содержание липидов колеблется от 25 до 75 % по массе по отношению к белку.
Липиды мембран относятся к трем основным классам:
глицерофосфатиды (фосфолипиды), сфинго- и гликолипиды, стероиды.
Мембранные липиды имеют сравнительно небольшую полярную (заряженную) головку и длинные незаряженные (неполярные) углеводородные цепи. Цвиттерионные липиды - фосфатидилхолин, фосфатидилэтаноламин и сфингомиелин. Их головки несут положительный и отрицательный заряд и при нейтральных pH электронейтральны.
Фосфатидилсерин и фосфатидилинозит имеют по одному, а кардиолипин - два нескомпенсированных отрицательных заряда.
Жирные кислоты, входящие в состав липидов биологических мембран, обычно имеют от 14 до 22 углеродных атомов. Углеводородные цепи могут быть полностью насыщенными либо содержать несколько двойных связей (обычно во втором положении глицеринового остатка). Двойные связи почти всех жирных кислот находятся в цис-конформации. Состав внутреннего наружного слоев может различаться.
Белковыйсостав: большинство мембран содержит большое число различных белков, молекулярная масса которых колеблется от 10 000 до 240 000.
Белки либо частично, либо целиком погружены в липидный слой мембран или пронизывают его насквозь. Это происходит в зависимости от степени гидрофобности, числа и локализации гидрофобных аминокислотных остатков в полипептидной цепи. Наиболее слабо связаны с мембраной так называемые периферические белки, которые удерживаются в мембране за счет слабых, в основном неэлектростатических, взаимо-действий. Белки, сильно связанные с липидами и глубоко погруженные в липидный слой, так называемые интегральные белки, составляют основную массу мембранных белков. Обычно в полипептидных цепях этих белков много неполярных аминокислотных остатков.
В функциональном отношении мембранные белки подразделяются на: ферментативные, транспортные и регуляторные. Выделяют также структурные белки, которые выполняют в основном «опорно-строительные» функции.
О воде(не надо, но вдруг): мембранную воду подразделяют на связанную, свободную и захваченную. Внутренняя связанная вода наименее подвижна, находится в виде одиночных молекул в углеводородной зоне мембран. Основная часть связанной воды -вода гидратных оболочек. Они образуются главным образом вокруг полярных частей молекул липидов и белков. Гидратные оболочки основных структурообразующих липидов состоят обычно из 10-12 молекул воды. Эта вода осмотически неактивна, не способна растворять какие-либо вещества.
По подвижности: свободная вода подвижнее слабосвязанной, а та подвижнее гидратной.
Свободная вода входит в состав мембран в виде самостоятельной фазы и обладает изотропным движением, характерным для жидкой воды. (В изотропной среде направление движения поверхности фиксированной фазы совпадает с направлением движения энергии световой волны.) Захваченная вода (в центральной части мембран между липидными бислоями) подвижна, как и жидкая свободная вода, но медленно обменивается с внешней водой из-за физической разобщенности.
Белки «плавают» в липидном слое в виде отдельных глобул и имеют определенную подвижность. Их активность зависит от фазового состояния липидов и вязкости мембраны.
Характер взаимодействия полярных и неполярных групп белка и липидного бислоя приводит к тому, что пептид должен быть расположен так, чтобы максимально возможное количество неполярных аминокислотных остатков было погружено в бислой. Это очевидное требование определяет характер трех основных типов белок-мембранных комплексов, которые включают бетта-складчатые и альфа-спиральные структуры с различным соотношением полярных и неполярных групп.
Три типа белок-мембранных взаимодействий:
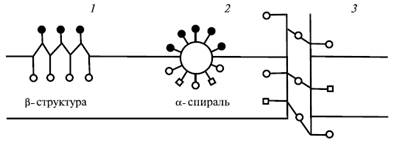
1) амфифильная бетта-структура
2) альфа-спираль амфифильная
3) альфа-спираль равномерно гидрофобная
черные кружки соответствуют заряженным боковым цепям;
квадраты - полярным, но незаряженным, белые кружки - неполярным боковым цепям
Амфифильные бетта-структуры: заборчик, вниз торчат неполярные боковые цепи, вверх – заряженные боковые цепи. Предполагается, что амфифильные бетта-складчатые структуры сворачиваются с образованием пор для пассивной диффузии веществ через мембраны. Внутри такой поры расположены полярные, а снаружи в контакте с бислоем - неполярные группы.
Амфифильные альфа-спирали: кружочек, кнаружи мембраны торчат заряженные боковые цепи, внутрь мембраны – чередуясь полярные, но незаряженные, белые кружки - неполярные боковые цепи. Их образуют пептидные гормоны.
Равномерно гидрофобная альфа-спираль: прямоугольник, в, внутри и снаружи мембраны торчат полярные и неполярные боковые цепи. Эти структуры характерны для интегральных мембранных белков, пронизывающих мембраны своими а-спиралями (бактериородопсины).
Дата добавления: 2016-04-11; просмотров: 7093;
