Газообмен в легких и перенос газов кровью. 2 страница
Выраженные гравитационные влияния при вертикальном положении тела на распределение кровотока по легким связаны у человека с низким уровнем внутрисосудистого давления крови в малом круге кровообращения. Среднее давление в легочной артерии человека на уровне сердца около 1.5-2.0 кПа (15-20 см вод.ст.). В артериальных сосудах верхних отделов легких оно снижено на величину гидростатического давления столба крови, равного расстоянию по вертикали между этими отделами и уровнем сердца. На рис.8.5 схематически представлено подразделение легких на функциональные зоны Веста в зависимости от соотношения в них давления в альвеолах (РА), мелких артериях (Ра) и мелких легочных венах (Pv).
В верхушках легких (зона 1) могут существовать области с давлением в легочных артериях (особенно в фазу диастолы) ниже
350




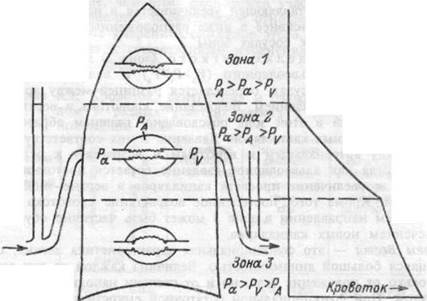
Рис.8.5. Модель, связывающая неравномерность распределения легочного кровотока при вертикальном положении тела человека с величиной давления, действующего на капилляры.
В зоне 1 (верхушка) альвеолярное давление (Рд) превышает давление в артериолах (Pa ) и кровоток ограничен. В зоне 2, где Ра>Рд, кровоток больше, чем в зоне 1. В зоне 3 кровоток усилен и определяется разностью давления в артериолах (Р ) и давления в венулах (РV). В центре вхемы легкого — легочные капилляры; вертикальные трубочки по сторонам легкого — манометры.
 альвеолярного (PA>Pa>Pv). При этом капилляры полностью спадаются, и кровоток через них становится невозможным. Такая ситуация в норме не наблюдается, поскольку давление в легочных артериях достаточно, чтобы "поднять" кровь до верхушек, однако, она может возникнуть в результате снижения артериального давления (например, при значительной кровопотере) или увеличении альвеолярного давления (при искусственной вентиляции под положительным давлением). Вентилируемые, но не снабжаемые кровью, т.е. не участвующие в газообмене, участки легких называют альвеолярным мертвым пространством.
альвеолярного (PA>Pa>Pv). При этом капилляры полностью спадаются, и кровоток через них становится невозможным. Такая ситуация в норме не наблюдается, поскольку давление в легочных артериях достаточно, чтобы "поднять" кровь до верхушек, однако, она может возникнуть в результате снижения артериального давления (например, при значительной кровопотере) или увеличении альвеолярного давления (при искусственной вентиляции под положительным давлением). Вентилируемые, но не снабжаемые кровью, т.е. не участвующие в газообмене, участки легких называют альвеолярным мертвым пространством.
В средней части легких (в зоне 2) давление в артериях под действием гидростатических сил увеличивается и становится выше альвеолярного (Pa>PA>Pv). Альвеолярное давление все еще превышает венозное, поэтому величину кровотока определяет разность между артериальным и альвеолярным давлением, а не арте-рио-венозный градиент давлений. Поскольку альвеолярное давление
351


 во всех отделах легких одинаково, а артериальное давление за счет гидростатической составляющей увеличивается в направлении сверху вниз, кровоток интенсивнее в ниже расположенных и, следовательно, более растянутых сосудах зоны 2.
во всех отделах легких одинаково, а артериальное давление за счет гидростатической составляющей увеличивается в направлении сверху вниз, кровоток интенсивнее в ниже расположенных и, следовательно, более растянутых сосудах зоны 2.
В нижних отделах легкого (зона 3) давление в легочных венах выше альвеолярного (РА>РV>Ра) и величина кровотока, как и в обычных сосудах, определяется разницей между артериальным и венозным давлением. Возрастание кровотока в верхне-нижнем направлении в этой зоне обусловлено, главным образом, расширением легочных капилляров. Давление в них соответствует среднему между артериальным и венозным и возрастает к основаниям легких, тогда как альвеолярное давление остается постоянным. Это приводит к увеличение просвета капилляров в верхне-нижнем направлении. Кроме того, постепенное возрастание кровотока в верхне-нижнем направлении в зоне 3 может быть частично обусловлено вовлечением новых капилляров.
Зоны Веста — это функциональная характеристика легких, отличающаяся большой динамичностью. Величина каждой из зон зависит не только от положения тела, но и от степени наполненности легких воздухом. При функциональной остаточной емкости легких распределение кровотока таково, что зона 2 занимает две три легких, а при остаточном объеме (после усиленного выдоха) все легкое можно отнести к зоне 3. При малом объеме легких снижается кровоток, преимущественно в области оснований легких, где легочная паренхима расправлена слабее. Причиной такого снижения является здесь сужение внеальвеолярных сосудов при недостаточном расправлении легких. Эти участки иногда называют зоной 4.
Вертикальное положение тела оказывает влияние на распределение не только легочного кровотока, но и вентиляции. Поскольку у человека в вертикальном положении существует градиент плеврального давления от верхушек к основанию легких, обусловленный собственной массой тканей легкого, а также других органов грудной полости, то альвеолы верхушек имеют большие размеры, а стенка их растянута и более напряжена, чем у альвеол нижних участков легких. Альвеолы с разной степенью растяжения вентилируются неравнозначно. Прирашение объема альвеол при одном и том же сдвиге транспулъмонального давления непропорционально меньше в растянутых альвеолах верхушки легких, чем в альвеолах основания.
Смещая однонаправленно интенсивность кровотока и вентиляции от верхних участком легких к нижним, гравитация, тем не менее, не обеспечивает в каждом из них оптимальное соответствие кровотока и вентиляции в различных функциональных легочных единицах {адекватности вентиляционно-перфузионных отношений), от которого в конечном итоге зависит эффективность легких как газооб-менного органа. При положении человека стоя или сидя кровь в капилляры верхушек легких почти не поступает и вентиляционно-перфузионное отношение для верхних отделов легких оказывается существенно увеличенным, несмотря на то, что их вентиляция также снижена, но в меньшей степени (табл.8.1). Кровоток, как пра-
352


 вило, тем больше, чем ниже расположен участок легкого. В нижних отделах вентиляционно- перфузионное отношение умеренно понижено. Однако, такое умеренное снижение этого отношения (до 0.7-0.6) еще не приводит к существенным изменениям в насыщении крови кислородом (см. табл.8.1).
вило, тем больше, чем ниже расположен участок легкого. В нижних отделах вентиляционно- перфузионное отношение умеренно понижено. Однако, такое умеренное снижение этого отношения (до 0.7-0.6) еще не приводит к существенным изменениям в насыщении крови кислородом (см. табл.8.1).
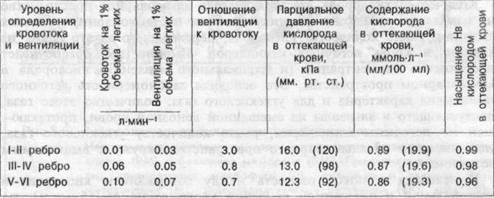
Таблица 8.1. Кровоток, вентиляция и насыщение крови кислородом в разных участках легких у здорового человека в положении сидя.
Механизмами, корригирующими в легких соответствие локального кровотока объему локальной вентиляции, являются вазомоторные и бронхомоторные ответы на изменение газового состава альвеолярного воздуха, а именно — вазоконстрикция при снижении в альвеолах парциального давления кислорода или при повышении в них парциального давления углекислого газа и бронхоконстрикция — в случае снижения альвеолярного парциального давления углекислого газа.
Локальный кровоток и локальная вентиляция являются взаиморе-гулируемыми параметрами: в гиповентилируемых участках кровоток снижается в результате возникающей в них гипоксической и гипер-капнической вазоконстрикции, а в участках с пониженным (по отношению к вентиляции) кровотоком гипокапническая бронхокон-стрикция вызывает уменьшение вентиляции. Действующие в этих случаях легочные регуляторные механизмы направлены на поддержание адекватных вентиляционно-перфузионных отношений в различных отделах легких, представляя собой ауторегуляцию газообмена в этом органе. Констрикция легочных сосудов проявляется уже при небольшом понижении парциального давления кислорода в альвеолах, например, при вентиляции легких гипоксической газовой смесью, содержащей 15- 16% кислорода. Следовательно, указанные ауто-регуляторные реакции могут возникать в обычных условиях в тех альвеолах, которые заполняются во время вдоха первыми и получают воздух с низким содержанием кислорода, оставшийся в дыхательном мертвом пространстве в конце предыдущего выдоха. Возникающая при этом вазоконстрикция ограничивает или даже прекращает кровоток в этих альвеолах, который направляется в другие группы альвеол.
353





 Увеличение бронхотонуса при уменьшении легочного кровотока обусловлено действием на гладкую мускулатуру бронхов, возникающей при этом, гипокапнии. Для возникновения гипокапнической бронхо-констрикции имеет значение рН притекающей к легким крови; снижение концентрации водородных ионов в крови усиливает бронхокон-стрикторную реакцию на гипокапнию.
Увеличение бронхотонуса при уменьшении легочного кровотока обусловлено действием на гладкую мускулатуру бронхов, возникающей при этом, гипокапнии. Для возникновения гипокапнической бронхо-констрикции имеет значение рН притекающей к легким крови; снижение концентрации водородных ионов в крови усиливает бронхокон-стрикторную реакцию на гипокапнию.
Газообмен в легких и перенос газов кровью.
Количество кислорода, поступающего в альвеолярное пространство из вдыхаемого воздуха в единицу времени в стационарных условиях дыхания, равно количеству кислорода, переходящего за это время из альвеол в кровь легочных капилляров. Именно это обеспечивает постоянство концентрации (и парциального давления) кислорода в альвеолярном пространстве. Эта основная закономерность легочного газообмена характерна и для углекислого газа: количество этого газа, поступающего в альвеолы из смешанной венозной крови, протекающей по легочным капиллярам, равно количеству углекислого газа, удаляющегося из альвеолярного пространства наружу с выдыхаемым воздухом.
У человека в покое разность между содержанием кислорода в артериальной и смешанной венозной крови равна 45-55 мл О2 на 1 л крови, а разность между содержанием углекислого газа в венозной и артериальной крови составляет 40- 50 мл СО2 на 1 л крови. Это значит, что в каждый литр крови, протекающей по легочным капиллярам, поступает из альвеолярного воздуха примерно 50 мл О2, а из крови в альвеолы — 45 л СО2. Концентрация О2 и СО2 в альвеолярном воздухе остается при этом практически постоянной, благодаря вентиляции альвеол.
Обмен газов между альвеолярным воздухом и кровью.Альвеолярный воздух и кровь легочных капилляров разделяет так называемая альвеолярно-капиллярная мембрана, толщина которой варьирует от 0.3 до 2.0 мкм. Основу альвеолярно-капиллярной мембраны составляет альвеолярный эпителий и капиллярный эндотелий, каждый из которых расположен на собственной базальной мембране и образует непрерывную выстилку, соответственно, альвеолярной и внутрисосудистой поверхности. Между эпителиальной и эндотелиальной базальными мембранами находится интерстиций. В отдельных участках базальные мембраны практически прилегают друг к другу (рис.8.6).
Обмен респираторных газов осуществляется через совокупность субмикроскопических структур, содержащих гемоглобин эритроцитов, плазму крови, капиллярный эндотелий и его две плазматические мембраны, сложный по составу соединительнотканный слой, альвеолярный эпителий с двумя плазматическими мембранами, наконец, внутренюю выстилку альвеол — сурфактант (поверхностно-активное вещество). Последний имеет толщину около 50 нм, представляет собой комплекс фосфолипидов, белков и полисахаридов и постоянно вырабатывается клетками альвеолярного эпителия, подвергаясь раз-
354




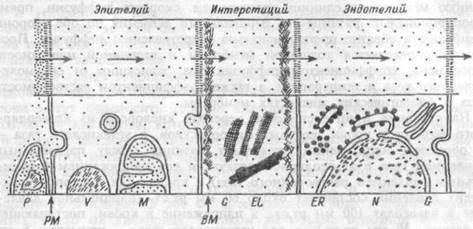
Рис.8.6. Альвеолярно-капиллярная мембрана (схема).
Непрерывные компоненты аэрогематического барьера: оболочка клеток (РМ) и базальная мембрана (ВМ). Прерывистые компоненты: альвеолярные макрофаги (Р), пузырьки и вакуоли (V), митохондрии (М), эндоплазматический ретикулум (ER), ядра (N), пластинчатый комплекс (G), коллагеновые (С) и эластические (EL) волокна соединительной ткани.
 рушению с периодом полураспада 12-16 часов. Наслоение сурфак-танта на эпителиальную выстилку альвеолы создает дополнительную к альвеолярно-капиллярной мембране диффузионную среду, которую газы преодолевают при их массопереносе. За счет сурфактанта удлиняется расстояние для диффузии газов, что приводит к небольшому снижению концентрационного градиента на альвеолярно-капиллярной мембране. Однако, без сурфактанта дыхание вообще было 6ы невозможно, так как стенки альвеолы слиплись бы под действием значительного поверхностного натяжения, присущего альвеолярному эпителию. Сурфактант снижает поверхностное натяжение альвеолярных стенок до близких к нулевым величинам и тем самым: а) создает возможность расправления легкого при первом вдохе новорожденного, б) препятствует развитию ателектазов при выдохе, в) обеспечивает до 2/3 эластического сопротивления ткани легкого взрослого человека и стабильность структуры респираторной зоны, г) регулирует скорость абсорбции кислорода по границе раздела фаз газ-жидкость и интенсивность испарения воды с альвеолярной поверхности. Сурфактант также очищает поверхность альвеол от попавших с дыханием инородных частиц и обладает бактериостатичес-кой активностью.
рушению с периодом полураспада 12-16 часов. Наслоение сурфак-танта на эпителиальную выстилку альвеолы создает дополнительную к альвеолярно-капиллярной мембране диффузионную среду, которую газы преодолевают при их массопереносе. За счет сурфактанта удлиняется расстояние для диффузии газов, что приводит к небольшому снижению концентрационного градиента на альвеолярно-капиллярной мембране. Однако, без сурфактанта дыхание вообще было 6ы невозможно, так как стенки альвеолы слиплись бы под действием значительного поверхностного натяжения, присущего альвеолярному эпителию. Сурфактант снижает поверхностное натяжение альвеолярных стенок до близких к нулевым величинам и тем самым: а) создает возможность расправления легкого при первом вдохе новорожденного, б) препятствует развитию ателектазов при выдохе, в) обеспечивает до 2/3 эластического сопротивления ткани легкого взрослого человека и стабильность структуры респираторной зоны, г) регулирует скорость абсорбции кислорода по границе раздела фаз газ-жидкость и интенсивность испарения воды с альвеолярной поверхности. Сурфактант также очищает поверхность альвеол от попавших с дыханием инородных частиц и обладает бактериостатичес-кой активностью.
Переход газов через альвеоло- капиллярную мембрану происходит по законам диффузии, но при растворении газов в жидкости процесс диффузии резко замедляется. Углекислый газ, например, диффундирует в жидкости примерно в 13000 раз, а кислород — в 300000 раз мед-
355

 леннее, чем в газовой среде. Количество газа, проходящее через легочную мембрану в единицу времени, т.е. скорость диффузии, прямо пропорциональна разнице его парциального давления по обе стороны мембраны и обратно пропорциональна сопротивлению диффузии. Последнее определяется толщиной мембраны и величиной поверхности газообмена, коэффициентом диффузии газа, зависящим от его молекулярного веса и температуры, а также коэффициентом растворимости газа в биологических жидкостях мембраны.
леннее, чем в газовой среде. Количество газа, проходящее через легочную мембрану в единицу времени, т.е. скорость диффузии, прямо пропорциональна разнице его парциального давления по обе стороны мембраны и обратно пропорциональна сопротивлению диффузии. Последнее определяется толщиной мембраны и величиной поверхности газообмена, коэффициентом диффузии газа, зависящим от его молекулярного веса и температуры, а также коэффициентом растворимости газа в биологических жидкостях мембраны.
Направление и интенсивность перехода кислорода из альвеолярного воздуха в кровь легочных микрососудов, а углекислого газа — в обратном направлении определяет разница между парциальным давлением газа в альвеолярном воздухе и его напряжением (парциальным давлением растворенного газа) в крови. Для кислорода градиент давления составляет около 60 мм рт.ст. (парциальное давление в альвеолах 100 мм рт.ст., а напряжение в крови, поступающей в легкие, 40 мм рт.ст.), а для углекислого газа — примерно 6 мм рт.ст. (парциальное давление в альвеолах 40 мм рт.ст., напряжение в притекающей к легким крови 46 мм рт.ст.).
Сопротивление диффузии кислорода в легких создают альвеоляр-но-капиллярная мембрана, слой плазмы в капиллярах, мембрана эритроцита и слой его протоплазмы. Поэтому общее сопротивление диффузии кислорода в легких слагается из мембранного и внутри-капиллярного компонентов. Биофизической характеристикой проницаемости аэрогематического барьера легких для респираторных газов является так называемая диффузионная способность легких. Это количество мл газа, проходящее через легочную мембрану в 1 минуту при разнице парциального давления газа по обе стороны мембраны 1 мм рт.ст. У здорового человека в покое диффузионная способность легких для кислорода равна 20-25 мл мин -1 мм рт.ст.-1.
Величина диффузионной способности легких зависит от их объема и соответствующей ему площади поверхности газообмена. Этим в значительной мере объясняется тот факт, что величина диффузионной способности легких у мужчин обычно больше,чем у женщин, а также то, что величина диффузионной способности легких при задержке дыхания на глубоком вдохе оказывается большей, чем в устойчивом состоянии на уровне функциональной остаточной емкости. За счет гравитационного перераспределения кровотока и объема крови в легочных капиллярах диффузионная способность легких в положении лежа больше, чем в положении сидя, а сидя — больше, чем в положении стоя. С возрастом диффузионная способность легких снижается.
Транспорт кислорода кровью.Кислород в крови находится в растворенном виде и в соединении с гемоглобином. В плазме растворено очень небольшое количество кислорода. Поскольку растворимость кислорода при 37 °С составляет 0.225 мл * л-1 * кПа-1 (0.03 мл-л-1 мм рт.ст.-1), то каждые 100 мл плазмы крови при напряжении кислорода 13.3 кПа (100 мм рг.ст.) могут переносить в растворенном состоянии лишь 0.3 мл кислорода. Это явно недостаточно для жиз-

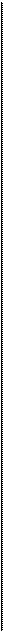 недеятельности организма. При таком содержании кислорода в крови и условии его полного потребления тканями минутный объем крови в покое должен был бы составлять более 150 л/мин. Отсюда ясна важность другого механизма переноса кислорода путем его соединения с гемоглобином.
недеятельности организма. При таком содержании кислорода в крови и условии его полного потребления тканями минутный объем крови в покое должен был бы составлять более 150 л/мин. Отсюда ясна важность другого механизма переноса кислорода путем его соединения с гемоглобином.
Каждый грамм гемоглобина способен связать 1.39 мл кислорода и, следовательно, при содержании гемоглобина 150 г/л каждые 100 мл крови могут переносить 20.8 мл кислорода. Величина, отражающая количество кислорода, которое может связаться с гемоглобином при его полном насыщении, называется кислородной емкостью гемоглобина. Другим показателем дыхательной функции крови является содержание кислорода в крови, которое отражает истинное количество кислорода, как связанного с гемоглобином, так и физически растворенного в плазме. В 100 мл артериальной крови в норме содержится 19-20 мл кислорода, в таком же объеме венозной крови — 13-15 мл кислорода, при этом артерио-венозная разница составляет 5-6 мл. Отношение количества кислорода, связанного с гемоглобином, к кислородной емкости последнего является показателем степени насыщения гемоглобина кислородом. Насыщение гемоглобина артериальной крови кислородом у здоровых лиц составляет 96%.
Образование оксигемоглобина в легких и его восстановление в тканях находится в зависимости от парциального напряжения кислорода крови: при его повышении. Насыщение гемоглобина кислородом возрастает, при понижении — уменьшается. Эта связь носит нелинейный характер и выражается кривой диссоциации оксигемоглобина, имеющей S-образную форму (рис.8.7). Оксигенированной артериальной крови соответствует плато кривой диссоциации, а десатурированной крови в тканях — круто снижающаяся ее часть. Пологий подъем кривой в верхнем ее участке (зона высокого напряжения О,) свидетельствует, что достаточно полное насыщение
 |  | ||
|
Рис.8.7. Кривая диссоциации оксигемоглобина.
1 — при увеличении
рН, или уменьшении
температуры, или
уменьшении 2,3-ДФГ;
2 — нормальная
кривая при рН 7,4 и
37°С;
3 — при уменьшении
рН или увеличении
температуры или
увеличении 2,3-ДФГ.
 357
357


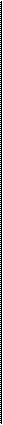

 гемоглобина артериальной крови кислородом обеспечивается даже при уменьшении напряжения О2 до 9.3 кПа (70 мм рт.ст.). Понижение напряжения О,, с 13.3 кПа на 2.0-2.7 кПа (со 100 на 15-20 мм рт.ст.) практически не отражается на насыщении гемоглобина кислородом (НЬО2 снижается при этом на 2-3%). При более низких значениях напряжения О2 оксигемоглобин диссоциирует значительно легче (зона крутого падения кривой). Так, при снижении напряжения О2 с 8.0 до 5.3 кПа (с 60 до 40 мм рт.ст.) насыщение гемоглобина кислородом уменьшается приблизительно на 15%.
гемоглобина артериальной крови кислородом обеспечивается даже при уменьшении напряжения О2 до 9.3 кПа (70 мм рт.ст.). Понижение напряжения О,, с 13.3 кПа на 2.0-2.7 кПа (со 100 на 15-20 мм рт.ст.) практически не отражается на насыщении гемоглобина кислородом (НЬО2 снижается при этом на 2-3%). При более низких значениях напряжения О2 оксигемоглобин диссоциирует значительно легче (зона крутого падения кривой). Так, при снижении напряжения О2 с 8.0 до 5.3 кПа (с 60 до 40 мм рт.ст.) насыщение гемоглобина кислородом уменьшается приблизительно на 15%.
Положение кривой диссоциации оксигемоглобина количественно принято выражать парциальным напряжением кислорода, при котором насыщение гемоглобина составляет 50% (Р50). Нормальная величина Р50 при температуре 37°С и рН 7.40 — около 3.53 кПа (26.5 мм рт.ст.).
Кривая диссоциации оксигемоглобина при определенных условиях может смещаться в ту или иную сторону, сохраняя S- образную форму, под влиянием изменения рН, напряжения СО2 температуры тела, содержания в эритроцитах 2,3-дяфосфоглицерата (2,3-ДФГ), от которых зависит способность гемоглобина связывать кислород. В работающих мышцах в результате интенсивного метаболизма повышается образование СО2 и молочной кислоты, а также возрастает теплопродукция. Все эти факторы понижают сродство гемоглобина к кислороду. Кривая диссоциации при этом сдвигается вправо (рис.8.7), что приводит к более легкому освобождению кислорода из оксигемоглобина, и возможность потребления тканями кислорода увеличивается. При уменьшении температуры, 2,3-ДФГ, снижении напряжения СО, и увеличении рН кривая диссоциации сдвигается влево, сродство гемоглобина к кислороду возрастает, в результате чего доставка кислорода к тканям уменьшается.
Транспорт кровью углекислого газа.Являясь конечным продуктом обмена веществ, СО2 находится в организме в растворенном и связанном состоянии. Коэффициент растворимости СО2 составляет 0.231 ммольл-1 * кПа-1 (0.0308 ммольл-1 * мм рт.ст-1.), что почти в 20 раз выше, чем у кислорода. Однако, в растворенном виде переносится меньше 10% всего количества СО,, транспортируемого кровью. В основном, СО, переносится в химически связанном состоянии, главным образом, в виде бикарбонатов, а также в соединении с белками (так называемые карбоминовые, или карбосоединения).
В артериальной крови напряжение СО2 5.3 кПа (40 мм рт.ст.), в интерстициальной жидкости его напряжение составляет 8.0- 10.7 кПа (60-80 мм рт.ст.). Благодаря этим градиентам, образующийся в тканях СО2 переходит из интерстициальной жидкости в плазму крови, а из нее — в эритроциты. Вступая в реакцию с водой, СО2 образует угольную кислоту: СО2 + Н2О <> Н2СО3. Реакция эта обратима и в тканевых капиллярах идет преимущественно в сторону образования Н2СО3 (рис.8.8.А). В плазме эта реакция протекает медленно, но в эритроцитах образование угольной кислоты под влиянием фермента ускоряет реакцию гидратации СО2 в 15000-20000 раз. Угольная кислота диссоциирует на ионы Н+ и НСО3. Когда содержание ионов
358
 НСО3 повышается, они диффундируют их эритроцита в плазму, а ионы Н+ остаются в эритроците, так как мембрана эритроцита сравнительно непроницаема для катионов. Выход ионов НСО3 в плазму уравновешивается поступлением из плазмы ионов хлора. При этом в плазме высвобождаются ионы натрия, которые связываются поступающими из эритроцита ионами НСО3, образуя NaHCO3. Гемоглобин и белки плазмы, проявляя свойства слабых кислот, образуют соли в эритроцитах с калием, а в плазме с натрием. Угольная кислота обладает более сильными кислотными свойствами, поэтому при ее взаимодействии с солями белков ион Н+ связывается с белковым анионом, а ион НСО3 с соответствующим катионом образует бикарбонат (в плазме NaHCO3, в эритроците КНСО3).
НСО3 повышается, они диффундируют их эритроцита в плазму, а ионы Н+ остаются в эритроците, так как мембрана эритроцита сравнительно непроницаема для катионов. Выход ионов НСО3 в плазму уравновешивается поступлением из плазмы ионов хлора. При этом в плазме высвобождаются ионы натрия, которые связываются поступающими из эритроцита ионами НСО3, образуя NaHCO3. Гемоглобин и белки плазмы, проявляя свойства слабых кислот, образуют соли в эритроцитах с калием, а в плазме с натрием. Угольная кислота обладает более сильными кислотными свойствами, поэтому при ее взаимодействии с солями белков ион Н+ связывается с белковым анионом, а ион НСО3 с соответствующим катионом образует бикарбонат (в плазме NaHCO3, в эритроците КНСО3).
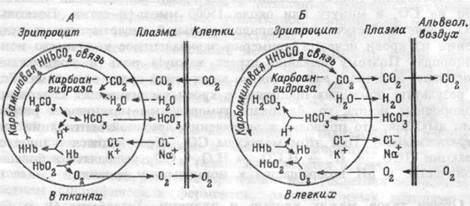
Рис.8.8. Схема процессов, происходящих в плазме и эритроцитах при газообмене в тканях (А) и легких (Б).
 В крови тканевых капилляров одновременно с поступлением СО2 внутрь эритроцита и образованием в нем угольной кислоты происходит отдача кислорода оксигемоглобином. Восстановленный гемоглобин представляет собой более слабую кислоту (т.е. лучший акцептор протонов), чем оксигенированный. Поэтому он легче связывает водородные ионы, образующиеся при диссоциации угольной кислоты. Таким образом, присутствие восстановленного гемоглобина в венозной крови способствует связыванию СО2 тогда как образование оксигемоглобина в легочных капиллярах облегчает отдачу углекислого газа.
В крови тканевых капилляров одновременно с поступлением СО2 внутрь эритроцита и образованием в нем угольной кислоты происходит отдача кислорода оксигемоглобином. Восстановленный гемоглобин представляет собой более слабую кислоту (т.е. лучший акцептор протонов), чем оксигенированный. Поэтому он легче связывает водородные ионы, образующиеся при диссоциации угольной кислоты. Таким образом, присутствие восстановленного гемоглобина в венозной крови способствует связыванию СО2 тогда как образование оксигемоглобина в легочных капиллярах облегчает отдачу углекислого газа.
В переносе кровью СО2 большое значение имеет также химическая связь СО2 с конечными аминогруппами белков крови, важнейший из которых — глобин в составе гемоглобина. В результате реакции с глобином образуется так называемый карбаминогемогло-бин. Восстановленый гемоглобин обладает большим сродством к СО2, чем оксигемоглобин. Таким образом, диссоциация оксигемоглобина в тканевых капиллярах облегчает связывание СО2, а в легких образование оксигемоглобина способствует выведению углекислого газа.
359


 Из общего количества СО,, которое может быть извлечено из крови, лишь 8-10% СО, находится в соединении с гемоглобином. Однако, роль этого соединения в транспорте СО2 кровью достаточно велика. Примерно 25- 30% СО2, поглощаемого кровью в капиллярах большого круга, вступает в соединение с гемоглобином, а в легких — выводится из крови.
Из общего количества СО,, которое может быть извлечено из крови, лишь 8-10% СО, находится в соединении с гемоглобином. Однако, роль этого соединения в транспорте СО2 кровью достаточно велика. Примерно 25- 30% СО2, поглощаемого кровью в капиллярах большого круга, вступает в соединение с гемоглобином, а в легких — выводится из крови.
Когда венозная кровь поступает в капилляры легких, напряжение СО2 в плазме снижается и находящийся внутри эритроцита в физически растворенном виде СО2 выходит в плазму. По мере этого, Н2СО3 превращается в СО2 и воду (рис.8.8.Б), причем карбоангидраза катализирует реакцию, идущую в этом направлении. Н2СО3 для такой реакции доставляется в результате соединения ионов НСО3 с ионами водорода, высвобождающихся из связи с белковыми анионами.
В состоянии покоя с дыханием из организма человека удаляется 230 мл СО2 в минуту или около 15000 ммоль в сутки. Поскольку СО2 является "летучим" ангидридом угольной кислоты, при его удалении из крови исчезает примерно эквивалентное количество ионов водорода. Поэтому дыхание играет важную роль в поддержании кислотно-щелочного равновесия во внутренней среде организма. Если в результате обменных процессов в крови увеличивается содержание водородных ионов, то, благодаря гуморальным механизмам регуляции дыхания, это приводит к увеличению легочной вентиляции {гипервентиляции). При этом молекулы СО2, образующиеся в процессе реакции НСО3 + Н+ -> Н2СО3 -> Н2О + СО2, выводятся в большем количестве и рН возвращается к нормальному уровню.
Обмен газов между кровью и тканями.Газообмен О2 и СО2 между кровью капилляров большого круга и клетками тканей осуществляется путем простой диффузии. Перенос дыхательных газов (О2 — из крови в ткани, СО2 — в обратном направлении) происходит под действием концентрационного градиента этих газов между кровью в капиллярах и интерстициальной жидкостью. Разность напряжения О2 по обе стороны стенки кровеносного капилляра, обеспечивающая его диффузию из крови в интерстициальную жидкость, составляет от 30 до 80 мм рт.ст. (4.0-10.7 кПа). Напряжение СО2 в интерстициальной жидкости у стенки кровеносного капилляра на 20-40 мм рт.ст. (2.7-5.3 кПа) больше, чем в крови. Поскольку СО2 диффундирует примерно в 20 раз быстрее, чем кислород, удаление СО2 происходит гораздо легче, чем снабжение кислородом.
Дата добавления: 2016-03-27; просмотров: 4810;
