Характеристика компонентов и фаз диаграммы
Кристаллизуясь (см. рис. 4.1, б), железо может существовать в двух полиморфных (аллотропных) модификациях : 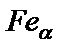 (a – железо) – от 1539 до 1392 °С и от 911°С и ниже, с объемно-центрированной кристаллической решеткой (ОЦК) и
(a – железо) – от 1539 до 1392 °С и от 911°С и ниже, с объемно-центрированной кристаллической решеткой (ОЦК) и 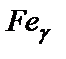 (g – железо) – в интервале температур от 1392 °С до 911 °С с гранецентрированной решеткой (ГЦК).
(g – железо) – в интервале температур от 1392 °С до 911 °С с гранецентрированной решеткой (ГЦК).
Взаимодействуя с углеродом, 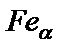 и
и 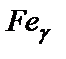 могут образовывать, во-первых, ограниченные твердые растворы и, во-вторых, химические соединения. Таким образом, на диаграмме Fe – Fe3C могут образовываться следующие четыре фазы:
могут образовывать, во-первых, ограниченные твердые растворы и, во-вторых, химические соединения. Таким образом, на диаграмме Fe – Fe3C могут образовываться следующие четыре фазы:
1) жидкость (жидкий раствор углерода в железе), существует выше линии ликвидус (ABCD). Обозначается буквой Ж;
2) ограниченный твердый раствор углерода в 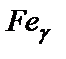 , то есть
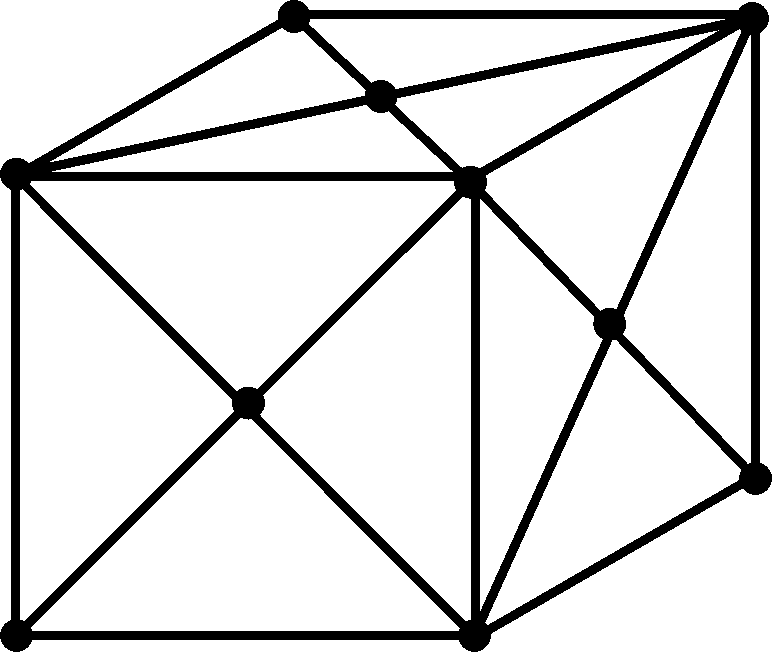
, то есть 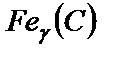 , с максимальной растворимостью углерода 2,14 %, при температуре 1147 °С (т. Е). При снижении температуры от 1147 °С до 7270С растворимость углерода в этой фазе уменьшается по линии ES до 0,8 % С (т. S). Эта фаза называется аустенитом (А). Кристаллическая решетка аустенита показана на рис. 4.2, а. Аустенит является высокотемпературной фазой;
, с максимальной растворимостью углерода 2,14 %, при температуре 1147 °С (т. Е). При снижении температуры от 1147 °С до 7270С растворимость углерода в этой фазе уменьшается по линии ES до 0,8 % С (т. S). Эта фаза называется аустенитом (А). Кристаллическая решетка аустенита показана на рис. 4.2, а. Аустенит является высокотемпературной фазой;
3) ограниченный твердый раствор углерода в 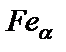 , то есть
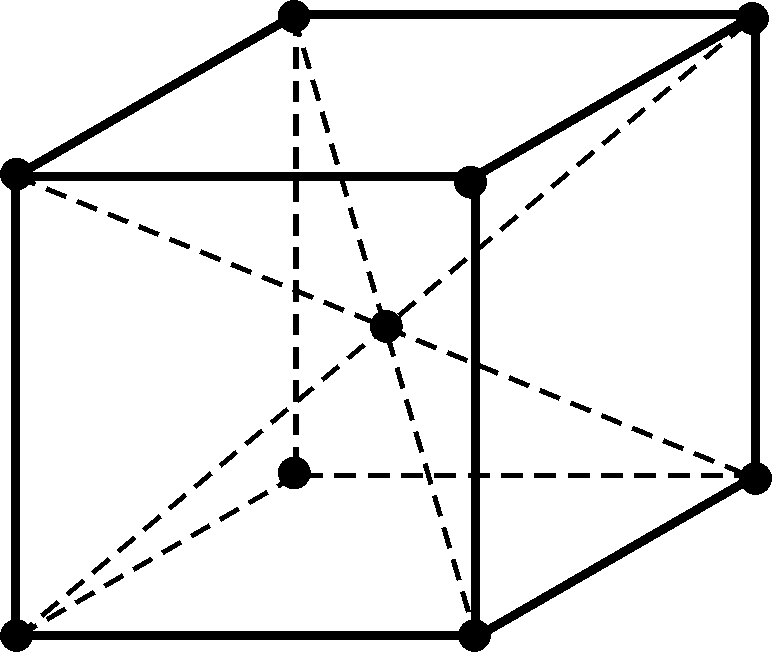
, то есть 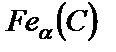 с максимальной растворимостью углерода, равной 0,025 %, при температуре 727 оС (т. Р). При понижении температуры от 727 °С до комнатной растворимость углерода уменьшается по линии PQ до 0,006 %. Эту фазу называют ферритом (Ф). Кристаллическая решетка феррита показана (рис. 4.2, б).
с максимальной растворимостью углерода, равной 0,025 %, при температуре 727 оС (т. Р). При понижении температуры от 727 °С до комнатной растворимость углерода уменьшается по линии PQ до 0,006 %. Эту фазу называют ферритом (Ф). Кристаллическая решетка феррита показана (рис. 4.2, б).
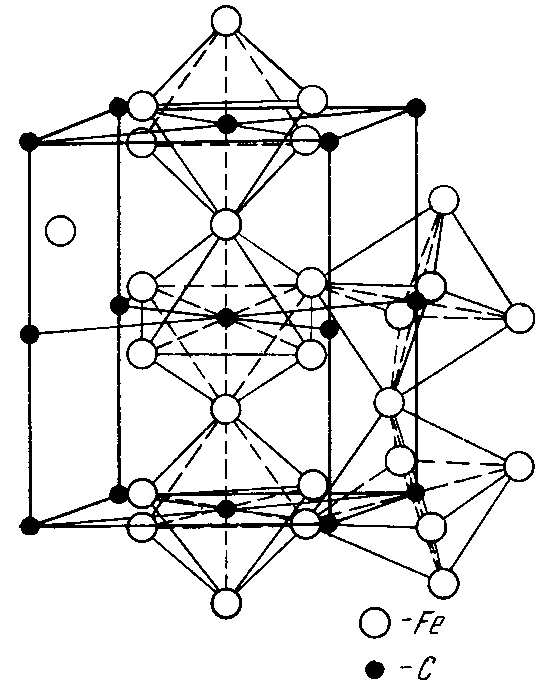
4) химическое соединение железа с углеродом – цементит (Fe3C – карбид железа), имеющий температуру кристаллизации 1250 °С, обладающий сложной ромбоэдрической кристаллической решеткой (рис. 4.2, в), содержащей при любой температуре 6,67 % углерода (остальное – железо). Так как цементит не взаимодействует, т.е. не растворяет в себе ни железо, ни углерод, то он является одновременно и компонентом системы и одной из фаз сплавов Fe – Fe3C.
| а) | б) | в) |
| 
| 
|
| г.ц.к. | о.ц.к. |
Рис. 4.2. Кристаллические решетки 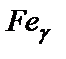 (а),
(а), 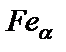 (б) и Fe3C (в)
(б) и Fe3C (в)
4.3. Фазовые превращения и формирование структур
по диаграмме Fe - Fe3C
Фазовые превращения, происходящие в системе Fe - Fe3C, можно подразделить на первичные (первичная кристаллизация – переход из жидкого состояния в твердое) и вторичные (перекристаллизации из одного твердого состояния в другое – тоже твердое).
Первичная кристаллизация идет по линиям ACD – ликвидус и AEСF – солидус. При температурах, соответствующих линии ACD (начало кристаллизации), из жидкого сплава начинают выделяться кристаллы твердой фазы, и при температурах, соответствующих линии AEСF, кристаллизация заканчивается.
В сплавах с содержанием углерода до 4,3 % кристаллизация начинается с выделения кристаллов аустенита, а в сплавах с содержанием углерода более 4,3 % – кристаллов цементита.
В сплавах, содержащих углерода до 2,14 % (в сталях), первичная кристаллизация заканчивается на участке линии солидус АЕ и в результате стали получают однородную структуру – аустенит 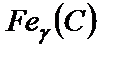 .
.
При охлаждении сплавов с содержанием углерода 2,14 – 4,3 % в интервале температур от линии ликвидус до линии солидус, вследствие образования аустенита, который в этом интервале температур содержит 2,14 %, т.е. меньше, чем начальная концентрация углерода в сплаве, остающаяся часть жидкой фазы обогащается углеродом до концентрации 4,3 % при достижении температуры 1147 °С.
В сплавах, содержащих углерода более 4,3 %, вследствие выпадения высокоуглеродистого цементита (С = 6,67 %), остающаяся в процессе охлаждения жидкая фаза обедняется углеродом до 4,3 % при температуре 1147 °С.
Таким образом, во всех сплавах, с содержанием углерода > 2,14 % (правее т. Е), оставшаяся жидкая фаза, при температуре 1147°С (линия ECF) имеет концентрацию углерода 4,3 %, называемую эвтектической концентрацией (или составом).
Согласно закономерностям кристаллизации по диаграмме с эвтектическим превращением жидкая фаза эвтектического состава должна перейти в твердую фазу – аустенит, но так как состав жидкой фазы – 4,3 %, а в аустените при температуре 1147 °С может раствориться только 2,14 % С (т. Е), то избыточный углерод (2,3 %) расходуется на образование цементита – Fe3C.
Поэтому на линии ECF кристаллизация происходит с одновременным выпадением кристаллов аустенита и цементита. Эта механическая смесь называется эвтектикой, или ледебуритом; превращение называется эвтектическим; происходит оно у всех сплавов при одной и той же температуре (1147° С), и на диаграмме, и на кривых охлаждения соответствует горизонтальному участку.
Формула эвтектического превращения:
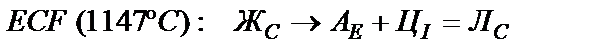 .
.
Обратите внимание, что эвтектическое превращение происходит только у сплавов с содержанием углерода более 2,14 %. Соответственно все железоуглеродистые сплавы делятся на стали (С < 2,14 %) и чугуны (С > 2,14 %).
Сплавы с содержанием углерода от 2,14 % до 4,3 % С называются доэвтектическими; сплав, имеющий 4,3 % С – эвтектическим, а сплавы, содержащие углерода более 4,3 % – заэвтектическими сплавами.
Вторичная кристаллизация (перекристаллизация в твердом состоянии) происходит по линиям: GS, SE, PSK, PQ, GP.
Она обусловлена существованием полиморфного 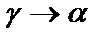 превращения, а также изменением растворимости углерода в
превращения, а также изменением растворимости углерода в 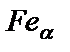 и
и 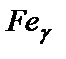 с понижением температуры. Наиболее характерным и важным является наличие эвтектоидного превращения, происходящего по линии PSK (727 °С). Рассмотрим это превращение.
с понижением температуры. Наиболее характерным и важным является наличие эвтектоидного превращения, происходящего по линии PSK (727 °С). Рассмотрим это превращение.
Аустенит 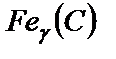 устойчив только при высоких температурах. При температурах, соответствующих линии РSK (температура 727 °С), начинается перекристаллизация, так как ниже этой линии аустенит существовать не может.
устойчив только при высоких температурах. При температурах, соответствующих линии РSK (температура 727 °С), начинается перекристаллизация, так как ниже этой линии аустенит существовать не может.
При этом у сплавов, содержащих углерода менее 0,8 %, при температурах, соответствующих линии GS, начинается переход аустенита в феррит. Вследствие выпадения феррита, растворимость углерода в котором значительно меньше, чем в аустените, последний обогащается углеродом и при температуре 727°С содержание углерода в аустените достигнет 0,8 %.
Вследствие того, что растворимость углерода в аустените с понижением температуры уменьшается (линия ES – с 2,14 % до 0,8 %), то из аустенита у всех сплавов, лежащих правее точки S (т.е. имеющих концентрацию углерода > 0,8 %), с понижением температуры от 1147 до 727 °С выделяется углерод в виде цементита вторичного, и при температуре 727°С, аустенит получает концентрацию углерода, равную 0,8 %.
Таким образом, у любого сплава, начиная с содержания углерода более 0,025 % (правее т. Р) на линии PSK (при температуре 727 °С), аустенит имеет концентрацию углерода равную 0,8 %, которая называется эвтектоидной концентрацией (или эвтектоидным составом).
Аустенит эвтектоидного состава при температуре 727 °С должен перейти в феррит, но поскольку в феррите при этой температуре может раствориться только 0,025 % углерода, то избыточный углерод (0,775 %) расходуется на образование цементита. Поэтому превращение на линии PSK происходит с одновременным выпадением кристаллов феррита и цементита, механическая смесь которых называется перлитом, а превращение называется эвтектоидным.
Формула эвтектоидного превращения:
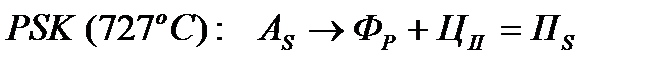 .
.
Эвтектоидное превращение, подобно эвтектическому, происходит при постоянной температуре и на диаграмме и кривых охлаждения соответствует горизонтальной линии.
Таким образом, образование эвтектики (ледебурита) и эвтектоида (перлита) объясняется разной растворимостью углерода в исходной фазе и фазе, которая должна образоваться в результате превращения; избыточный углерод расходуется на образование цементита, в результате чего и получаются механические смеси: эвтектика и эвтектоид.
Сплавы с содержанием углерода до 0,8 % называются доэвтектоидными, а более 0,8 % (до 2,14 %) называются заэвтектоидными; сплав, содержащий 0,8 % углерода – эвтектоидным.
Предельная растворимость углерода в 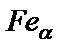 составляет 0,025 % при температуре 727 °С (точка Р).
составляет 0,025 % при температуре 727 °С (точка Р).
При дальнейшем охлаждении растворимость углерода уменьшается по линии PQ до 0,006 при комнатной температуре. Избыточный углерод выделяется из феррита ниже температур, соответствующих линии PQ, в виде кристаллов третичного цементита.
У сплавов с содержанием углерода более 2,14 % в результате эвтектоидного превращения ледебурит будет состоять из смеси эвтектоида (перлита) и цементита.
Диаграмма состояния дает возможность дать количественную оценку соотношения фаз в процессе кристаллизации любого сплава, описываемого диаграммой. Для этого применяют правило отрезков.
Дата добавления: 2016-03-22; просмотров: 1372;
