Задание 7 контрольной работы
Напишите уравнение электролитической диссоциации раствора слабой кислоты и найдите концентрации ионов Н+ и кислотного остатка в моль/л в растворе, если известны константа диссоциации Кдисс. И нормальность Сн
| Вариант | Формула кислоты | Название кислоты | Сн,моль/л | Кдисс |
| HCOOH | Муравьиная | 0,005 | 1,8 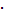 10-4 10-4
| |
| CH3COOH | Уксусная | 0,005 | 1,74 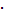 10-5 10-5
| |
| HNO2 | Азотистая | 0,05 | 5,1 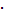 10-4 10-4
| |
| C6H6COOH | Бензойная | 0,05 | 6,6 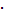 10-5 10-5
| |
| HIO4 | Иодная | 0,005 | 2,8 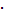 10-2 10-2
| |
| HIO3 | Иодноватая | 0,001 | 1,6 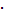 10-1 10-1
| |
| HF | Плавиковая | 0,01 | 6,8 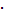 10-4 10-4
| |
| HCN | Синильная | 0,1 | 6,2 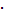 10-10 10-10
| |
| HBrO | Бромноватистая | 0,1 | 2,5 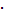 10-9 10-9
| |
| C2H5COOH | Пропионовая | 0,01 | 1,35 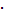 10-5 10-5
| |
| HCNS | Роданисто-водородная | 0,001 | 1,4 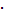 10-1 10-1
| |
| C6H4(OH)COOH | Салициловая | 0,001 | 1,1 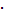 10-3 10-3
| |
| HClO2 | Хлористая | 0,001 | 1,1 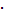 10-2 10-2
| |
| HClO | Хлорноватистая | 0,05 | 5,0 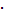 10-8 10-8
| |
| HCNO | Циановая | 0,01 | 3,5 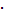 10-4 10-4
| |
| HCOOH | Муравьиная | 0,02 | 1,8 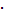 10-4 10-4
| |
| CH3COOH | Уксусная | 0,01 | 1,74 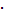 10-5 10-5
| |
| HNO2 | Азотистая | 0,01 | 5,1 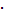 10-4 10-4
| |
| C6H5COOH | Бензойная | 0,01 | 6,6 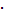 10-5 10-5
| |
| HIO4 | Йодная | 1,0 | 2,8 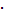 10-2 10-2
| |
| HIO3 | Йодноватая | 2,0 | 1,6 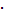 10-1 10-1
| |
| HF | Плавиковая | 0,05 | 6,8 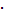 10-4 10-4
| |
| HCN | Синильная | 0,5 | 6,2 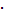 10-10 10-10
| |
| HBrO | Бромноватистая | 0,5 | 2,5 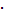 10-9 10-9
| |
| C2H5COOH | Пропионовая | 0,05 | 1,35 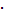 10-5 10-5
| |
| HNO2 | Азотистая | 2,0 | 5,1 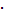 10-4 10-4
| |
| C6H4(OH)COOH | Салициловая | 1,0 | 1,1 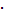 10-3 10-3
| |
| HClO2 | Хлористая | 1,0 | 1,1 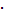 10-2 10-2
| |
| HClO | Хлорноватистая | 0,1 | 5,0  10-5 10-5
| |
| HCNO | Циановая | 0,05 | 3,5  10-4 10-4
|
Дата добавления: 2016-03-15; просмотров: 749;
