Распространенность химических элементов
Строение и устойчивость атомного ядра
Полной теории структуры атомных ядер до сих пор нет. Наиболее распространена модель оболочечного строения ядра атома. Предполагают, что протоны и нейтроны, независимо друг от друга, заполняют ядерные слои и оболочки.
В настоящее время известно около 300 устойчивых и более 1000 радиоактивных ядер. Ядра, содержащие 2, 8, 14, 20, 28, 50, 82 протона или нейтрона и 126, 152 нейтрона особенно стабильны. Предполагается, что эти «магические числа» нуклонов соответствуют завершенным ядерным слоям. Элементы с числом протонов в ядре равным одному из магических чисел имеет большее число изотопов, чем соседние с ним элементы. Ядра с числом нуклонов, стоящим непосредственно за «магическим числом», особенно легко разрушаются.
Изотопы – это атомы одного и того же химического элемента, которые различаются количеством нейтронов в ядре, а следовательно, и массой. Известно более 110 химических элементов.
Радиоактивность
Первым шагом в научном решении проблемы превращения элементов было открытие в 1896 г. Беккерелем естественной радиоактивности урана. Два года спустя Мария и Пьер Кюри обнаружили радиоактивность у тория, а затем открыли 2 новых радиоактивных элемента – полоний и радий. Эти открытия доказали, что химические элементы не являются вечными и неизменными, а могут превращаться друг в друга.
Радиоактивность – это способность некоторых атомных ядер самопроизвольно превращаться в другие ядра с испусканием различных видов радиоактивных излучений и элементарных частиц.
Известны три основных вида радиоактивного излучения:
- альфа-излучение – поток ядер гелия;
- бета-излучение – поток быстрых электронов;
- гамма-излучение – коротковолновое электромагнитное излучение с очень малой длиной волны (менее 10-10 м), что обуславливает его чрезвычайно высокую проникающую способность.
Продолжительность жизни атомов определяется строением их ядер и характеризуется периодом полураспада, то есть временем, в течение которого распадается половина всех ядер данного элемента. Период полураспада может быть от 10-3 с до 1010 лет, но для большинства изотопов – 30 с - 10 суток.
На Земле встретить радиоактивный элемент можно только в 3 случаях:
- он «пережил» 4,3 млрд. лет со времени образования планеты Земля (торий, уран);
- его запасы постоянно пополняются за счет естественных процессов;
- он получен искусственно в результате деятельности человека (ускорители частиц, атомные реактора и пр.).
Основные типы радиоактивных превращений:
1) наиболее часто происходит β-распад ядер – ядро испускает электрон (β-частицу) за счет превращения одного нейтрона ядра в протон.
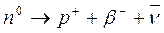 .
.
Часть энергии, выделяющейся при β-распаде, уносит с собой антинейтрино 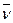 .
.
Образуется изотоп элемента с порядковым номером на единицу большим, чем у исходного, и с той же атомной массой.
 .
.
2) для ядер с недостатком нейтронов, то есть для самых легких элементов, характерен позитронный распад – распад с выделение позитрона (античастицы электрона).
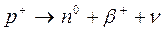 .
.
При этом образуется изотоп элемента на единицу меньшим, чем у исходного, и с той же атомной массой.
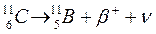 .
.
3) к такому же изменению ядра, как при позитронном распаде, приводит электронный захват – электрон, находящийся близко к ядру, захватывается ядром
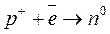 .
.
 .
.
4) наибольшие изменения исходного ядра наблюдаются при α-распаде. Выделение ядром α-частицы (ядра гелия) приводит к изменению заряда ядра на 2, а массы на 4. Этот распад наиболее характерен для тяжелых элементов.
 .
.
Для тяжелых элементов наряду с естественной радиоактивностью возможно самопроизвольное (спонтанное) деление ядра на две части. Впервые это явление было открыто для ядер урана в 1940 г. Флёровым и Петржаком.
Все элементы, находящиеся в Периодической системе Д.И. Менделеева после висмута (№ 83), радиоактивны. Среди последних существуют только 3 ядра, продолжительность жизни которых настолько велика, что они сохранились на Земле: торий-232, уран-235 и уран-238. Они являются родоначальниками цепочек последовательных радиоактивных превращений, образуя «семейства», в которые входят большинство встречающихся в природе радиоактивных элементов, обладающих меньшей продолжительностью жизни. Цепочки распада завершаются образованием стабильных изотопов свинца и гелия.
Анализ руд и минералов на содержание урана-238 или торий-232 и соответствующих изотопов свинца позволяет с достаточной точностью определять возраст геологических объектов.
Кроме радиоактивного распада превращения элементов происходят при разнообразных ядерных реакциях. Первое искусственное ядерное превращение осуществил в 1919 г. Резерфорд: ядро-мишень бомбардируется частицами (например, α-частицами), при этом образуется промежуточное короткоживущее составное ядро, которое затем испускает элементарную частицу или легкое ядро и в превращается в новый изотоп.
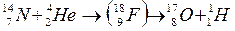 или.
или. 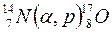
Важным видом ядреных реакций являются термоядерные реакции. Это реакции слияния легких атомных ядер в более сложные.
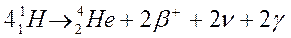 .
.
Термоядерные реакции способны протекать только при очень высоких температурах 107 К (ядра звезд, атомный взрыв, мощный газовый разряд). Практически сейчас осуществимы только неуправляемые термоядерные реакции при взрывах ядерных бомб.
Распространенность химических элементов
Среднее относительное содержание химического элемента в доступной нам части Вселенной называется его распространенностью или кларком.
Кларк зависит от вероятности ядерных реакций его образования и относительной устойчивости изотопов элемента. Наиболее распространены во Вселенной водород и гелий. Кларк элемента уменьшается с увеличением заряда его ядра. Более распространены элементы с четным зарядом ядра.
| <== предыдущая лекция | | | следующая лекция ==> |
| Свойства пространства-времени и законы сохранения | | | Доменное производство. |
Дата добавления: 2016-03-05; просмотров: 703;
