ГЛАВА 63. ГЛАВНЫЙ КОМПЛЕКС ГЕНОВ ГИСТОСОВМЕСТИМОСТИ
Чарлз Б. Карпентер (Charles В. Carpenter)
Антигены, обеспечивающие внутривидовые различия особей, обозначаются как аллоантигены, а когда они включаются в процесс отторжения аллогенных тканевых трансплантатов, то приобретают название антигенов тканевой совместимости (гистосовместимости). Эволюция закрепила единичный участок тесно сцепленных генов гистосовместимости, продукты которых на поверхности клеток обеспечивают сильный барьер при аллотрансплантации. Термины «major histocompatibility antigens» (главные антигены гистосовместимости) и «major histocompatibility gene complex» (MHC) (главный генный комплекс гистосовместимости) относятся соответственно к продуктам генов и генам этого хромосомного участка. Многочисленные минорные антигены гистосовместимости, наоборот, кодируются множественными участками генома. Им соответствуют более слабые аллоантигенные различия молекул, выполняющих разнообразные функции. Структуры, несущие детерминанты MHC, играют значительную роль в иммунитете и самораспознавании в процессе дифференцировки клеток и тканей. Информация о МНС-контроле иммунного ответа получена в опытах на животных, когда гены иммунного ответа были картированы внутри MHC—у мышей (Н-2), крыс (RT1), морских свинок (GPLA). У человека MHC назван HLA. Отдельным буквам аббревиатуры HLA придается различное значение, и с международного согласия HLA служит для обозначения человеческого МНС-комплекса.
Относительно MHC можно сделать несколько обобщений. Во-первых, в малом участке (менее 2 сантиморган) MHC кодируется три класса генных продуктов. Молекулы класса I, экспрессируемые практически всеми клетками, содержат одну тяжелую и одну легкую полипептидную цепи и являются продуктами трех редуплицированных локусов—HLA-A, HLA-B и HLA-C. Молекулы класса II, экспрессия которых ограничивается В-лимфоцитами, моноцитами и активированными Т-лимфоцитами, содержат две полипептидные цепи (a и b) неравной величины и являются продуктами нескольких тесно сцепленных генов, в сумме обозначаемых как зона HLA-D. Молекулы класса III представляют собой компоненты комплемента С4, С2 и Bf. Во-вторых, молекулы классов I и II образуют комплекс с псевдоантигеном, или антиген гистосовместимости и псевдоантиген слитно распознаются Т-лимфоцитами, имеющими соответствующий рецептор для антигена. Распознавание своего и несвоего при запуске и в эффекторной фазе иммунного ответа непосредственно направляется молекулами I и II классов. В-третьих, четких ограничений межклеточных взаимодействий, в которых участвуют супрессорные Т-лимфоциты, у человека не выявлено, но роль генов HLA достаточно важна для некоторых проявлений супрессорной Т-клеточной активности. В-четвертых, в МНС-регионе локализуются гены ферментных систем, не имеющих непосредственного отношения к иммунитету, но важных для роста и развития скелета. Известные локусы HLA на коротком плече 6-й хромосомы представлены на рис. 63-1.
Локусы системы HLA. Антигены класса I. HLA-антигены I класса определяются серологически с помощью человеческих сывороток, главным образом от многорожавших женщин, и в меньшей степени с помощью моноклональных антител. Антигены I класса присутствуют с разной плотностью во многих тканях организма, включая В-клетки, Т-клетки, тромбоциты, но не на зрелых эритроцитах. Количество серологически выявляемых специфичностей велико, и система HLA является наиболее полиморфной из известных генетических систем человека. Внутри HLA-комплекса для серологически выявимых HLA антигенов I класса четко определяются три локуса. Каждый антиген 1 класса содержит b2-микроглобулиновую субъединицу (мол. масса 11500) и тяжелую цепь (мол. масса 44000), несущую антигенную специфичность (рис. 63-2). Существует 70 четко определенных А- и В-специфичностей и восемь специфичностей локуса С. Обозначение HLA обычно присутствует в наименовании антигенов главного комплекса гистосовместимости, но может не употребляться, когда позволяет контекст. Антигены, неокончательно классифицированные ВОЗ, имеют в обозначении букву w после названия локуса. Номер, следующий за обозначением локуса, служит собственным названием антигена. HLA-антигены населения Африки, Азии и Океании в настоящее время недостаточно четко определены, хотя они включают часть общих антигенов, свойственных лицам западноевропейского происхождения. Распределение HLA-антигенов различно в разных расовых группах, и они могут быть использованы как антропологические маркеры в изучении заболеваний и миграционных процессов.
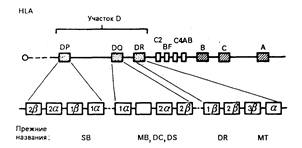
Рис. 63-1. Схематическое изображение хромосомы 6.
Показана локализация зоны HLA в регионе 21 короткого плеча. Локусы HLA-A, HLA-B и HLA-C кодируют тяжелые цепи класса I (44000), тогда как b2-микроглобулиновая легкая цепь (11500) молекул класса I кодируется геном хромосомы 15. Зона HLA-D (класс II) расположена центромерно по отношению к локусам А, В и С с тесно сцепленными генами компонентов комплемента С4А, С4В, Bf и С2 на участке B-D. Порядок расположения генов комплемента не установлен. Каждая молекула класса II D-региона образована a- и b-цепями. Они присутствуют на клеточной поверхности в разных участках (DP, DQ и DR). Цифра, предшествующая знакам a и b, означает, что существуют различные гены для цепей данного типа, например, для DR существует три гена b-цепей, так что экспрессируемые молекулы могут быть 1ba, 2ba или 3ba. Антигены DRw52(MT2) и DRw53(MT3) находятся на 2b-цепи, тогда как DR — на lb-цепи. DR неполиморфен, а молекулы DQ-антигенов полиморфны как по a-, так и по b-цепям (2a2b). Другие типы DQ (1a1b) имеют ограниченный полиморфизм. Полиморфизм DP связан с b-цепями. Общая протяженность HLA-региона— около 3 сМ.
Поскольку хромосомы парны, каждый индивид имеет до шести серологически определимых антигенов HLA-A, HLA-B и HLA-C, по три от каждого из родителей. Каждый из этих наборов обозначается как гаплотип, и в соответствии с простым менделевским наследованием четвертая часть потомства имеет идентичные гаплотипы, половина — часть общих гаплотипов и оставшаяся четверть — полностью несовместима (рис. 63-3). Значение роли этого генного комплекса в трансплантационном ответе подтверждается тем, что подбор по гаплотипу пар донор — реципиент среди потомства одного поколения обеспечивает наилучшие результаты при трансплантации почек — около 85—90% длительного выживания (см. гл. 221).
Антигены класса II. Зона HLA-D примыкает к локусам класса I на коротком плече 6-й хромосомы (см. рис. 63-1). Этот регион кодирует серию молекул класса II, каждая из которых содержит a-цепь (мол, масса 29000) и b-цепь (мол. масса 34000) (см. рис. 63-2). Несовместимость по этому региону, особенно по антигенам DR, определяет пролиферативную реакцию лимфоцитов in vitro. Смешанная лимфоцитарная реакция (MLR) оценивается по уровню пролиферации в смешанной культуре лимфоцитов (MLC) и может быть положительной даже при идентичности по антигенам HLA-A, HLA-B и HLA-C (см. рис. 63-3). Антигены HLA-D определяются с помощью стандартных стимулирующих лимфоцитов, гомозиготных по HLA-D и инактивированных рентгеновскими лучами или митомицином С с целью придания реакции однонаправленности. Существует 19 таких антигенов (HLA-Dwl-19), обнаруженных с использованием гомозиготных типирующих клеток.
Попытки определения HLA-D серологическими методами сначала позволили обнаружить серию D-связанных (DR) антигенов, экспрессированных на молекулах класса II В-лимфоцнтов, моноцитов и активированных Т-лимфоцитов. Затем были описаны и другие тесно сцепленные антигенные системы, которые получили различные наименования (MB, MT, DC, SB). Идентичность отдельных групп молекул класса II сейчас установлена, и гены соответствующих a- и b-цепей выделены и секвенированы. Генная карта класса II, представленная на рис. 63-1, отражает минимальное число генов и молекулярных участков. Хотя молекула масса II может содержать DRa из гаплотипа одного из родителей, a DRb— другого (транскомплементация), комбинаторика вне каждого из участков DP, DQ, DR редка, если вообще возможна. Молекулы DR и в определенной степени DQ могут служить стимулами для первичной MLR. Вторичная MLR определяется как тест с примированными лимфоцитами (PLT) и дает возможность получить результат через 24—36 ч вместо 6—7 дней для первичной реакции. Аллоантигены DP были открыты благодаря их способности вызывать стимуляцию PLT, хотя они не дают первичной MLR. Хотя В-лимфоциты и активированные Т-лимфоциты экспрессируют все три набора молекул класса II, антигены DQ не экспрессируются на 60-90% DP- и DR-позитивных моноцитов.
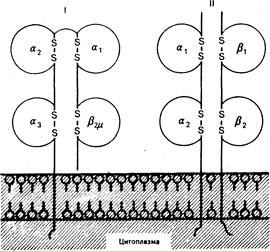
Рис. 63-2. Схематическое изображение молекул клеточной поверхности классов I и II.
Молекулы класса I состоят из двух полипептидных цепей. Тяжелая цепь с мол. массой 44 000 проходит сквозь плазматическую мембрану; ее наружный участок состоит из трех доменов (a1, a2 и a3), формируемых дисульфидными связями. Легкая цепь с мол. массой 11500 (b2-микроглобулин, b2мю) кодируется хромосомой 15 и нековалентно связана с тяжелой цепью. Аминокислотная гомология между молекулами I класса составляет 80—85%, снижаясь до 50% в участках a1 и a2, которые, вероятно, соответствуют участкам аллоантигенного полиморфизма. Молекулы класса II образованы двумя нековалентно связанными полипсптидными цепями, a-цепь с мол. массой 34000 и b-цепь с мол массой 29000. Каждая цепь содержит два домена, сформированных дисульфидными связями (из С. Б. Carpenter, E. L. Milford, Renal Transplantation: Immunobiology in the Kidnev/Eds. B. Brenner, F. Rector, New York: Samiders, 1985).

Рис. 63-3. HLA-зона хромосомы 6: наследование HLA-гаплотипов. Каждый хромосомный сегмент сцепленных генов обозначается как гаплотип, и каждый индивид наследует по одному гаплотипу от каждого родителя. На диаграмме представлены антигены А, В и С гаплотипов а и b для данного гипотетического индивида; ниже раскрыты обозначения гаплотипов в соответствии с текстом. Если мужчина с гаплотипом ab женится на женщине с гаплотипом cd, потомки могут быть только четырех типов (с точки зрения HLA). Если в мейозе у одного из родителей происходит рекомбинация (отмечена прерывистыми линиями), то это приводит к формированию измененного гап-лотнпа. Частота измененных гаплотипов у детей служит мерой расстояний на генетической карге (1% частота рекомбинаций== 1 сМ; см. рис. 63-1) (из Г.. В. Carpenter. Kidney International, Г)78. 14. 283).
Молекулярная генетика. Каждая полипептидная цепь молекул классов I и II содержит несколько полиморфных участков в дополнение к «частной» антигенной детерминанте, определяемой с помощью антисывороток. В тесте клеточно-опосредованного лимфолиза (CML) определяется специфичность киллерных Т-клеток (Тк), которые возникают в процессе пролиферации при MLR, путем тестирования на клетках-мишенях от доноров, не служивших источником стимулирующих клеток для MLR. Антигенные системы, определяемые этим методом, обнаруживают тесную, но неполную корреляцию с «частными» антигенами класса 1. Клонирование циготоксических клеток позволило обнаружить набор полиморфных детерминант-мишеней на молекулах HLA, некоторые из которых невозможно выявить с помощью аллоантисывороток и моноклональных антител, полученных иммунизацией мышей человеческими клетками. Некоторые из этих реагентов могут быть использованы для идентификации «частных» детерминант HLA, в то время как другие направлены к более «общим» (иногда называемым супертипируемыми) детерминантам. Одна такая система «общих» HLA-B антигенов имеет два аллеля, Bw4 и Bw6. Большинство «частных» HLA-B связаны или с Bw4, или с Bw6. Другие системы сопряжены с подгруппами HLA антигенов. Например, HLA-B-позитивные тяжелые цепи содержат дополнительные участки, общие для В7, В27, Bw22 и В40 или для В5, В15, В18 и Bw35. Существуют и другие типы перекрывающихся антигенных детерминант, о чем свидетельствует реакция моноклональных антител с участком, общим для тяжелых цепей HLA-A и HLA-B. Изучение аминокислотной последовательности и псптидных карт некоторых молекул HLA показало, что гипервариабельные участки антигенов класса I сосредоточены в наружном a1-домене (см. рис. 63-2) и прилегающем участке a2-домена. Вариабельные последовательности молекул класса II различны для разных локусов. Замечательно, что a3-домен класса I, a2-домен класса II и b2-домен, а также часть мембранной молекулы Т8 (Leu 2), участвующей в межклеточных взаимодействиях (см. гл. 62), обнаруживают значительную гомологию последовательности аминокислот с константными зонами иммуноглобулинов. Это подтверждает гипотезу об эволюционном формировании семейства генных продуктов, которые несут функции иммунологичсского распознавания. При исследовании геномной ДНК HLA для молекул классов I и II были обнаружены типичные экзон-интронные последовательности, причем экзоны были идентифицированы для сигнальных пептидов (5') каждого из доменов, трансмембранного гидрофобного сегмента и цитоплазматического сегмента (З'). Имеются пробы кДНК для большинства цепей HLA, а применение ферментативных гидролизатов для оценки состояния полиморфизма рестрикционных фрагментов по длине (ПДРФ), позволило получить данные, которые коррелируют с результатами изучения молекул класса 11 серологическими методами в MLR. Однако многочисленность (20—30) генов класса 1 делает оценку полиморфизма по ПДРФ затруднительной. Многие из этих генов не экспрессируются (псевдогены), хотя некоторые могут соответствовать дополнительным локусам класса I, которые экспрессируются только на активированных Т-клетках; функции их неизвестны. Разработка специфических проб на локусы HLA-A и HLA-B поможет разобраться в этой достаточно сложной проблеме.
Комплемент (класс III). Структурные гены трех компонентов комплемента—С4, С2 и Bf—присутствуют в зоне HLA-B-D (см. рис. 63-1). Это два локуса С4, кодирующие С4А и С4В, первоначально описанные как эритроцитарные антигены Rodgers и Chido соответственно. Эти антигены оказались в действительности абсорбированными из плазмы молекулами С4. Другие компоненты комплемента не имеют тесного сцепления с HLA. Между генами С2, Bf и С4 кроссинговера не описано. Все они кодируются участком между HLA-B и HLA-DR длиной около 100ко. Существуют два аллеля С2, четыре Bf, семь С4А и три С4В, кроме того, в каждом локусе имеются молчащие аллели QO. Исключительная полиморфность гистотипов комплемента (комплотипы) делает эту систему пригодной для генетических исследований.
Таблица 63-1. Наиболее распространенные гаплотины HLA
| HLA-B | HLA-DR | BF | С2 | С4А | С4В |
| S | С | QO | |||
| S | С | ||||
| S | С | ||||
| F | С |
В табл. 63-1 представлены четыре наиболее широко распространенных гаплотипа, обнаруженных у лиц западноевропейского происхождения. Результаты MLR у людей, не состоящих в родстве, отобранных по признаку совместимости по этим гаплотипам, отрицательны, в то же время реакция обычно имеет место, если неродственные индивиды подобраны только на совместимость по HLA-DR и DQ. Такие идентичные распространенные гаплотипы, возможно, в неизменном виде происходят от единого предка.
Другие гены 6-й хромосомы. Недостаточность стероид 21-гидроксилазы, аутосомно-рецессивный признак, вызывает синдром врожденной гиперплазии надпочечников (гл. 325 и 333). Ген для этого фермента локализуется на участке HLA-B-D. Ген 21-гидроксилазы, прилегающий к гену С4А, делетирован у лиц, страдающих упомянутым синдромом, вместе с С4А (C4AQO), и ген HLA-B может трансформироваться с конверсией В 13 в редкий Bw47, обнаруживаемый только в измененных гаплотипах. В отличие от поздно проявляющегося дефицита 21-гидроксилазы, сцепленного с HLA, врожденная гиперплазия надпочечников, связанная с дефицитом 21b-гидроксилазы, не сцеплена с HLA. В нескольких семейных исследованиях показано, что идиопатический гемохроматоз, аутосомно-рецессивное заболевание, сцеплено с HLA (см. гл. 310). Хотя патогенез расстройств всасывания железа в желудочно-кишечном тракте неизвестен, установлено, что гены, модулирующие этот процесс, находятся вблизи участка HLA-A.
| Таблица 63-2. Сцепление генетических дефектов | с HLA | |
| Дефекты | Локализация | Обнаруживаемые |
| генов | гаплотипы | |
| Дефицит С2 | HLA-B-D | Aw25, B18, BfS, DR2 |
| Дефицит 21-ОН | HLA-B-D | A3, Bw47, BfF, DR7 |
| Дефицит 21-ОН (позднее проявление) | HLA-B-D | В14, BfS, DR1 |
| Идиопатический гемохроматоз | HLA-A | A3, B14 |
| Болезнь Педжета | HLA-A-D | |
| Спинно-мозжечковая атаксия | HLA-A-D | |
| Болезнь Ходжкина | HLA-A-D |

Рис. 63-4. Схема относительной роли HLA-A, HLA-B, HLA-C и HLA-D антигенов в инициации аллоиммунного ответа и в образовании эффекторных клеток и антител.
Два главных класса Т-лимфоцитов распознают антигены: Тк — предшественники цитотоксических «киллерных» клеток и Тх—хелперные клетки, способствующие развитию цитотоксического ответа. Тх также обеспечивают помощь В-лимфоцитам при развитии «зрелого» IgG-ответа. Важно отметить, что Тк обычно распознают антигены класса I, тогда как сигнал для Тх создает преимущественно HLA-D, который тесно связан с антигенами класса II (из С. В. Carpenter.— Kidney International, 1978, 14, 283).
Гены иммунного ответа. При изучении in vitro ответа на синтетические полипептидные антигены, гемоцианин, коллаген, столбнячный токсоид выявлено, что зона HLA-D аналогична региону Н-2. I у мыши. Презентация антигенных фрагментов на поверхности макрофагов или других клеток, несущих молекулы II класса, требует сопряженного распознавания комплекса «молекула II класса + антиген» Т-лимфоцитами, несущими соответствующий рецептор (ы) (см. гл. 62). Стержнем этой гипотезы «свое-)-Х» или «измененное свое» состоит в том, что Т-зависимый иммунный ответ, действие Т-хелперов/индукторов (Тх) осуществляется только в том случае, если будут синтезированы соответствующие детерминанты класса II. Гены последних и есть Ir-гены. Поскольку аллогенные детерминанты класса И распознаются как уже измененные, аллогенная MLP представляет собой модель иммунной системы, в которой присутствие псевдоантигена необязательно (рис. 63-4). Эффекторные фазы иммунитета требуют распознавания псевдоантигена в комплексе с собственными структурами. Последние у человека, как и у мыши, представляют собой молекулы антигенов гистосовместимости I класса. Человеческие клеточные линии, инфицированные вирусом гриппа, лизируются иммунными цитотоксическими Т-лимфоцитами (Тк) только в том случае, если реагирующие клетки и клетки-мишени идентичны по локусам HLA-A и HLA-B. Аллогенная MLR служит моделью и для формирования цитотоксических Т-лимфоцитов, рестриктированных по классу I (см. рис. 63-4). Детали рестрикции по различным молекулам классов I и II и эпитопам могут быть вычленены при использовании примированных клеток, подвергшихся размножению и клонированию. Например, на уровне антигенпрезентирующих клеток данный Тх-клон распознает антигенный фрагмент, комплексированный со специфическим участком молекулы класса II, с помощью рецептора Ti. Рестриктирующими элементами.для некоторых микробных антигенов являются аллели DR и Dw.
Супрессия иммунного ответа (или, низкий уровень отвечаемости) к пыльце кедра, антигенам стрептококков и шистосом доминантна и сцеплена с HLA, что свидетельствует о существовании генов иммунной супрессии (Is). Показано также наличие специфических аллельных ассоциаций HLA с уровнем иммунного ответа, например, для антигена клещевины Ra5 — с DR2 и для коллагена — с DR4.
Ассоциации с болезнями. Если главный комплекс гистосовместимости выполняет важную биологическую функцию, то какова эта функция? Одна из гипотез состоит в том что он играет роль в иммунном надзоре за неопластическими клетками, появляющимися в течение жизни индивида. Велико значение этой системы при беременности, поскольку между матерью и плодом всегда существует тканевая несовместимость. Высокая степень полиморфизма может также способствовать выживаемости видов в противостоянии огромному числу микробных агентов присутствующих в окружающей среде. Толерантность к «своему» (аутотолерантность) может перекрестие распространяться на микробные антигены, следствием которой будет высокая восприимчивость, приводящая к возникновению смертельных инфекций, в то время как полиморфизм по системе HLA способствует тому что часть популяции распознает опасные агенты как чужеродные и включает адекватную ответную реакцию. Эти гипотезы связывают роль HLA с преимуществами, благодаря которым система выживает в условиях давления отбора Каждая из этих гипотез имеет определенные подтверждения.
Важным свидетельством роли комплекса HLA в иммунобиологии послужило обнаружение положительной ассоциации некоторых патологических процессов с антигенами HLA. Изучение этих ассоциаций было стимулировано открытием генов иммунного ответа, сцепленных с Н-2-комплексом, у мышеи. В табл. 63-3 суммированы наиболее значимые ассоциации HLA и болезней.
Установлено что частота встречаемости HLA-B27 повышается при некоторых ревматических заболеваниях, особенно при анкилозирующем спондилите, заболевании явно семейного характера. Антиген В27 имеется лишь у 7% лиц западноевропейского происхождения, но его обнаруживают у 80-90% больных анкилозирующим спондилитом. В пересчете на относительный риск это означает, что этот антиген ответствен за восприимчивость к развитию анкилозирующего спондилита, которая в 87 раз выше у его носителей, чем в общей популяции. Аналогично показана высокая степень ассоциации с антигеном В27 острого переднего увеита, синдрома Рейтера и реактивных артритов по крайней мере при трех бактериальных инфекциях (иерсиниозе, сальмонеллезе и гонорее). Хотя обычная форма ювенильного ревматоидного артрита также ассоциирована с В27, тип заболевания со слабо выраженным суставным синдромом и иритом связан с В27. При псориатическом артрите центрального типа чаще встречается В27, тогда как Bw38 ассоциирован как с центральным, так и с периферическим типами. Псориаз ассоциирован с Cw6. У больных с дегенеративным артритом или подагрой не обнаруживается каких-либо изменений в частоте встречаемости антигенов.
Большинство других ассоциаций с болезнями свойственно антигенам HLA-D-зоны Например, глютенчувствительная энтеропатия у детей и взрослых ассоциирована с антигеном DR3 (относительный риск 21) Действительный процент больных с данным антигеном варьирует от 63 до 96% в сравнении с 22—27% в контроле. Тот же антиген чаще обнаруживается у больных с активным хроническим гепатитом и герпетиформным дерматитом, страдающих в то же время и глютенчувствительной энтеропатией. Ювенильный инсулинзависимыи сахарный диабет (тип I) ассоциирован с DR3 и DR4 и отрицательно ассоциирован с DR2 У 17—25% больных диабетом I типа обнаружен редкий аллель Bf (М). Диабет с началом во взрослом периоде жизни (типа II) не имеет ассоциации с HLA. Гипертиреоидизм в США ассоциирован с В8 и Dw3, в то время как в японской популяции — с Bw35. Более широкое обследование здоровых и больных представителей различных рас поможет прояснить вопрос об универсальных HLA-маркерах. Например, антиген В27, редкий у здоровых лиц японской национальности, обычен у больных с анкилозирующим спондилитом. Точно так же DR4 — маркер тля диабета I типа у представителей всех рас. Иногда HLA-маркер явно ассоциирован только с частью симптомов внутри синдрома. Например, миастения значительно сильнее ассоциирована с антигенами В8 и DR3 у больных без тимомы, а рассеянный склероз — с антигеном DR2 у лиц с быстро прогрессирующим течением болезни. Синдром Гудпасчера, связанный с аутоиммунным поражением клубочковых базальных мембран, идиопатический мембранозный гломерулонефрит, отражающий аутоиммунные процессы с образованием антител к антигенам клубочков, а также мембранозный нефрит, индуцированный золотом, в значительной степени ассоциированы с HLA-DR.
Таблица 63-3. Заболевания, ассоциированные с HLA-антигенами
| Заболевания | Наиболее тесно ассоциированные антигены | Относительный риск' | ||
| Ревматоидные | ||||
| Анкилозирующий спондилит | В27 | 87,0 | ||
| Синдром Рейтера | В27 | 37,0 | ||
| Острый передний увеит | В27 | 10,3 | ||
| Реактивный артрит (Yersinia, Salmonella, Gonococcus) | В27 | 18,0 | ||
| Псориатический артрит (центральный) | В27 | 10,7 | ||
| Bw38 | 9,1 | |||
| Псориатический артрит (периферический) | В27 | 2,0 | ||
| Bw38 | 6,5 | |||
| Ювенильный ревматоидный артрит | В27 | 4,5 | ||
| DRw8 | 3,6 | |||
| Ювенильный артрит со слабо выраженным суставным синдромом | DR5 | 5,2 | ||
| Ревматоидный артрит | Dw4/DR4 | 6,0 | ||
| Синдром Шегрена | Dw3 | 9,7 | ||
| Системная красная волчанка | DR3 | 5,8 | ||
| Системная красная волчанка (в результате | DR4 | 5,6 | ||
| приема апрессина) | ||||
| Желудочно-кишечные | ||||
| Глютенчувствительная энтеропатия | DR3 | 21,0 | ||
| Хронический активный гепатит | DR3 | 6,8 | ||
| Язвенный колит | В5 | 3,8 | ||
| Гематологические | ||||
| Идиопатический гемохроматоз | A3 | 8,2 | ||
| В14 | 26,7 | |||
| A3, В 14 | 90,0 | |||
| Пернициозная анемия | DR5 | 5,4 | ||
| Кожные | ||||
| Герпетиформный дерматит | Dw3 | 15,4 | ||
| Псориаз вульгарный | Cw6 | 4,8 | ||
| Псориаз вульгарный (в японской популяции) | Cw6 | 10,7 | ||
| Пузырчатка вульгарная (в европейской попу ляции) | DR4 А10 | 14,4 5,9 | ||
| Болезнь Бехчета | В5 | 6,3 | ||
| Эндокринные | ||||
| Сахарный диабет I типа | DR4 | 6,4 | ||
| DR3 | 3,3 | |||
| DR2 | 0,2 | |||
| BfFI | 15,0 | |||
| В8 | 2,7 | |||
| Гипертиреоидизм | Dw3 | 3,7 | ||
| Гинертиреоидизм (в японской популяции) | Bw35 | 3,9 | ||
| Заболевания | Наиболее тесно ассоциированные антигены | Относительный риск' | ||
| Недостаточность надпочечников | Dw3 | 10,5 | ||
| Подострый тиреоидит (de Quervain) | Bw35 | 13,7 | ||
| Тиреоидит Хашимото | DR5 | 3,2 | ||
| Н еврологические | ||||
| Миастения | В8 | 2,7 | ||
| DR3 | 2,5 | |||
| Рассеянный склероз | DR2 | 3,9 | ||
| Маниакально-депрессивное расстройство | Bwl6 | 2,3 | ||
| Шизофрения | А28 | 2,3 | ||
| Почечные | ||||
| Идиопатический мембранозный гломеруло- | DR3 | 12,0 | ||
| Нефрит | ||||
| Болезнь Гудпасчера (анти-GMB) | DR2 | 15,9 | ||
| Болезнь минимальных изменений (стероидный | В12 | 3,5 | ||
| ответ) | ||||
| Полицистозная болезнь почек | В5 | 2,6 | ||
| IgA-нефропатия | DR4 | 4,0 | ||
| Нефропатия, вызванная золотом | DR3 | 14,0 | ||
| Инфекционные | ||||
| Туберкулоидная лепра (в азиатской попу | В8 | 6,8 | ||
| ляции) | ||||
| Полнопаралич | Bwl6 | 4.3 | ||
| Низкий ответ на вирус вакцины | Cw3 | 12,7 | ||
| Иммунодефицитные | ||||
| Дефицит IgA (доноры крови) | DR3 | 13,0 | ||
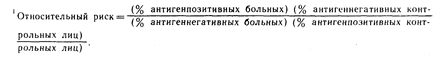
Неравновесное сцепление. Хотя распределение аллелей HLA варьирует в расовых и этнических популяциях, наиболее характерную особенность популяционной генетики антигенов HLA представляет наличие неравновесного сцепления для некоторых антигенов А и В, В и С, В, D и локусов комплемента. Неравновесность сцепления означает, что антигены тесно сцепленных локусов оказываются вместе чаще, чем следует из предположения о случайной ассоциации. Классическим примером неравновесного сцепления является связь антигена локуса AHLA-A1 с антигеном локуса В HLA-B8 у лиц западноевропейского происхождения. Одновременное наличие А1 и В8, рассчитанное на основе частот их генов, должно наблюдаться с частотой 0,17. 0,11, т. е. примерно 0,02. Тогда как наблюдаемая частота их сосуществования составляет 0,08, т. е. в 4 раза больше, чем ожидаемая, и разность между этими величинами составляет 0,06. Последняя величина обозначается дельта (D) и служит мерой неравновесности. Обнаружено неравновесное сцепление и других гаплотипов А- и В-локусов: A3 и В7, А2 и В 12, А29 и В 12, A11 и Bw35, Для некоторых детерминант D-зоны описано неравновесное сцепление с антигенами В-локуса (например, DR3 и В8); а также для антигенов В- и С-локусов. Серологически выявляемые антигены HLA служат маркерами для генов целого гаплотипа внутри семейства и маркерами специфических генов в популяции, но только при наличии неравновесного сцепления.
Значение неравновесного сцепления велико, поскольку такие генные ассоциации могут порождать определенные функции. Давление отбора в процессе эволюции может быть основным фактором в сохранении некоторых генных комбинаций в генотипах. Так, например, существует теория, согласно которой А1 и В8, а также некоторые детерминанты D и других регионов обеспечивают селективное преимущество перед лицом эпидемий таких болезней, как чума или оспа. Однако возможно также, что потомки людей, выживших во время подобных эпидемий, сохраняют восприимчивость к иным болезням, поскольку их уникальный генный комплекс не обеспечивает адекватный ответ на другие факторы окружающей среды. Главная трудность этой гипотезы состоит в допущении, что отбор действует на несколько генов одновременно и обеспечивает тем самым возникновение наблюдаемых значений Л, однако потребность в сложных взаимодействиях между продуктами разных локусов МНС-комплекса — лишь начальное звено для наблюдаемых явлений и селекция может усилить множественное неравновесное сцепление. Сохранение некоторых распространенных гаплотипов, названных выше, поддерживает этот взгляд.
С другой стороны, гипотеза отбора необязательно должна объяснять неравновесное сцепление. Когда популяция, лишенная некоторых антигенов, скрещивается с другой, для которой характерна высокая частота этих антигенов, находящихся в равновесии, D может проявиться через несколько поколений. Например, нарастание D для А1 и В8, обнаруженное в популяциях в направлении с востока на запад, от Индии к Западной Европе, может быть объяснено на основе миграции и ассимиляции населения. В малых группах неравновесность может быть обусловлена совместимостью, эффектом основателей и дрейфом генов. Наконец, некоторые случаи неравновесного сцепления являются результатом неслучайного кроссинговера во время мейоза, так как хромосомные сегменты могут быть в большей или меньшей степени ломкими. Будь то давление отбора или ограничения кроссинговера, неравновесность сцепления может исчезать в течение нескольких поколений. Большое число неслучайных ассоциаций имеется в HLA-генном комплексе и определение их причин может обеспечить проникновение в механизмы, лежащие в основе чувствительности к болезням.
Сцепление и ассоциации. В табл. 63-2 перечислены болезни, служащие примером сцепления с HLA, когда наследственные признаки маркируются в пределах семьи соответствующими гаплотипами. Например, дефицит С2, 21-гидроксилазы, идиопатический гемохроматоз наследуются по рецессивному типу с наличием часгичного дефицита у гетерозигот. Эти генетические нарушения также являются HLA-ассоциированными и обусловливаются избытком некоторых HLA-аллелей у больных людей, не состоящих в родстве. Дефицит С2 обычно сцеплен с гаплотипами HLA-Aw 25, В 18, В55, D/DR2, а при идиопатическом гемохроматозе проявляется как сцепление, так и сильная ассоциация между HLA-A3 и В 14. Высокая степень неравновесного сцепления в этом случае вызвана мутациями у лица, послужившего его источником; кроме того, недостаточен был период времени, необходимый для возвращения пула генов в состояние равновесия. С этой точки зрения HLA-гены — простые маркеры сцепленных генов. С другой стороны, для проявления конкретного нарушения может требоваться взаимодействие со специфическими HLA-аллелями. Последняя гипотеза потребовала бы признания более высокого темпа мутаций с экспрессией дефектных генов, что происходит только при условии сцепления с некоторыми HLA-генами.
Болезнь Педжета и спинно-мозжечковая атаксия являются HLA-сцепленными аутосомно-доминантными наследственными заболеваниями; они обнаруживаются сразу у нескольких членов семьи. Болезнь Ходжкина служит проявлением HLA-сцепленного рецессивного наследственного дефекта. Никаких HLA-ассоциаций не было обнаружено при этих заболеваниях, что свидетельствует в пользу исходной множественности «основоположников» этих болезней с мутациями, связанными с различными аллелями HLA.
Сцепление с HLA без труда определяется, когда доминантность и рецессивность признаков легко разграничить, т. е. когда высока экспрессивность и процесс детерминируется дефектом единичных генов. При большинстве ассоциаций HLA-маркеры отражают факторы риска, вовлекаемые в реализацию и модуляцию иммунного ответа под влиянием множественных генов. Примером полигенного иммунного заболевания является атоническая аллергия, при которой ассоциация с HLA может быть очевидной только у лиц с низким генетически контролируемым (не в связи с HLA) уровнем продукции IgE. Другой пример такого рода — дефицит IgA (см. табл. 63-3), ассоциированный с HLA-DR3.
Клиническое значение системы HLA. Клиническое значение типирования HLA для диагностики ограничивается определением В27 при диагностике анкилозирующего спондилита; тем не менее и в этом случае наблюдается 10% ложноположительных и ложноотрицательных результатов. Изучение HLA имеет ценность также в практике генетических консультаций для раннего определения болезней в семьях с идиопатическим гемохроматозом, врожденной гиперплазией надпочечников, связанной с дефицитом стероидгидроксилазы, в особенности если HLA-типирование осуществляется на клетках, полученных амниоцентезом. Высокая степень полиморфизма в системе HLA делает ее ценным инструментом для тестирования различных клеточных препаратов, в особенности в судебно-медицинской практике. Некоторые болезни, такие как сахарный диабет I типа и другие, для которых показаны HLA-ассоциации, требуют дополнительного изучения роли компонентов системы HLA в патогенезе этих заболеваний.
Дата добавления: 2016-03-05; просмотров: 1394;
