В равных объемах различных газов при одинаковых условиях
(t0С , P) содержится одно и то же число молекул.Законсформулирован итальянским физиком Авогадро в 1811г и имеет ряд следствий.
Следствие 1. В одном моле вещества содержится 6, 02 ∙10 23 молекул.
Значение 6, 02 ∙ 10 23 моль –1 называют числом
Авогадро(NA).
Следствие 2. Один моль любого газа при нормальных условиях (н.у.)
С(273 K), 1,03 . 105 Па) занимает объем 22,4 л/моль.
1 моль О2 (М(О2)=32 г/моль) – содержит 6,02•1023 молекул кислорода, он занимает объем 22,4 л/моль.
1 моль Н2 (М(Н2)=2 г/моль) – содержит 6,02•1023 молекул водорода, он занимает объем 22,4 л/моль.
Задача. Какой объем водорода выделится при травлении 3,25 г Zn соляной кислотой?
Для решения задачи записываем уравнение реакции:
Zn + 2 HCl → ZnCl2 + H2
65 22,4
где 65 – молярная масса цинка; 22,4 – молярный объем водорода.
При травлении 65 г цинка выделится 22,4 л/моль водорода, а при травлении 32,5 г цинка выделится Х л водорода. Найдем объем выделившегося водорода при н.у.
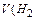 ) = X =
) = X = 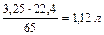
В результате работ немецкого химика Рихтера, английских ученых Дальтона и Волластона (1792 – 1800 г.) были установлены так называемые “соединительные веса” или эквиваленты реагирующих веществ.
Химическим эквивалентом вещества называют такое его количество, которое соединяется полностью с одним моль атомов водорода или замещает такое же количество водорода в его соединениях.
Например, в соединениях НС1, H2О, NH3 эквиваленты хлора, кислорода, азота соответственно равны 1 моль, 1/2 моль, 1/3 моль. За единицу эквивалента принят эквивалент водорода Э (Н) =1 моль атомов). Эквивалент выражают в молях. Кроме понятия эквивалент пользуются понятием молярная масса эквивалента.
Молярная масса эквивалента – это масса одного химического эквивалента вещества МЭ (Н) = 1 г/моль; МЭ (N) = 14∙1/3 = 4,67 г/моль; МЭ (Cl) = 35,45 г/моль; МЭ (S) = 32∙1/2 = 16 г/моль.
Молярная масса эквивалента элемента равна отношению молярной массы элемента (М) к его валентности (В). Например:
S+4O2 , валентность серы равна IV; MЭ (S+4) = M(S)/B = 32/4 = 8 г/моль;
S+6O3, валентность серы равна VI; MЭ (S+6) = M(S)/B = 32/6 = 5,3 г/моль.
Для газообразных веществ удобно пользоваться эквивалентным объемом.
Эквивалентный объем (Vэ) – это объем, занимаемый одним химическим эквивалентом газообразного вещества при нормальных условиях. Эквивалентная масса водорода составляет 1/2 его моля (M(H2)=2 г/моль). Молярный объем водорода равен 22,4 л (н.у.), тогда эквивалентный объем водорода равен 11,2 л/моль. Эквивалентная масса кислорода составляет 1/4 его моля, (M(О2)= 32 г/моль).
Молярный объем кислорода составляет 22,4 л/моль (н.у.), тогда эквивалентный объем кислорода равен 5,6 л/моль.
Дата добавления: 2016-02-27; просмотров: 2770;
