Общие сведения о металлах и сплавах
Все металлы в твердом состоянии имеют кристаллическое строение. В отличие от аморфных веществ, внутреннее строение которых характеризуются ближним порядком, для кристаллического строения присущ дальний порядок, предполагающий геометрически правильное чередование частиц в пространстве. По определению кристаллом является твердое тело, ограниченное плоскими гранями, пересекающимися под определенными углами. Форма кристаллов характеризуется не столько соотношением сторон, сколько двугранными углами между смежными гранями. Различные формы кристаллов можно систематизировать, изучая их геометрию и симметрию. Внешняя форма кристалла является отображением его внутренней структуры, созданной взаимным расположением частиц в пространстве. Внутреннее строение кристаллов отражает кристаллическая решетка - система атомов определенным образом расположенных в пространстве. Первичный элемент кристаллической решетки – элементарная ячейка представляет собой геометрическую фигуру из материальных частиц, определенным образом расположенных в пространстве. Каждая частица (атом, ион), входящая в элементарную ячейку, одновременно принадлежит окружающим ее элементарным ячейкам.
 Существуют разные типы кристаллических решеток, отличающиеся значениями координационного числа и базиса.
Существуют разные типы кристаллических решеток, отличающиеся значениями координационного числа и базиса.
Координационное число показывает, какое количество частиц в кристаллической решетке расположено на кратчайшем расстоянии от данной частицы. Базис соответствует числу частиц, необходимых для построения элементарной ячейки.
 Основные схемы кристаллических решеток металлов приведены на рис. Кубическая объемноцентрирован-ная кристаллическая решетка у натрия, калия, вольфрама, хрома и др. Кристаллическая решетка объемно-центрированная кубическая решетка имеет базис 2 и координационное число 8. Куби-ческая гранецентрированная ре-шетка с базисом 4 и координа-ционным числом 12 характерна для алюминия, меди, серебра, золота, никеля. Гексагональную плотноупакованную решетку образуют цинк, магний, берилий и др. (рис. 1, в). Металлические кристаллы отличаются от остальных кристаллов высокой пластичностью, электрической проводимостью и теплопроводностью, что обусловлено наличием металлической связи между атомами металлов. Металлическая связь образуется за счет перекрытия внешних орбиталей атомов металлов. Электроны переходят в состояние проводимости и могут принадлежать всем атомам кристалла. Мигрирующие обобщенные электроны образуют ненаправленную связь между атомами в кристаллической решетке металлов. Особенностью кристаллических решеток металлов являются большие координационные числа (8…12), свидетельствующие о высокой плотности упаковки атомов.
Основные схемы кристаллических решеток металлов приведены на рис. Кубическая объемноцентрирован-ная кристаллическая решетка у натрия, калия, вольфрама, хрома и др. Кристаллическая решетка объемно-центрированная кубическая решетка имеет базис 2 и координационное число 8. Куби-ческая гранецентрированная ре-шетка с базисом 4 и координа-ционным числом 12 характерна для алюминия, меди, серебра, золота, никеля. Гексагональную плотноупакованную решетку образуют цинк, магний, берилий и др. (рис. 1, в). Металлические кристаллы отличаются от остальных кристаллов высокой пластичностью, электрической проводимостью и теплопроводностью, что обусловлено наличием металлической связи между атомами металлов. Металлическая связь образуется за счет перекрытия внешних орбиталей атомов металлов. Электроны переходят в состояние проводимости и могут принадлежать всем атомам кристалла. Мигрирующие обобщенные электроны образуют ненаправленную связь между атомами в кристаллической решетке металлов. Особенностью кристаллических решеток металлов являются большие координационные числа (8…12), свидетельствующие о высокой плотности упаковки атомов.
Некоторые металлы обладают полиморфизмом: в различных условиях они могут образовывать кристаллы различной формы. Так, например, железо при остывании из расплава испытывает ряд поли-морфных превращений. В интервале температур от 1539 °С до 1392 °С железо существует в виде высокотемпературной δ-модификации (Fеδ) с кристаллической решеткой в виде объемно-центрированного куба. При температуре 1392 °С происходит перекристаллизация железа. Оно переходит в модификацию Fеγ, приобретая гранецентрированную кубическую решетку. При температуре ниже 911 °С Fеγ вновь испытывает полиморфное превращение переходя в Fе 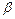 , с объемно- центрированной кубической кристаллической решеткой (ОЦК). При температуре ниже 768 °С Fе
, с объемно- центрированной кубической кристаллической решеткой (ОЦК). При температуре ниже 768 °С Fе 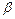 переходит в Fеα. При этом изменяются параметры кристаллической решетки ОЦК и железо начинает проявлять магнитные свойства.
переходит в Fеα. При этом изменяются параметры кристаллической решетки ОЦК и железо начинает проявлять магнитные свойства.
Кроме железа, свойством полиморфизма обладают и другие металлы, например, марганец, кобальт, олово. Кристаллическое строение сплавов более сложное в сравнении с чистыми металлами. Сплавы в твердом состоянии могут образовывать механические смеси, химические соединения или твердые растворы. Механические смеси характеризуются отсутствием химического взаимодействия или взаимного растворения компонентов. Их кристаллическое строение характеризуется присутствием кристаллических решеток обоих компонентов сплава. В химическом соединении компоненты сплава в строгом соотношении по массе вступают в химическое взаимодействие. При этом образуется новая кристаллическая решетка. В твердых растворах компоненты сплава взаимно растворяются друг в друге в интервалах концентраций.
Кристаллическое строение твердых растворов определяется типом кристаллической решетки компонента сплава, который выполняет функцию растворителя. Различают два основных вида твердых растворов - замещения и внедрения (рис. 2). В твердых растворах замещения атомы растворенного компонента замещают отдельные атомы растворителя в узлах кристаллической решетки (рис.2.б). располагаясь в междоузлиях (рис.2, в).
 |

 |
При затвердевании расплава металла вначале образуются мельчайшие кристаллы правильной формы, затем, по мере охлаждения,они увеличиваются в размерах и срастаются между собой в виде деформированных (неправильной внешней формы) кристаллов. Кристаллы неправильной формы называют зернами. Зерно пред-ставляет собой комплекс одинаково ориентированных кристаллических решеток. Соседние зерна отличаются различной ориентацией кри-сталлических решеток. Они повернуты друг относительно друга на десятки градусов.
Кристаллические решетки зерна могут иметь различные несовершенства. Несовершенства кристаллических решеток в виде точечных и линейных дефектов и состояние границ зерен в металлах влияют на свойства металлов. К точечным дефектам относят вакансии, межузловые и примесные атомы. Точечные дефекты возникают за счет смещения отдельных частиц в кристалле с их мест с образованием вакансии и атома в междоузлии. Равновесная концентрация вакансий зависит от энергии образования пары вакансия – атом в междоузлии и температуры. Количество точечных дефектов понижается в процессе отдыха металла. Вакансии в кристалле перемещаются, т.к. их место может быть занято соседними атомами. Примесные атомы могут быть случайными и специально введенными для придания сплаву требуемых свойств. В местах расположения примесных атомов, а также дислоцированных атомов, оказавшихся в междоузлиях, кристаллическая решетка будет упруго искаженной. Даже при незначительной концентрации точечных дефектов они могут вызвать значительные изменения физических свойств кристалла.
К линейным дефектам относят цепочки вакансий и дислоцированных атомов (линейные и винтовые дислокации). Линейные дислокации возникают под влиянием пластических и температурных деформаций и являются следствием нарушения совпадения кристаллических плоскостей. Винтовые дислокации возникают при неполном сдвиге одной части кристалла относительно другой. Дислокации подвижны внутри кристаллов и активно взаимодействуют между собой и с другими дефектами.

 Поверхностные дефекты характерны для материалов, состоящих из кристаллов, различно ориентированных в пространстве и совпадают с границами зерен. Мозаичная кристаллическая структура образуется в результате сращивания отдельных кристаллических зерен под малыми углами, составляющими доли градуса. На границах зерен возникают области скоплений дефектов структуры - дислокаций и вакансий. Зависимость прочности кри-сталлического тела от плотности дефектов строения представлена на рис 3. Если прочность бездефектных кристаллов исключительно высока, то повышение плотности дефектов приводит к резкому ее снижению (Рк). Дальнейшее увеличение плот-ности дефектов специальными мето-дами искажения кристаллической решетки способно повысить реальную прочность металлов. Плотность дислокаций увеличивают закалкой и пластическим деформированием.
Поверхностные дефекты характерны для материалов, состоящих из кристаллов, различно ориентированных в пространстве и совпадают с границами зерен. Мозаичная кристаллическая структура образуется в результате сращивания отдельных кристаллических зерен под малыми углами, составляющими доли градуса. На границах зерен возникают области скоплений дефектов структуры - дислокаций и вакансий. Зависимость прочности кри-сталлического тела от плотности дефектов строения представлена на рис 3. Если прочность бездефектных кристаллов исключительно высока, то повышение плотности дефектов приводит к резкому ее снижению (Рк). Дальнейшее увеличение плот-ности дефектов специальными мето-дами искажения кристаллической решетки способно повысить реальную прочность металлов. Плотность дислокаций увеличивают закалкой и пластическим деформированием.
Дата добавления: 2016-02-09; просмотров: 1298;
