Антигенная структурааналогична таковой стрептококков; относятся к серогруппе D.
Факторы патогенности.Энтерококки являются УПМ. Факторы патогенности возбудителя — компоненты клеточной стенки, ферменты агрессии и токсины.
Экологическая ниша.Широко распространены в природе; обитают в кишечнике различных позвоночных и человека. Энтерококки входят в состав микрофлоры ротовой полости, кишечника и мочеполовой системы взрослых; так, E.faecium выделяют из испражнений у 25 % клинически здоровых лиц.
Устойчивость в окружающей средеболее высокая, чем у стрептококков, и приближается к таковой стафилококков, поэтому энтерококки используются в санитарной микробиологии в качестве санитарно-показательных микробов. Чувствительны к действию обычно применяемых антисептиков и дезинфек-тантов. Обладают природной устойчивостью к большинству антибиотиков, кроме того, все антибиотики, даже последних поколений,
действуют на энтерококки только бактериос-татически.
Эпидемиология ипатогенез аналогичны таковым стрептококковых инфекций.
Клиника.Часто вызывают поражения мочеполовой системы, особенно у катетеризированных пациентов; также вызывают 10—20 % всех бактериальных эндокардитов и 5 % бактериемии. Гемолизирующие энтерококки также способны вызывать пищевые отравления и дисбактериозы кишечника. В патологии человека наибольшее значение имеют Е. fae-calis, E. faecium и Е. durans.
Микробиологическая диагностика.Материал для исследования — гной, кровь, моча, и др. — определяется клинической картиной болезни.
Лабораторная диагностика включает бактериологический и серологический методы. Бактериоскопия мазков из исследуемого материала не проводится, так как в них энтерококки могут располагаться поодиночке, парами, тетрадами и другими способами и поэтому их невозможно морфологически отличить от других грамположительных кокков. Выделение возбудителя обычно не представляет трудностей энтерококки дифференцируют со стрептококками.
16.1.1.2.3. Аэрококки (род Aerococcus), лейконостоки (род Leuconostoc), педиококки (род Pediococcus) и лактококки (род Lactococcus)
Микробы родов Aerococcus, Leuconostoc, Pediococcus и Lactococcus обладают низкой па-тогенностью; заболевания, вызванные ими у человека, регистрируют достаточно редко (обычно у иммунокомпромиссных хозяев).
Род Aerococcus образуют неподвижные шаровидные клетки 1,0—2,0 мкм в диаметре; в мазках из культур, выращенных на жидких средах, располагаются тетрадами. Факультативные анаэробы, но лучше растут в микроаэрофиль-ных условиях. Образуют Н202, вызывая позеленение кровяного агара. Хемоорганотрофы с окислительным метаболизмом; углеводы ферментируют с образованием кислоты. Каталазаотрицательны или слабоположительны. Желатину не разжижают, нитраты не восстанавливают. Температурный оптимум — 30 °С (также растут при 10 °С, но не при 45 °С).
Типовой вид—A. viridans. Сапрофиты, широко распространенные в стационарах; иногда могут загрязнять оборудование для инвазивных исследований. Контаминирование медицинского инструментария способно приводить к эндокардитам и инфекциям мочевыводя-щих путей. Принципы выделения аэрококков аналогичны таковым при индикации стрептококковых инфекций; бактерии образуют беловато-серые колонии, сформированные крупными кокками, собранными в тетрады или пары. Подобно энтерококкам способны расти на средах, содержащих 6,5% NaCl, однако не растут при 10 "С и чувствительны к бацитрацину.
Род Leuconostoc — неподвижные неспо-рообразующие сферические, овальные или палочковидные (с закругленными концами) бактерии; средние размеры — 0,5/0,7x0,7/1,2 мкм. Факультативные анаэробы, хемоорганотрофы; нуждаются в наличии углеводов при культивировании; преимущественно ферментируют моно- и дисахариды с образованием кислоты и газа. Основные ферментативные продукты — лактат и этанол. Каталазаотрицательны; аргинин не гидроли-зуют; индол не образуют; нитраты не восстанавливают; гемолитическую активность не проявляют. Растут медленно; колонии мелкие, на средах с сахарозой образуют более крупные слизистые колонии. Широко распространены в природе, часто колонизируют пищевые продукты. Типовой вид — L. mesen-teroides. До 1985 г. отдельные сведения указывали на возможную роль лейконостоков в развитии пищевых токсикоинфекций, но затем появились многочисленные сообщения о выделении бактерий из крови новорожденных и больных с иммунодефицитами, страдающих бактериемиями, эндокардитами, пневмониями, а также из спинномозговой жидкости при менингитах. Колонии лейконостоков сероватого цвета; на кровяных средах гемолиза не вызывают. Отличительными особенностями являются способность гидролизовать эскулин в присутствии желчных солей, образование газа при ферментации глюкозы и резистентность к ванкомицину.
Род Pediococcus представлен шаровидными бактериями 1,0—2,0 мкм в диамет-
ре; в мазках встречаются в виде тетрад или парно. Неподвижны, спор не образуют. Факультативные анаэробы, но некоторые виды растут в микроаэрофильных или анаэробных условиях. Хемоорганотрофы; пищевые потребности сложные, нуждаются в наличии ферментируемых углеводов (моно- и диса-харидов). Глюкозу расщепляют с образованием газа; основной ферментативный продукт — лактат. Цитохромов не имеют; катала-заотрицательны; Нитраты не восстанавливают. Температурный оптимум — 25-40 "С. Широко распространены в природе, обычно на растениях и пищевых продуктах. Типовой вид — P. damnosus. Патогенность микробов остается недоказанной, несмотря на то что P. acidilactici можно выделить из ран и крови пациентов с иммунодефицитами. Колонии гладкие, беловато-серые, не дающие гемолиза на кровяных средах; образованы крупными кокками, собранными в тетрады или пары. Бактерии гидро-лизуют эскулин в присутствии желчных солей, не образуют газа при ферментации глюкозы и резистентны к ванкомицину.
Род Lactococcus представлен сферическими или овальными клетками 0,5/1,2х0,6/2,5 мкм; в мазках из бульонных культур располагаются парами или короткими цепочками. Неподвижны; спор не образуют; капсул не имеют. Факультативные анаэробы; хемоорганотрофы с ферментативным метаболизмом. Углеводы расщепляют с образованием преимущественно молочной кислоты. Пищевые потребности сложные. Каталаза- и оксида-заотрицательны; растут при 10 °С, но не при 45 "С (оптимум — 30 °С). По системе Л энсфилд АГ относятся к группе N. Колонизируют растения и пищевые продукты. Типовой вид — L. lactis. В настоящее время патогенность не доказана, имеются лишь сообщения о выделении из организма человека L. garviae, образующего беловатые негемолизирующие колонии, организованные коккобациллярными или нитчатыми клетками.
16.1.2. Аэробные грамотрицательные кокки
16.1.2.1. Нейссерии (род Neisseria)
Нейссерии — грамотрицательные аэробные кокки, относятся к роду Neisseria, включаю-
щему восемь видов: Neisseria meningitidis (менингококки), Neisseria gonorrhoeae (гонококки), N.flava, N. subflava, N. perflava, N. sicca, N. mucosa, N. flavescens. Обитают на слизистых оболочках человека и млекопитающих; 7 видов встречаются у человека, из них 5 видов являются представителями нормофло-ры носоглотки и верхних дыхательных путей (N. sicca, N. flavescens, N. perflava, N. mucosa и N. lactamica), хотя описаны единичные случаи их выделения при гнойных менингитах, отитах, синуситах и других ГВЗ у иммунокомпро-миссных лиц. Нейссерии содержат аллергены и могут быть причиной аллергических заболеваний (бронхиальная астма). Наибольшее клиническое значение имеют менингококки и гонококки. Основные отличительные признаки бактерий рода Neisseria представлены в табл. 16.6.
Морфология.Грамотрицательные неспоро-образующие кокки диаметром 0,6—1,0 мкм, неподвижны. Отличаются склонностью к образованию пар и тетрад, связанной с делением клеток в двух плоскостях; обращенные друг к другу поверхности бывают утолщены. Исключением считают Neisseria elongata, образующую короткие (0,5 мкм) палочки (дип-лобациллы и короткие цепочки). Некоторые виды имеют капсулу и микроворсинки.
Культуральные свойства.Аэробы, хемоорганотрофы. Температурный оптимум роста — 35—37 °С, патогенные виды могут расти в интервале температур 24—41 "С, а непатогенные способны к росту при температурах ниже 24 °С. Оптимум рН 6—8. Патогенные виды прихотливы к условиям культивирования, не растут на обычных питательных средах; непатогенные виды менее прихотливы. Виды, обитающие в носоглотке, образуют желтый пигмент — от слабо-желтого до яркого, особенно заметный у 48-часовых культур на плотных средах с добавлением куриного желтка. Наличие в питательной среде свободных жирных кислот ингибирует рост нейссерий, что инактивируют внесением крахмала, сыворотки или древесного угля.
Ферментативная активностьнизкая, особенно у патогенных видов. Имеют каталазу (исключая Neisseria elongata), цитохромокси-дазу; ферментация углеводов по оксидатив-
ному типу зависит от вида; конечный продукт — уксусная кислота Сахаролитические свойства выражены нечетко. Некоторые виды образуют сходный с крахмалом полисахарид на среде с 5 % сахара. Многие виды редуцируют нитриты, некоторые восстанавливают нитраты. Биохимические свойства нейссерий представлены в табл. 16.6.
Антигенная структура.Все виды нейссерий имеют полисахаридный соматический О-АГ; штаммы, образующие капсулу, также имеют капсульный антиген.
Факторы патогенности:капсула, пили, эндотоксин, поверхностные белки наружной мембраны. Патогенными для человека являются менингококки и гонококки.
Устойчивость в окружающей среденизкая, поэтому в культурах старше 1—2 суток практически не содержится живых клеток. Клинический материал транспортируют в лабораторию в утепленных контейнерах при
30—35 "С. Чувствительны к действию обычно применяемых антисептиков и дезинфектан-тов. Высокочувствительны к пенициллинам, тетрациклинам, стрептомицину
16.1.2.1.1. Менингококки
Менингококковая инфекция — это острое инфекционное заболевание человека, вызываемое Neisseria meningitidis, которое передается воздушно-капельным путем и характеризуется локальным поражением слизистой оболочки носоглотки с последующей генерализацией в виде менингококковой септицемии (менингококцемия) и воспаления мягких мозговых оболочек (менингококковый менингит).
Заболевание выделено в самостоятельную нозологическую форму после открытия возбудителя (Вайхзельбаум, 1887 г.). Описание морфологии менингококка дал Флекснер в 1907 г., а в 1899 г. Ослер выделил менингококк из крови больного,
что позволило окончательно установить этиологию инфекции.
Морфология.Клетки имеют округлую форму диаметром 0,6—1,0 мкм, располагаются попарно. Поверхности, обращенные друг к другу, вогнутые или ровные. Клетки полиморфны. Грамотрицательны, но отношение к окраске по Граму выражено недостаточно четко, поэтому в мазках наблюдается неравномерное окрашивание — молодые клетки окрашиваются интенсивно, а отмирающие и мертвые клетки — очень слабо. Жгутиков не имеют, спор не образуют. Клинические изоляты образуют макрокапсулу, которая утрачивается при росте на питательных средах.
Культуральные свойства.Строгий аэроб, капнофил. Очень требователен к питательным средам и условиям культивирования. На простых питательных средах не растет, поэтому для его культивирования к основным средам добавляют нативные белки (сыворотка, кровь, яичный желток и др.). В качестве источников углерода и азота используют аминокислоты (глутамин, таурин, аспарагин,
L-аргинин, глицин, тирозин), поэтому их необходимо включать в среду культивирования. Наиболее подходящей бессывороточной средой следует считать среду Мюллера— Хинтона, включающую полный набор аминокислот и мясной экстракт как источник факторов роста. Оптимум рН среды 7,2-7,4. Температурный оптимум роста 37 "С, рост наблюдается в пределах 30—38 "С. Повышенная концентрация С02 и влажность стимулируют рост менингококков. На сывороточном агаре образует круглые бесцветные нежные колонии маслянистой консистенции диаметром от 0,5 до 1,5 мм. В отличие от условно-патогенных нейссерий не образует пигмента. На кровяном агаре образует нежные округлые колонии слегка сероватого цвета с блестящей поверхностью. Не дает гемолиза, что отличает его колонии от колоний стафилококков, стрептококков и гемофилов. При первичном посеве очень требователен к условиям культивирования, поэтому отсутствие роста на бессывороточном агаре при 37 °С, на сывороточном агаре при 20 °С и среде с 5 % желчи
дифференцируют менингококки от условно-патогенных нейссерий.
Биохимическая активностьнизкая (см. табл. 16.6). Разлагает глюкозу и мальтозу до кислоты, не разжижает желатин, не образует индол и сероводород, не восстанавливает нитраты. Ферментация глюкозы и мальтозы является дифференциально-диагностическим признаком. В отличие от условно-патогенных нейссерий не образует крахмалоподобный полисахарид из сахарозы. Данный признак выявляется на сывороточном агаре с 5 % сахарозы с помощью водного раствора Люголя. Обладает, как и все аэробы, цитохромоксидазой и ката-лазой, что отличает его от пневмококков и гемофилов. Отсутствие |3-галактозидазы и наличие у-глютаминтрансферазы отличают менингококки от N. lactamica, колонизирующей слизистую носоглотки у детей.
Антигенная структура.Имеет несколько АГ: родовые, общие для рода нейссерий (белковые и полисахаридные, которые представлены полимерами аминосахаров и сиаловых кислот); видовой (протеиновый); группоспецифические (гликопротеидный комплекс); типоспецифи-ческие (белки наружной мембраны), которые разграничивают серотипы внутри серогрупп В и С; специфичность их достаточно ограничена, так как подобные АГ обнаруживают у представителей различных серогрупп и гонококков. По капсульным АГ выделяют девять серогрупп (А, В, С, D, X, Y, Z, W|3, и 29Е), а также сравнительно недавно выделенные еще четыре серогруппы (Н, I, К, L). Капсульные АГ некоторых серогрупп имму-ногенны для человека. Штаммы серогруппы А вызывают эпидемические вспышки, В, С и Y — спорадические случаи заболевания. Высокая вирулентность представителей серогруппы А связана, по-видимому, с их высокой инвазивной активностью. На основании различий типоспецифических АГ выделяют серотипы, которые обозначают арабскими цифрами (серотипы выявлены в серогруппах В, С, Y, W135). Особый интерес среди сероти-повых АГ представляет АГ серотип 2 группы В. Он наиболее изучен и является общим для штаммов, принадлежащих к группам В, С, Y, W135. Выявлено, что штаммы, выделенные от больных с генерализованной формой менин-
гококковой инфекции, часто относятся к се-ротипу 2. В связи с этим наличие АГ серотипа 2 рассматривается как фактор патогенности менингококка. Серотипирование имеет большое значение в эпидемиологии, так как периодически наблюдающиеся подъемы заболеваемости связаны со сменой циркулирующих серогрупп. Во время эпидемий преобладают менингококки групп А и С, которые являются наиболее патогенными.
Факторы патогенности.Основной фактор патогенности — капсула, защищающая менингококки от различных воздействий, в первую очередь от фагоцитоза. AT, образующиеся к полисахаридам капсулы, проявляют бактерицидные свойства. Токсические проявления менингококковой инфекции обусловлены высокотоксичным эндотоксином, который по летальности для лабораторных животных сравним с эндотоксинами энтеробактерий. Оба они оказывают сенсибилизирующее действие и индуцируют феномен Шварцмана в концентрациях, в 5-10 раз меньших, чем ЛПС грамотрицательной кишечной микрофлоры. Для генерализованных форм менингококковой инфекции характерны кожные высыпания, неотличимые от таковых при феномене Шварцмана. ЛПС менингококков проявляют выраженное пирогенное действие, а также вызывают образование AT Тяжесть болезни определяется количеством эндотоксина в крови больного. Эндотоксину принадлежит ведущая роль в патогенезе поражений сосудов и кровоизлияний во внутренние органы. Наиболее постоянный и диагностически значимый признак менингококцемии — экзантема в виде характерной геморрагической сыпи (петехии, пурпура, экхимозы).
К другим факторам патогенности относятся пили, белки наружной мембраны, наличие гиалуронидазы и нейроминидазы. Пили являются фактором адгезии к слизистой оболочке носоглотки и, предположительно, тканям мозговой оболочки. Менингококки выделяют IgA-протеазы, расщепляющие молекулы IgA в шарнирной области, что защищает бактерии от действия Ig.
Лабораторные животные мало восприимчивы к менингококку. Субдуральное введение живой культуры может вызвать заболевание у
кроликов, обезьян и коз. Внутрибрюшинное заражение белых мышей и морских свинок вызывает их гибель с явлениями интоксикации. Заражение в алантоисную полость 11—18-дневных куриных эмбрионов вызывает гибель эмбриона через 48 ч.
Устойчивость в окружающей среде.Слабо устойчив к внешним воздействиям, в оптимальных условиях на плотных и жидких средах культура гибнет через 48—72 ч, на полужидких средах сохраняется до месяца (рекомендуют сохранять на среде Дорсе, полужидком агаре и среде сО сливками). Наиболее приемлемый способ консервации культуры — лиофильное высушивание. Вне организма человека довольно быстро погибает, а при низкой температуре быстро теряет способность к образованию колоний, что необходимо учитывать при доставке материала в микробиологическую лабораторию; при высыхании погибает. При температуре 10 °С погибает через 2 ч, температура 55 °С убивает его через 5 мин, 80 °С— за 1-2 мин, кипячение — моментально (аналогичный эффект оказывает ультрафиолетовое облучение). Чувствителен к действию обычно применяемых антисептиков и дезинфектантов, особенно к солям тяжелых металлов. Под действием 1% раствора фенола гибнет в течение 1 мин, аналогичное действие оказывают 0,5—1% раствор хлорамина, 70% этанол, 3—5% раствор карболовой кислоты. Чувствителен к большинству применяемых в клинике антибиотиков, однако в последние годы отмечается тенденция к росту числа резистентных штаммов.
Эпидемиология.Экологической нишей для менингококка является слизистая оболочка носоглотки человека. Источник инфекции — больной человек или носитель. Различают три группы источников инфекции: больные генерализованными формами (около 1 % от общего числа инфицированных лиц), больные назофа-рингитом (10—20 % от общего числа инфицированных лиц) и здоровые носители. Основное значение имеют здоровые носители, которые составляют до 80-90 %. Здоровое носитель-ство у детей 1—2 лет встречается очень редко; с возрастом количество носителей нарастает, достигая максимума к 14—19 годам. Носительство продолжается в среднем 2-3 недели, при наличии хронических воспали-
тельных процессов носоглотки может длиться 6 недель и более.
Механизм передачи — аэрогенный, путь — воздушно-капельный. В отличие от других респираторных инфекций заражение происходит при длительном и тесном контакте. Заболеваемость носит сезонный характер, увеличиваясь в осенне-зимний период.
Восприимчивость к менинкококку невысокая. Болеют в основном дети до 15 лет (70—80 %) и лица юношеского возраста (10— 15 %). Возникновению вспышек способствует скученность детей в детских организованных коллективах, учащихся школ и техникумов, студентов в общежитиях, новобранцев в казармах и т. п. Заболевания возникают при низком распространении носительства менингококка в коллективе (2 % и ниже). В коллективах, где носительство составляет 20 % и выше, заболевания не регистрируются, поскольку интенсивная циркуляция менингококка иммуноло-гически перестраивает организм, обеспечивая «естественную иммунизацию» населения в эндемичных очагах заболевания.
Упоминания об эпидемиях цереброспинального менингита встречаются в трудах античных врачей. Первые клинические описания менингококкового менингита сделали в XVII в. Уйллис (Виллизии) и Сиденхэм. В настоящее время менингококковая инфекция зарегистрирована более чем в 150 странах мира, в том числе в России. В Африке имеется гиперэндемическая зона заболеваемости менингококковой инфекцией, так называемый «менингитный пояс», которая охватывает районы, расположенные между югом Сахары и экваториальным лесом, Красным морем и Атлантическим океаном. В «менингитном поясе» расположены 15 стран, через которые проходит трансконтинентальная дорога, с которой связывают распространение менингококковой инфекции, — эпидемии отмечаются здесь через каждые 10—15 лет.
Патогенез. Менингококки внедряются в организм человека через слизистые оболочки носоглотки. Размножаясь, они формируют первичный очаг воспаления. По окончаниям обонятельного нерва воспалительный процесс может распространиться на оболочки мозга. Возможно и гематогенное распространение менингококка по организму. Важная роль в патогенезе принадлежит эндотоксину, который участвует в развитии токсического шока и угнетении фаго-
цитарной активности нейтрофилов. Патогенез заболевания включает поражения токсического и септического характера в сочетании с аллергическими реакциями. Преобладание того или иного компонента проявляется в различных клинических формах.
Клиника.Менингококковая инфекция клинически протекает в локализованной форме: менингококконосительство, острый назофа-рингит или в генерализованной форме: ме-нингококцемия, менингит, менингоэнцефа-лит, эндокардит, артрит, полиартрит, иридо-циклит, пневмония.
Эпидемический цереброспинальный менингит начинается внезапно, после 5—7-дневного инкубационного периода. В начале болезни отмечаются сильная головная боль, рвота, высокая лихорадка, затем развиваются менингеальные симптомы. Однако следует отметить, что степень проявления менингеальных симптомов значительно варьирует. Поскольку клиническая картина не отличается от клиники менингитов, вызванных другими микробами, то поставить этиологический диагноз клинически крайне сложно, поэтому ведущая роль здесь отводится методам лабораторной микробиологической диагностики.
Иммунитет.Постинфекционный иммунитет при генерализованных формах инфекции довольно стойкий, повторные случаи заболевания почти не наблюдаются, однако иммунитет носит гуморальный и группоспецифи-ческий характер.
Невосприимчивость кменингококку обусловлена наличием сывороточных противоменинго-кокковых бактерицидных AT. Новорожденные дети обладают естественным приобретенным пассивным трансплацентарным иммунитетом в течение 2—6 месяцев. Изучение уровня AT у представителей разных возрастных групп выявило, что дети с 6 месяцев до 10 лет имеют низкий уровень AT У детей 10-15 лет наблюдается рост титра AT к полисахаридному, белковому и ЛПС АГ. Развитие иммунных реакций вызывают капсульные полисахариды менингококков групп А и С. Защиту обеспечивают AT, проявляющие комплементзависимую бактерицидность. Элиминацию возбудителя со слизистой оболочки и из тканей осуществляют комплементсвя-зывающие IgM и IgG. Для эффективного уничтожения менингококков необходима активация комплемента, вызывающего лизис бактерий.
При менингококконосительстве выявлены гомологичные и группоспецифические AT к менингококкам. Это явление рассматривается как естественная иммунизация «живой» вакциной.
Микробиологическая диагностика.Выбор материала для исследования обусловлен клинической формой болезни. Материалом для исследования служат носоглоточная слизь (от больных и носителей), ликвор, кровь, гной с мозговых оболочек, соскоб из элементов геморрагической сыпи на коже и др. При цереброспинальном менингите основным исследуемым материалом является ликвор, который берут в день госпитализации больного асептически люмбальной пункцией в количестве 2—5 мл. Ликвор собирают в стерильную пробирку и сразу же сеют на питательные среды или же немедленно, не допуская охлаждения, отправляют в лабораторию. Носоглоточную слизь берут специальным тампоном, изогнутым под углом, с задней стенки глотки при визуальном контроле, вводя тампон за мягкое нёбо. От трупа исследуемый материал (гной с оболочек мозга, из кожных поражений и т. п.) берут во время вскрытия. Поскольку менингококки очень неустойчивы вне организма человека, клинический материал транспортируют в утепленных контейнерах при 30—35 °С.
Для микробиологической диагностики применяют бактериоскопический, бактериологический и серологический методы.
Бактериоскопическое исследование ликвора и крови позволяет определить наличие возбудителя. При наличии гнойного ликвора готовят мазки без предварительной обработки; если ликвор прозрачный или мутный, его центрифугируют при 3500 об/мин в течение 5 мин, а затем из осадка готовят мазки, которые окрашивают по Граму, метиленовым синим и другими методами для определения лейкоцитарной формулы, выявления менингококков и определения их количества. При микроскопии мазков ликвора в положительных случаях наблюдают полинуклеарные лейкоциты, эритроциты, нити фибрина и менингококки в виде типичных грамотрицательных диплококков бобовидной формы, окруженных капсулой в виде плохоокрашенного ореола. Результаты микроскопического исследования использу-
ются только в качестве предварительного, ориентировочного ответа, поскольку морфологически нельзя отдифференцировать менингококк от других грамотрицательных бактерий, способных вызывать менингит (гонококки, другие нейссерии, гемофилы, бранхамеллы). Для микроскопического исследования крови готовят препарат «толстой капли», который высушивают и окрашивают метиленовой синькой без фиксации. При микроскопии в положительных случаях обнаруживают на голубом фоне менингококки, имеющие типичную морфологию, окруженные капсулой в виде бесцветного ореола. Трупный материал исследуют только бактериоскопически из-за низкой жизнеспособности менингококка. Носоглоточная слизь не микроскопируется из-за наличия в ней условно-патогенных нейссерии, морфологически сходных с менингококком.
Бактериологическое исследование проводят с целью выделения и идентификации чистой культуры менингококка. Бактериологическому исследованию подвергают носоглоточную слизь, кровь и ликвор. Посев материала для получения чистой культуры производят на плотные или полужидкие питательные среды, содержащие сыворотку, кровь или асцитическую жидкость. Культуры инкубируют в течение 18—24 ч при 37 "С в сосуде со свечой или в специальном термостате с повышенным содержанием (8—10 %) СОг Идентификацию выделенной культуры проводят на основании следующих свойств:
• оксидазаположительные колонии рассматривают как возможно принадлежащие к видам Neisseria;
• наличие в культуре Neisseria meningitidis подтверждают образованием уксусной кислоты при ферментации глюкозы и мальтозы (но не лактозы, сахарозы и фруктозы);
• принадлежность к серогруппам определяют в реакции агглютинации (РА).
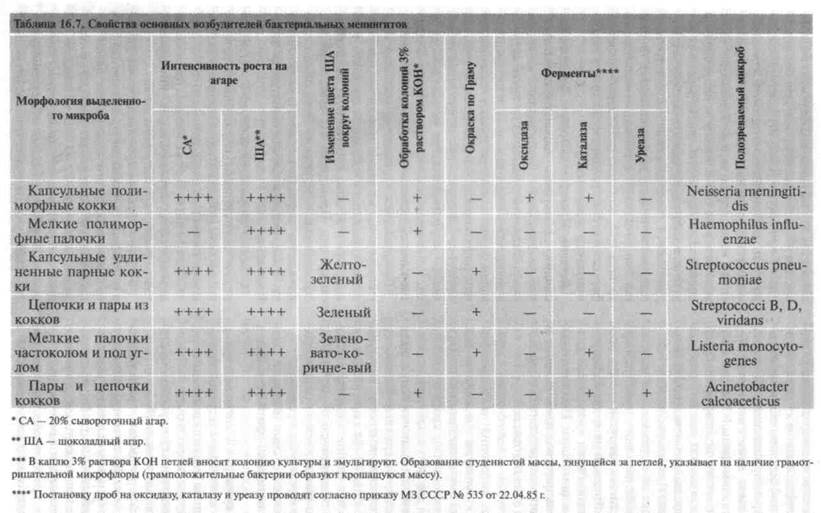
Проводят дифференциацию выделенной культуры с другими бактериями, вызывающими менингит. Основные свойства возбудителей бактериальных менингитов, учитываемые через 24 ч от начала бактериологического исследования, представлены в табл. 16.7.
Серологический метод используют для обнаружения растворимых бактериальных АГ в
ликворе и других видах исследуемого материала или AT в сыворотке крови. Для обнаружения АГ применяют ИФА, РИА, иммуноэлект-рофорез, реакцию коагглютинации. У больных менингококковой инфекцией AT обнаруживаются с конца первой недели болезни, достигая максимума на 2—3-й неделе, а затем их титр снижается. У больных и лиц, перенесших ме-нингококковую инфекцию, в сыворотке обнаруживаются специфические AT: бактерицидные, агглютинины, гемагглютинины. В разгар менингококковой инфекции повышается уровень IgM, особенно при генерализованных формах; в период реконвалесценции, в основном, обнаруживаются IgG.
Лечение.Препарат выбора — бензилпени-циллин, эффективны также полусинтетические пенициллины (ампициллин, оксацил-лин). Оптимально назначение антибиотиков в сочетании с диуретиками. При непереносимости пенициллинов назначают левомицетин или рифампицин. Антимикробную терапию следует сочетать с симптоматическими средствами, корригирующими водно-солевой и кислотно-щелочной баланс, а также с седа-тивными средствами и глюкокортикоидами.
Профилактика.Проводится комплекс мер, направленных на ликвидацию источника инфекции: больных необходимо выявлять, изолировать и лечить; носителей — выявлять и санировать. Проводится бактериологическое обследование в окружении больного с целью выявления здоровых носителей менингококка. Выявленные носители санируются антибиотиками.
С целью разрыва механизма и путей передачи разуплотняют и разобщают детские коллективы, общежития, казармы. Роспуск контактировавших лиц производится на срок от 10 до 30 дней. В очаге проводятся текущая дезинфекция, проветривание помещений, ультрафиолетовое облучение и т. п.
В очаге инфекции проводится специфическая активная и пассивная профилактика. Для создания пассивного иммунитета детям дошкольного возраста вводят однократно иммуноглобулин в дозе 1,5—3,0 мл не позднее 7-го дня после регистрации первого случая заболевания. Профилактический эффект иммуноглобулина сохраняется в течение нескольких
|
месяцев после введения. Для активной иммунизации используют вакцины из очищенных капсульных полисахаридов менингококков серогрупп А и С. В России проводят вакцинацию групп риска менингококковой вакциной А или бивакциной А+С. Кроме того, возможно проведение химиопрофилактики с применением антибиотиков в замкнутых коллективах,, если имеет место хотя бы один случай менингококковой инфекции.
16.1.2.1.2. Гонококки
Гонококковая инфекция — это острое или хроническое инфекционное заболевание человека, вызываемое Neisseria gonorrhoeae, которое передается половым путем и характеризуется гнойным воспалением слизистой оболочки мочеполовых путей (гонорея), конъюнктивы глаз (бленнорея), других органов, интоксикацией.
Возбудитель гонореи был открыт Нейссером в 1879 г. Первые культуры получили Лейстков и Леффлер (1882), этиологическую роль доказал Бумм (1885).
Морфология.Неподвижные аспорогенные грамотрицательные диплококки (средний размер клетки 1,25+1,0x0,7+0,8 мкм), образующие капсулу. Полиморфны — встречаются более мелкие или более крупные клетки, а также палочковидные формы. Хорошо окрашиваются анилиновыми красителями (мети-леновым синим, бриллиантовым зеленым и др.), цитоплазма имеет осмиефильные включения. Под действием пенициллина образуют.!,-формы; под влиянием химиопрепаратов быстро меняют свойства и становятся грам-пол ожительными.
Культуральные свойства.Аэробы, хемоорга-нотрофы; для роста требуют свежеприготовленных влажных питательных сред с добавлением нативных белков крови, сыворотки или асцитической жидкости; широко используют безасцитные среды (например, среда КДС-1 с гидролизатом казеина, дрожжевым аутоли-затом и нативной сывороткой); оптимум рН 7,2—7,4, температуры — 37 "С. Не вызывают гемолиза на средах, содержащих кровь; на средах с добавлением молока, желатина и картофеля не растут. Через 24 ч на плотных питательных средах гонококки, содержащие в
клеточной стенке протеин 11, образуют слегка мутные бесцветные колонии; бактерии, не содержащие протеин II, образуют круглые прозрачные колонии в виде капель росы (1—3 мм в диаметре) с ровными краями. На жидких питательных средах растут диффузно и образуют поверхностную пленку, через несколько дней оседающую на дно.
Биохимическая активностькрайне низкая (см. табл. 16.6). Разлагают только глюкозу с образованием кислоты, измененные формы иногда не ферментируют ни одного углевода, продуцируют каталазу и цитохромоксидазу. Протеолитическая активность отсутствует, аммиака, сероводорода и индола не образуют.
Антигенная структурасложная. Содержат соматический и капсульный антигены. ЛПС проявляют сильные иммуногенные свойства; основной пул антител, синтезируемых в организме, составляют Ig к ЛПС, которые обладают бактерицидным действием. Основную антигенную нагрузку несут пили и поверхностные белки наружной мембраны. Пили состоят из цепочек белковых субъединиц (молекулярная масса около 20 000 Да), остатков Сахаров и фосфорной кислоты; нарушение последовательности соединения субъединиц изменяет Антигенные свойства. Наружная мембрана содержит протеины I, II и III классов, которые проявляют сильные иммуногенные свойства; на основании их состава выделяют 16 сероти-пов. В присутствии комплемента AT к белкам клеточной стенки проявляют бактерицидные свойства. Вариабельность протеинов, детерминированная кодированием в нескольких генах, определяет высокую частоту антигенных вариантов. Экспрессия некоторых АГ гонококка определяется изменением условий окружающей среды.
Факторы патогенности:капсула, пили, эндотоксин, поверхностные белки наружной мембраны, протеазы.
Все свежевыделенные культуры имеют капсулу, которая обладает антифагоцитарным действием (препятствует прямому контакту микробицидных субстанций с клеточной стенкой, маскирует ее антигенные детерминанты). АТ-опсонины к АГ капсулы стимулируют фагоцитоз гонококков. Полисахариды в капсулах не обнаружены, присущие им функции выполняют высокомолекулярные поверхностные полифосфаты.
Пили обеспечивают адгезию к эпителию. Генетически опосредованная вариабельность строения пилей обеспечивает прикрепление и выживаемость гонококков на клетках эпителия при смене хозяина и воздействии AT. У авирулентных штаммов они отсутствуют.
Клеточная стенка содержит эндотоксин.
Наружная мембрана содержит белки трех классов. Поверхностный белок 1 класса обуславливает устойчивость к бактерицидным факторам слизистых оболочек, а также инвазивные свойства бактерий и их способность вызывать системные инфекции. Поверхностный белок П класса образует отдельную белковую фракцию, называемую протеинами мутности или Ора-протеина-ми (от англ. opacity — мутность). Их считают первичными факторами вирулентности гонококков, и они обуславливают прикрепление к эпителию, а также ингибируют фагоцитарные реакции.
Синтезируют IgArnpomea3y, действующую внекле-точно и разрушающую пролин-треониновые связи в тяжелых цепях Ig, а также расщепляющую молекулу IgA в шарнирной области. Эти эффекты инактивируют AT, препятствующие адгезии, что облегчает прикрепление к рецепторам эпителиальных клеток, а также защищает бактерии от фагоцитоза, опосредованного AT
Устойчивость в окружающей среде.Гонококки очень неустойчивы во внешней среде, что следует помнить при заборе и транспортировке исследуемого клинического материала. Чувствительны к действию обычно применяемых антисептиков и дезинфек-тантов, особенно к солям тяжелых металлов. Высокочувствительны к пенициллинам, тет-рациклинам, стрептомицину. Способность к синтезу р-лактамаз обусловлена R-плазми-дой, но среди выделенных в клинике штаммов число продуцентов р-лактамаз невелико.
Эпидемиология.Термин «гонорея» ввел Талон во II в. н. э., хотя заболевание известно очень давно; во всяком случае, в вавилонских, ассирийских и греческих мифах упоминается болезнь, являющаяся, судя по описанию клинической картины, гонореей. В настоящее время гонорею относят к наиболее распространенным инфекционным заболеваниям, передаваемым половым путем. Источник инфекции — больной человек, особенно хронической бессимптомно протекающей формой гонореи. Экологической нишей являются слизистые оболочки мочеполовых путей человека. Механизм передачи— контактный,
путь — половой, крайне редко — бытовой (например, больная гонореей мать может заразить маленькую дочь при пользовании общей мочалкой, сиденьем унитаза и т. п.). Восприимчивость к гонококкам очень высокая.
Патогенез.Входными воротами для возбудителя служит цилиндрический эпителий уретры, шейки матки, конъюнктивы и прямой кишки. Взаимодействие гонококков с эпителиальными клетками опосредовано пи-лями, взаимодействующими с рецепторами эпителиальных клеток, что имеет решающее значение в развитии инфекции. Гонококки прикрепляются к эпителию, где мишенью для их цитотоксического действия служат поверхностные структуры клеток. Бактерии вызывают гибель и слущивание клеток, что нарушает процесс самоочищения слизистых оболочек. Нарушение функций слизистых вызывают как сами бактерии, так и ЛПС, а также пеп-тидогликаны клеточных стенок гонококков. Микроворсинки клеток, лишенных ресничек, действуя как псевдоподии, захватывают бактерии, попадающие внутрь этих «непрофессиональных» фагоцитов. Подобное явление известно как эндоцитоз, опосредованный патогенным микробом. В цитоплазме клеток фагосомы сливаются в гигантские вакуоли, где гонококки размножаются, оставаясь недоступными действию AT, фагоцитов и многих антибиотиков. Вакуоли сливаются с ба-зальной мембраной, и бактерии попадают в прилегающую соединительную ткань, где вызывают местное воспаление, либо проникают в кровоток с возможным последующим диссе-минированием. Прикрепившись к эпителию, гонококки становятся недоступными для фагоцитоза. Размножение Neisseria gonorrhoeae внутри нейтрофилов остается предметом дискуссии. В окрашенных мазках клинического материала гонококки видны как внутри, так и вне нейтрофилов. Создается впечатление, что большинство фагоцитированных нейтрофи-лами бактерий подверглось внутриклеточному лизису, однако это положение не бесспорно, поскольку имеются отдельные сведения о способности гонококков выживать и реплицировать в фагоцитах за счет нарушения регуляции образования каталазы и подавления активности эндоперекисей в фаголизосомах.
Таблица 16.8. Локализация и виды гонококковой инфекции
Инфекции нижних отделов мочеполового тракта:
1. Цервицит
2. Уретрит (у мужчин и женщин)
3. Абсцессы желез, прилегающих к влагалищу (преддверные и парауретральные железы) Инфекции верхних отделов мочеполового тракта:
1. Эндометрит
2. Эпидидимит
3. Воспалительные заболевания газовых органов (воспаление фаллопиевых труб, яичника и тканей придатков) .
Инфекции прочих органов и тканей:
1. Проктит (ректальная гонорея)
2. Фарингит
3. Бленнорея
4. Тазовый перитонит и перигепатит (синдром Фитц-Хью — Куртиса)
5. Фарингеальная гонорея Диссеминированная гонококковая инфекция:
1. Синдром дерматита-артрита-тендосиновиита (лихорадка, полиартрит, тендосиновиит и кожные поражения в виде геморрагических папул и пустул, вызванные иммунными комплексами или гонококками)
2. Септический моноартикулярный артрит
3. Редко развивающиеся поражения (эндокардит с поражением клапанов и менингит)
Гематогенное диссеминирование инфекции отмечают у 1 % заболевших.
Клиника.Гонококковая инфекция проявляется в виде гнойного воспаления слизистой оболочки мочеполовых путей (гонорея), конъюнктивы глаз (бленнорея), других органов. Инкубационный период 2—4 дня. Заболевание характеризуется резью при мочеиспускании, выделению гноя из уретры. Заболевание имеет тенденцию к переходу в хроническую бессимптомную форму. Нелеченая гонорея является одной из основных причин бесплодия как у мужчин, так и у женщин. Нелеченая бленнорея ведет к слепоте.
Гонококковая инфекция проявляется воспалением тазовых органов и бесплодием у женщин. Диссеминирование возбудителя может приводить к пельвиоперитониту, менингитам, артритам, эндокардитам и септицемиям. Женщины более склонны к диссеминированным поражениям. Заболевание у
них часто протекает бессимптомно, поэтому своевременное лечение не проводится, что делает женщин основным резервуаром инфекции. У мужчин бессимптомное течение гонореи наблюдают редко. Клинические формы гонококковой инфекции представлены в табл. 16.8.
Иммунитетпо своему механизму — нестерильный, практически отсутствует после перенесенного заболевания, поэтому часто регистрируются повторные заболевания.
Дата добавления: 2016-02-04; просмотров: 4048;
