ОЧИЩЕННЯ ВИКИДІВ ВІД ГАЗО- І ПАРОПОДІБНИХ ЗАБРУДНЕНЬ
Технологічні гази промислових агрегатів (печей, котлів, ванн, вагранок) крім твердих частинок вміщують шкідливі газо- і пароподібні викиди у вигляді окислів сірки і азоту, окису вуглецю, сірководню, хлору, хлористого водню тощо, які забруднюють атмосферу. Вловлювання газоподібних викидів має на меті санітарне очищення газів і використання напівпродуктів, які вловлюються, для одержання добрив, кислот, сірки та інших цінних хімічних продуктів.
Методи очищення промислових викидів від газоподібних забруднень за характером протікання фізико-хімічних процесів поділяються на шість основних груп:
- поглинання при промиванні газів рідинами – абсорбція;
- промивання викидів розчинами реагентів, які хімічно сполучають домішки – хемосорбція;
- поглинання газоподібних домішок твердими активними речовинами – адсорбція;
- термічна нейтралізація газів;
- поглинання домішок шляхом застосування каталітичних перетворень;
- біохімічне очищення газів.
Абсорбція
Абсорбція – фізико-хімічний процес поглинання речовин з розчинів чи сумішей газів твердими тілами або рідинами з утворенням розчинів. При абсорбції поглинання речовини відбувається всім об’ємом поглинача. Абсорбція знаходить широке застосування в техніці, головним чином для розділення газоподібних сумішей на складові частини шляхом розчинення одного чи декількох компонентів цієї суміші в рідині, яка називається абсорбентом. Фізична сутність процесу абсорбції пояснюється плівковою теорією, згідно з якою при стиканні рідини і газоподібних речовин на поверхні поділу обох фаз утворюються рідинна і газова плівки. Розчинний в рідині компонент газоподібної суміші проникає шляхом дифузії спочатку крізь газову плівку, а потім крізь рідинну і надходить у внутрішні шари адсорбенту. Для здійснення дифузії необхідно, щоб концентрація розчиненого компонента в газовій суміші перевищувала його рівновагову концентрацію над рідиною. Якщо концентрація розчинного компонента в газоподібній суміші менша його рівновагової концентрації над рідинною, дифузія відбувається у зворотному напрямку. В цьому випадку замість поглинання розчиненого компонента відбувається виділення його з розчину в газоподібному стані. Такий процес називається десорбцією і застосовується в техніці для витягання поглинених речовин з абсорбенту.
Типова схема промислової абсорбційної установки наведена на рисунку 6.1. Апарат для поділу суміші газів на складові частини шляхом розчинення одного чи декількох компонентів цієї суміші в рідині називається абсорбером.
абсорбент

абсорбент
a) б)
Рисунок 6.1 – Схема абсорбера:
1 – корпус; 2 – горизонтальні решітки; 3 – насадки; 4 – підведення абсорбенту; 5 – перерозподільний пристрій для рідини; 6 – виведення абсорбенту
Звичайний абсорбер, який називають також скрубером, – це металева або керамічна колона діаметром до 6 м і висотою до 40 м з декількома горизонтальними решітками, на яких розміщена насадка, що збільшує поверхню стикання рідини і газів. Найбільш розповсюдженими насадками є куски коксу, каміння та металеві або керамічні кільця. Суміш газів подається в нижню частину колони і піднімається вверх. Назустріч їй насадками стікає вниз абсорбент, внаслідок чого один або декілька газів цієї суміші розчиняються в рідині. Нерозчинені складові частини газової суміші видаляються з абсорбера через вихідний патрубок, а рідина витікає трубопроводом.
Вирішальною умовою при виборі абсорбенту є розчинність в ньому витягуваного компонента та її залежність від температури і тиску. Якщо розчинність газів при 0°С і парціальному тиску складає сотні грамів на 1 кг розчинника, то такі гази називають добре розчинними.
Для видалення з технологічних викидів таких газів, як аміак, хлористий або фтористий водень доцільно застосовувати як поглинальну рідину воду [34], тому що розчинність їх у воді складає сотні грамів на 1 кг Н2О. При поглинанні ж з газів сірчаного ангідриду чи хлору витрати води будуть значними, тому що розчинність їх складає соті частки грама на 1 кг води. В деяких спеціальних випадках замість води застосовують водні розчини таких хімічних речовин, як сірчана кислота (для вловлювання водяних парів), в’язкі масла (для вловлювання ароматичних вуглеводнів із коксового газу) тощо.
Контакт газового потоку з рідким розчинником здійснюється пропусканням газового потоку через насадкову колону (рис. 6.1) або розпиленням рідини чи барботажем газу через шар абсорбувальної рідини. Залежно від реалізованого способу контакту газ – рідина розрізняють:
- насадкові башти: форсункові (рис. 5.1), відцентрові скрубери (рис. 5.7 і 5.8);
- барботажно-пінні (рис. 5.4) скрубери;
- скрубери Вентурі (рис. 5.11…5.14) та інші.
Розрахунок абсорбера складається з визначення об’ємних витрат поглинальної рідини Qp , необхідної поверхні дотику газу з рідиною і параметрів допоміжних апаратів (потужність насосів, розмір баків тощо).
Об’ємні витрати поглинальної рідини розраховують з рівняння матеріального балансу процесу абсорбції – маса поглиненого компонента m, г/с, яка видалена з очищуваного газу, повинна бути рівна масі цього компонента, яка перейшла в рідину:
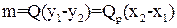 , (6.1)
, (6.1)
де 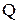 – об’ємні витрати газу, який очищається, м3/с;
– об’ємні витрати газу, який очищається, м3/с;
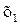 i
i 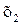 – початкова і кінцева концентрації газового компонента в поглинальній рідині, г/м3 ;
– початкова і кінцева концентрації газового компонента в поглинальній рідині, г/м3 ;
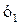 і
і 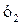 – початкова і кінцева концентрації газоподібного компонента в газі, який очищається, г/м3 .
– початкова і кінцева концентрації газоподібного компонента в газі, який очищається, г/м3 .
Необхідну поверхню дотику газу 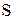 , м2 , з рідиною визначають за формулою:
, м2 , з рідиною визначають за формулою:
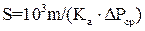 , (6.2)
, (6.2)
де 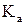 – коефіцієнт абсорбції (коефіцієнт масопередачі), кг/(м2·год·Па);
– коефіцієнт абсорбції (коефіцієнт масопередачі), кг/(м2·год·Па);
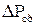 – середня рушійна сила абсорбції, Па.
– середня рушійна сила абсорбції, Па.
Коефіцієнт абсорбції характеризує швидкість розчинення газового компонента в рідині й визначається загальним опором дифузії цього компонента через газову і рідинну плівки. Для добре розчинних газів значення коефіцієнта абсорбції можна визначити за формулою, яка запропонована І. Л. Пейсаховим:
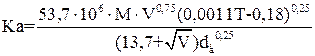 , (6.3)
, (6.3)
де 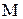 – молекулярна маса компонента, який поглинається, кг;
– молекулярна маса компонента, який поглинається, кг;
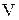 – швидкість газу у вільному перерізі скрубера, м/с;
– швидкість газу у вільному перерізі скрубера, м/с;
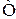 – абсолютна температура газу, К;
– абсолютна температура газу, К;
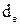 – еквівалентний діаметр насадки, рівний збільшеному вчетверо значенню живого перерізу насадки, поділеного на її питому поверхню, м.
– еквівалентний діаметр насадки, рівний збільшеному вчетверо значенню живого перерізу насадки, поділеного на її питому поверхню, м.
Рушійна сила абсорбції рівна різниці парціального тиску компонента, який поглинається в газовій фазі, та рівноважного парціального тиску цього компонента над поглинальною рідиною. Для підрахунку середньої рушійної сили абсорбції необхідно знайти середньоарифметичне значення рушійної сили абсорбції виходячи з її значення на вході та виході з апарата. Якщо ці значення відрізняються більше як в два рази, то ∆Pcp, Па, необхідно розрахувати як середню логарифмічну величину:


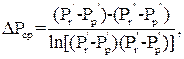 (6.4)
(6.4)

де 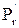 і
і 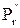 – відповідний парціальний тиск компонента, який поглинається в газовій фазі на вході та виході з апарата, Па;
– відповідний парціальний тиск компонента, який поглинається в газовій фазі на вході та виході з апарата, Па;
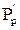 і
і 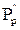 – відповідно парціальний рівноваговий тиск компонента, який поглинається над рідиною на вході та виході з апарата, Па.
– відповідно парціальний рівноваговий тиск компонента, який поглинається над рідиною на вході та виході з апарата, Па.
Слід мати на увазі, що при протитечії (газ і рідина рухаються назустріч один одному) значення ∆Pcp більше, ніж при прямотечії (газ і рідина рухаються в одну сторону). Отже, протитечія вигідніша, тому що для її здійснення необхідна апаратура меншого розміру. Прямотечію доцільно застосовувати, коли рівноваговий тиск компонента, який поглинається, над рідиною дуже малий і майже не збільшується при розчиненні газового компонента. Звичайно це здійснюється в тих випадках, коли компонент газу, який розчиняється, вступає в реакцію з рідиною або її компонентами (хемосорбція). Прямотечія особливо неефективна для погано розчинних газів.
Хемосорбція
Хемосорбція – поглинання газів, парів і розчинених речовин твердими чи рідкими поглиначами (сорбентами) з утворенням малолетких чи малорозчинних хімічних сполук. Прикладами хемосорбції в системі тверде тіло – газ (пара) можуть бути: поглинання кисню окислом барію при температурі біля 600°С з утворенням перекису барію, поглинання азоту розжареним металевим магнієм з утворенням нітриду магнію. Звичайне окислення металів можна розглядати як хемосорбцію кисню повітря. Газоподібний двоокис вуглецю сорбується гашеним вапном з утворенням вуглекислого кальцію. Пари хлорного водню поглинаються гашеним вапном, утворюючи при цьому хлорний кальцій.
Максимальна кількість речовини, яка поглинається, визначається стехіометричною ємністю і пружністю парів одержаної хімічної сполуки при даній температурі. Поглинання відбувається звичайно в динамічних умовах, тобто при продуванні пароповітряної суміші через шар зернистого хемосорбенту або при барботуванні газу через шар поглинального розчину. Проте для системи тверде тіло – газ (пара) стехіометрична ємність практично не використовується, тому що гальмом хімічної реакції є процес дифузії поглинальної речовини крізь шар продуктів реакції, утворених на зернах поглинача. Для кращого використання ємності доцільно наносити тонкий шар хемосорбенту на пористу основу – вугілля, пемзу тощо. Хемосорбція при певних умовах є зворотним процесом.
Хемосорбція застосовується в техніці при поглинанні двоокису вуглецю, окислів азоту, сірчаного ангідриду, аміаку тощо [34]. Поглинання звичайно здійснюється в колонах, споряджених пористою насадкою, через яку зверху подається поглинальний розчин, а знизу – потік пароповітряної суміші.
Адсорбція
Адсорбція – поглинання якої-небудь речовини з газоподібної суміші або розчину поверхневим шаром рідини, або твердого тіла. Речовина, на поверхні якої проходить адсорбція, називаєтеся адсорбентом, а та, що поглинається з об’ємної фази, – адсорбатом. Залежно від характеру взаємодії між молекулою адсорбату і адсорбентом адсорбцію прийнято поділяти на фізичну адсорбцію і хемосорбцію. Фізична адсорбція обумовлена силами міжмолекулярної взаємодії, які зв’язують молекули в рідинах і деяких кристалах, та проявляється в поведінці сильно стиснутих газів. При хемосорбції молекули адсорбату і адсорбенту утворюють хімічні сполуки. Часто адсорбція обумовлена як фізичними, так і хімічними силами, тому не існує чіткої границі між фізичною адсорбцією і хемосорбцією.
Установки, в яких здійснюють адсорбцію, називаються адсорберами. Існують адсорбери періодичної та безперервної дії.
В адсорберах періодичної дії газова суміш, з якої повинні бути витягнуті деякі компоненти, надходить через патрубок 1 в адсорбер (рис. 6.2), проходить через шар пористого адсорбенту 2, розташованого на горизонтальній решітці 3, і видаляється з апарата через патрубок 4. Після насичення адсорбента, яке визначається початком проскакування компонента, що поглинається, проводиться десорбція. Шар адсорбенту прогрівається паром, який надходить через патрубок 5. При цьому з адсорбенту відганяються пари витягнутих речовин, які відводяться через патрубок 6 на конденсацію і наступну переробку. Потім адсорбент сушать гарячим паром і після охолодження повторюють цикл процесу.

 2
2
Рисунок 6.2 – Адсорбер періодичної дії:
1 – штуцер для відведення конденсату; 2 – решітка; 3 – люки для вивантаження адсорбенту; 4 – адсорбент; 5 – штуцер для відведення парів при десорбції; 6 – патрубок для підведення забрудненого газу; 7 – люк для завантаження адсорбенту; 8 – штуцер для відведення очищеного газу та повітря під час регенерації
В промисловості звичайно застосовують установки безперервної дії. Вони складаються з двох і більше описаних вище адсорберів, які почергово включаються для адсорбції газів. Після насичення адсорбенту в першому адсорбері подачу газу переключають на другий, а в першому в цей час проводять десорбцію, сушку і охолодження, після чого його переключають на цикл поглинання, а другий адсорбер – на десорбцію, сушку і охолодження.
В адсорберах безперервної дії (їх називають гіперсорбери) зернистий адсорбент переміщується вертикальною колоною, у верхній частині якої проходить адсорбція, а в нижній – десорбція під дією нагрівання.
Крім гіперсорберів застосовують адсорбери безперервної дії з киплячим шаром адсорбенту (рис. 6.3).
В корпусі 1 одноступеневого адсорбера встановлена розподільна решітка 2, через яку знизу подається газ, що приводить дрібнозернистий адсорбент в стан киплячого шару 3. Адсорбент безперервно надходить зверху і видаляється через трубу 5 на десорбцію.
До промислових адсорбентів висувають такі вимоги: вони повинні бути з великою динамічною ємністю (часом захисної дії), великою питомою поверхнею, вибірністю адсорбції, термічною і механічною стійкістю, здібністю до регенерації, простотою виготовлення, дешевизною.

Адсорбент
 3
3
Адсорбент
Рисунок 6.3 – Адсорбер з киплячим шаром адсорбенту:
1 – циліндричний корпус з конусом знизу; 2 – розподільна решітка;
3 – адсорбент; 4 – патрубок для введення адсорбенту; 5 – пристрій для виведення очищеного газу; 6 – патрубок для виведення адсорбенту; 7 – штуцер для подачі забрудненого газу
Для адсорбційного очищення газів в промисловості частіше всього застосовують такі пористі адсорбенти: активоване вугілля, силікагелі, цеоліти, глинисті матеріали, пористе скло тощо. Всі вони по-різному відповідають перерахованим вимогам і при їх виборі враховують найбільшу активність відносно компонента, який треба вилучити.
Одним із основних параметрів при виборі адсорбенту є адсорбційна здатність до компонента, який вилучається. Адсорбційна здатність або маса речовини а, яка поглинається одиницею маси адсорбенту в довільний момент часу, залежить від концентрації адсорбованої речовини (парціального тиску 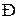 , Па) біля поверхні адсорбента, загальної площі цієї поверхні, фізичних, хімічних та електричних властивостей адсорбованої речовини і адсорбенту, температурних умов та наявності інших домішок.
, Па) біля поверхні адсорбента, загальної площі цієї поверхні, фізичних, хімічних та електричних властивостей адсорбованої речовини і адсорбенту, температурних умов та наявності інших домішок.
Як характеристики адсорбційних властивостей пористих тіл вико-ристовують залежність адсорбційної здатності від парціального тиску газового компонента, який поглинається при постійній температурі (ізотерма адсорбції):
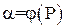 при
при 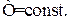
На рис. 6.4 зображені типи ізотерм адсорбції для різних адсорбентів. У всіх випадках адсорбційна здатність сорбенту збільшується при підви-щенні тиску адсорбату, але характер цього збільшення різний. Випукла ізотерма 1 специфічна для адсорбції на дрібнодисперсних сорбентах, які застосовуються для очищення газової суміші при малому парціальному тиску компонентів, які вилучаються, і для осушування. Ізотерма 2 типова для непористих адсорбентів при полімолекулярній фізичній адсорбції. Ізотерма 3 спостерігається на адсорбентах з розвинутою системою великих і середніх пор. Ці сорбенти доцільно застосовувати для вилучення летких газів при парціальному тиску, близькому до тиску насичення.

α (мг/г)
Р (Па)
Рисунок 6.4 – Ізотерми адсорбції
В основі інженерно-технічного розрахунку адсорбційного методу очищення знаходиться сітка кривих, що відображає рівновагу компонента, який поглинається адсорбентом, тобто сітка ізотерм адсорбції 3.
На рис. 6.5 зображені ізотерми адсорбції SO2 на активованому вугіллі СКТ в діапазоні температур від 20 до 150°С. Як видно, зі збільшенням температури відбувається зниження адсорбційної здатності активованого вугілля. На цій властивості адсорбентів заснований процес їх регенерації. Регенерацію здійснюють нагріванням насиченого адсорбенту до температури, вищої за робочу, або продуванням його паром чи гарячим газом.
При проектуванні адсорбера використовують такі початкові дані: об’ємні витрати очищуваного газу G, м3/с, концентрацію домішок, які витягуються С´, мг/м3, і тиск вихідних газів Р, Па. У результаті розрахунку визначають необхідну масу адсорбенту, конструктивні розміри, гідравлічний опір апарата і тривалість захисної дії адсорбера.
α (мг/г)

Р (Па)
Рисунок 6.5 – Ізотерми адсорбції SO2 на активованому вугіллі СКТ
при різних температурах, °С: 1 –20; 2 –50; 3 – 100; 4 – 150
На першому етапі розрахунку і проектування адсорбера вибирають робочу температуру і тип сорбенту. Для збільшення адсорбційної здібності сорбенту робочу температуру, як правило, вибирають мінімально можливою. Вибір типу сорбенту проводиться за ізотермами адсорбції при робочих параметрах температури і концентрації домішок з умови мінімальної маси сорбенту.
Мінімальну необхідну масу сорбенту 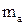 , г/с, визначають з рівняння матеріального балансу за компонентом, який вловлюється:
, г/с, визначають з рівняння матеріального балансу за компонентом, який вловлюється:
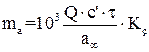 , (6.5)
, (6.5)
де 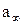 – статична поглинальна здібність адсорбенту в робочих умовах, мг/г адсорбенту;
– статична поглинальна здібність адсорбенту в робочих умовах, мг/г адсорбенту;
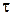
 – час процесу адсорбції, с;
– час процесу адсорбції, с;
 – коефіцієнт запасу рівний 1,1…1,2.
– коефіцієнт запасу рівний 1,1…1,2.
Швидкість потоку газу в адсорбері 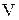 , м/с, розраховують, виходячи з допустимого зменшення тиску
, м/с, розраховують, виходячи з допустимого зменшення тиску 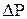 , Па, в адсорбері:
, Па, в адсорбері:
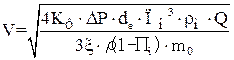 , (6.6)
, (6.6)
де 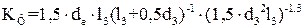 – коефіцієнт форми зерна сорбенту, який враховує нерівномірну доступність всієї поверхні зерна потоку газу;
– коефіцієнт форми зерна сорбенту, який враховує нерівномірну доступність всієї поверхні зерна потоку газу;
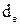 – еквівалентний діаметр зерна сорбенту, м, для циліндричних зерен довжиною
– еквівалентний діаметр зерна сорбенту, м, для циліндричних зерен довжиною 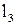 діаметром
діаметром 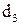 рівний
рівний
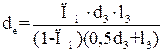 , (6.7)
, (6.7)
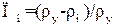 – пористість шару сорбенту визначається через уявну
– пористість шару сорбенту визначається через уявну 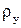 і насипну
і насипну 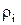 густину сорбенту;
густину сорбенту;
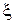 – коефіцієнт гідравлічного опору, який визначається залежно від режиму течії газу: при
– коефіцієнт гідравлічного опору, який визначається залежно від режиму течії газу: при 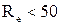
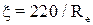 ; при
; при 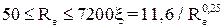 , де
, де 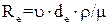 – критерій Рейнольдса. Звичайно, виходячи з умов здійснення необхідного часу контакту газу з сорбентом і мінімальних гідравлічних опорів;
– критерій Рейнольдса. Звичайно, виходячи з умов здійснення необхідного часу контакту газу з сорбентом і мінімальних гідравлічних опорів;
υ – швидкість газу приймається рівною 0,15…0,5 м/с .
Геометричні розміри адсорбера (діаметр 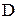 , м, і довжина
, м, і довжина 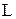 , м, шару адсорбенту) підраховуються за формулами:
, м, шару адсорбенту) підраховуються за формулами:
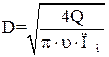 ,
, 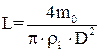 . (6.8)
. (6.8)
Час захисної дії адсорбера визначається, виходячи з характеру кривої ізотерми адсорбції. Для області ізотерми адсорбції, в якій діє закон Генрі 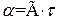 , де
, де 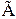 – безрозмірний коефіцієнт Генрі, рівний відношенню кількості адсорбованої речовини α0 до початкової концентрації речовини в газовому потоці
– безрозмірний коефіцієнт Генрі, рівний відношенню кількості адсорбованої речовини α0 до початкової концентрації речовини в газовому потоці 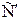 ; тривалість адсорбції
; тривалість адсорбції 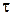 , с, визначають за формулою:
, с, визначають за формулою:
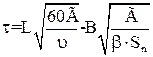 , (6.9)
, (6.9)
де 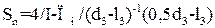 – питома поверхня адсорбенту, м2/м3;
– питома поверхня адсорбенту, м2/м3;
В – коефіцієнт, залежний від співвідношення речовини, яка поглинається в газовому потоці на виході та вході адсорбера (табл. 6.1).
Коефіцієнт масопередачі 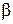 , с–1 визначають залежно від режиму течії газу:
, с–1 визначають залежно від режиму течії газу:
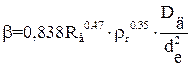 , при
, при 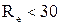 (6.10)
(6.10)
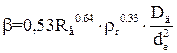 , при
, при 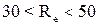 (6.11)
(6.11)
де 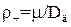 – дифузійний критерій Прандтля;
– дифузійний критерій Прандтля;
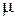 – коефіцієнт динамічної в’язкості газу при робочих умовах, Па·с;
– коефіцієнт динамічної в’язкості газу при робочих умовах, Па·с;
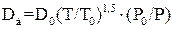 – коефіцієнт дифузії газу, який вловлюється в повітрі, м2/с;
– коефіцієнт дифузії газу, який вловлюється в повітрі, м2/с;
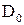 – коефіцієнт дифузії при
– коефіцієнт дифузії при 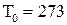 °К і
°К і 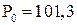 кПа.
кПа.
Таблиця 6.1– Значення коефіцієнтів 
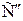 / / 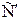
| В | 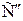 / / 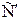
| В | 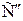 / / 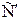
| В |
| 0,005 | 1,84 | 0,1 | 0,94 | 0,5 | 0,07 |
| 0,01 | 1,67 | 0,2 | 0,63 | 0,6 | – 0,10 |
| 0,03 | 1,35 | 0,3 | 0,42 | 0,8 | – 0,27 |
| 0,05 | 1,19 | 0,4 | 0,23 | 0,9 | – 0,68 |
Для області ізотерми адсорбції, в якій дотримується рівняння Ленгмюра: 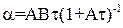 , де А і В – константи, які залежать від властивостей адсорбенту і адсорбованої речовини. Тривалість адсорбції
, де А і В – константи, які залежать від властивостей адсорбенту і адсорбованої речовини. Тривалість адсорбції 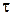 , с, визначається за формулою:
, с, визначається за формулою:
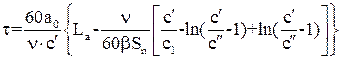 , (6.12)
, (6.12)
де 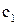 – вміст речовини в газовому потоці, рівноважний з кількістю речовини, рівній половині
– вміст речовини в газовому потоці, рівноважний з кількістю речовини, рівній половині 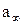 , кг/м3.
, кг/м3.
Для області ізотерми адсорбції, де величина адсорбції практично не залежить від вмісту речовини в газовому потоці (тобто 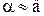 ), тривалість адсорбції
), тривалість адсорбції 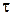 , с, визначають за формулою:
, с, визначають за формулою:
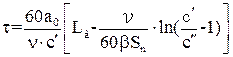 , (6.13)
, (6.13)
Якщо одержаний час захисної дії адсорбера відрізняється від заданого τ на величину 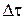 , то довжину апарата
, то довжину апарата 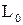 , м, змінюють на величину
, м, змінюють на величину
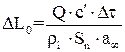 (6.14)
(6.14)
і перераховують масу сорбенту.
Адсорбція ефективна при видаленні великих концентрацій забруднювальних речовин (при цьому необхідна висока адсорбційна ємність або велика маса адсорбенту). В тих випадках, коли концентрації забруднювачів невеликі й обробленню підлягає велика кількість повітря, адсорбція може виявитися ефективною для видалення летких вуглеводнів і органічних розчинників. Цей метод застосовується у випадках, коли необхідна гарантована рекуперація достатньо цінних домішок, коли треба видалити пари отруйних речовин і канцерогенів, які передбачаються.
Адсорбцію широко застосовують при видаленні парів розчинників при фарбуванні, органічних смол і парів розчинників в системі вентиляції підприємств для виробництва скловолокна і склотканин, а також парів ефіру, ацетону та інших розчинників у виробництві нітроцелюлози і бездимного пороху. Адсорбенти також використовують для:
- очищення вихлопних газів автомобілів;
- видалення отруйних компонентів (наприклад, сірководню з газових потоків), які викидаються в атмосферу через лабораторні витяжні шафи;
- видалення радіоактивних газів при експлуатації ядерних реакторів, зокрема радіоактивного йоду.
Дата добавления: 2016-02-02; просмотров: 2163;
