Температура наибольшей плотности и температура замерзания морской воды.
Пресная вода имеет наибольшую плотность при +4 0С и замерзает при 00 С. С повышением солености температура наибольшей плотности (Тмах.плт.) и температура замерзания (Тзамерз.) понижаются почти линейно (рис.2), причем температура наибольшей плотности понижается быстрее, чем температура замерзания. Из графика видно, что при значении солености S =24.695‰ кривые пересекаются, образуя характерную точку, в которой температура замерзания и температура наибольшей плотности равны: Тмах.плт = Тзамерз. = - 1.330 С.
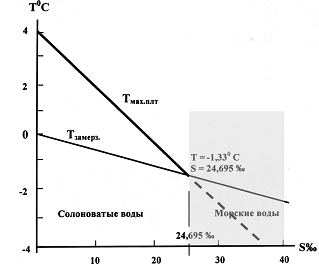
Рис. 2. Температура наибольшей плотности и температура замерзания морской воды.
При солености меньшей 24.695‰ температура наибольшей плотности лежит выше температуры замерзания, как и для пресной воды. Такие воды называют солоноватыми. При солености большей 24.695‰ температура наибольшей плотности лежит ниже температуры замерзания и такая вода никогда не достигает температуры наибольшей плотности, так как замерзает раньше. Воды с соленостью большей 24.695‰ называют морскими. Деление на эти два типа вод - солоноватые и морские было сделано русским океанографом Н. М. Книповичем.
Морские воды в отличие от пресных и солоноватых с понижением температуры всегда увеличивают свою плотность вплоть до замерзания. Эти особенности влекут за собой различия в конвекции, замерзании, тепловом режиме в морских и солоноватых водоемах.
При замерзании морской воды происходит выделение соли из образовавшегося льда, из-за чего соленость незамерзшей воды возрастает. Но с увеличением солености понижается температура замерзания. Следовательно, одной из особенностей льдообразования в морской воде будет то, что этот процесс происходит только при непрерывном понижении температуры. В пресной же воде замерзание происходит при неизменной температуре 00 С.
Вторая особенность льдообразования в морской воде связана с точкой пересечения кривых температуры наибольшей плотности и температуры замерзания. Температура наибольшей плотности воды с соленостью меньше 24.695‰, так же как и пресной воды, лежит выше температуры ее замерзания. Поэтому процесс замерзания развивается в такой воде так же, как в пресной. Осенью начинается общее выхолаживание водоемов. Охлаждается, прежде всего, поверхностный слой, плотность воды которого при этом повышается, и вода с поверхности опускается вниз, а на ее место поднимается более теплая, но менее плотная вода.
Благодаря перемешиванию вся толща воды достигает сначала определенной температуры (гомотермии), равной температуре наибольшей плотности. При дальнейшем охлаждении плотность воды поверхностного слоя начинает уменьшаться и перемешивание прекращается. Для образования льда в воде с соленостью меньше 24.695‰ оказывается достаточным ее охлаждение до температуры замерзания сравнительно тонкого поверхностного слоя.
Температура наибольшей плотности воды с соленостью большей 24.695‰ лежит ниже температуры ее замерзания. При охлаждении такой воды перемешивание во время замерзания не прекращается. Поэтому для образования льда необходимо охладить значительно больший по толщине поверхностный слой, чем при замерзании пресной и солоноватой воды.
Диффузия и осмос
Частицы растворенного вещества в слабых растворах, каким является морская вода, отдалены друг от друга на большие расстояния. Находясь в неупорядоченном движении, они устремляются в сторону наименьшего сопротивления среды. Такой средой является либо чистый растворитель, либо вода с меньшей концентрацией солей. Поэтому, когда соприкасаются два раствора различной концентрации, частицы растворенного вещества начинают переходить из раствора с большей концентрацией в раствор с меньшей концентрацией. Переход будет продолжаться до тех пор, пока концентрации обоих растворов не выровняются.
Переход частиц из слоя в слой, осуществляемый без помощи механического перемешивания, называется молекулярной диффузией.
Основным процессом, определяющим перенос солей и газов в океане в горизонтальном и особенно в вертикальном направлении, является турбулентная диффузия.
С соленостью морской воды связано физическое свойство - осмос, отсутствующее в дистиллированной воде. Это свойство имеет важное биологическое значение, обеспечивая проникновение в морские организмы необходимых им для питания веществ, растворенных в морской воде.
Явление осмоса наблюдается в том случае, когда раствор отделен от растворителя полупроницаемой пленкой, которая пропускает молекулы растворителя, но не пропускает молекулы растворенного вещества. В этом случае молекулы растворителя, стремясь выровнять концентрацию, начинают переходить в раствор, повышая его уровень до положения равновесия. Выравнивание концентраций по обе стороны такой мембраны возможно лишь при односторонней диффузии растворителя. Поэтому выравнивание всегда идёт от чистого растворителя к раствору или от разбавленного раствора к концентрированному. В результате этого создается давление на пленку, называемое осмотическим давлением. Оно равно избыточному внешнему давлению, которое следует приложить со стороны раствора, чтобы прекратить осмос, т. е. создать условия осмотического равновесия.
Осмос имеет важнейшее значение в биологических процессах, его широко используют при определении концентрации растворов, исследовании разнообразных биологических структур. Осмотические явления иногда используются в промышленности, например при получении некоторых полимерных материалов, очистке высоко минерализованной воды, для опреснения морской воды.
Дата добавления: 2016-02-02; просмотров: 1696;
