Чувствительность ВВ к тепловым импульсам
В составе любого ВВ имеются все компоненты, необходимые для протекания реакции. Но в любом ВВ, используемом в промышленности, химические реакции в условиях дневной поверхности протекают с очень малыми скоростями, во многих случаях трудно поддающимися регистрации. Это позволяет длительно хранить ВВ при нормальных условиях.
Зависимость скорости реакции К от температуры вещества и концентраций
[ А] и [В], реагирующих по бимолекулярному закону веществ,определяется уравнением Аррениуса
K = Z [ А][В] exp{ - E/ RT}. ( 1.1)
Под скоростью реакции подразумевается изменение концентраций реагирующих веществ за единицу времени. Концентрации в этом случае принято выражать числом грамм-молекул вещества в одном литре, а время в секундах. Если скорость реакции, например, 0,08 моля в секунду, то это значит, что за секунду концентрация реагирующих веществ уменьшилась на 0,08 моля в литре. Важнейшими факторами, влияющими на скорость реакции являются: концентрация реагирующих веществ, температура и катализаторы, роль которых могут выполнять примеси. Z называется константой скорости реакции и для бимолекулярных реакций при условии: [ А]=[В]=1 моль/ л ;она численно равна скорости реакции.
Для мономолекулярных реакций уравнение (1.1) будет иметь вид
K = Z exp{ - E/ RT}. (1.2)
При этом Z равна числу молей вещества, распавшихся в единицу времени в единице объёма. Величина Z принимается постоянной, что является достаточно условным положением. В уравнении R – газовая постоянная, численно равная работе, совершаемой одним молем идеального газа при изобарном нагревании его на один градус: 8,31 ×103 Дж./ о K ×кмоль. Согласно уравнению (1.2), в реакцию вступают далеко не все молекулы, а только активные, энергия которых превосходит некоторую величину E , характерную для данной реакции. Величину E называют энергией активации. Энергия активации рассчитывается в Дж. на кмоль. Множитель exp{- E/ RT} характеризует относительное число активных молекул в одной килограмм –молекуле (кмоль) вещества.
Вычисление значений Еи Z производится аналитически или эмпирически путём построения графиков зависимости скорости реакции от температуры.
Логарифмируя уравнение Аррениуса для мономолекулярных реакций можем получить связь между ln К и обратной величиной температуры .
ln К 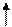
 ln К = ln Z - E/ RT ( 1.3)
ln К = ln Z - E/ RT ( 1.3)
Эта связь выражается прямой линией (рис1).
Тангенс угла a наклона прямой линии к оси абсцисс определяет величину E/R, а отрезок, отсекаемый ею на оси ординат равен ln Z .
1/ Т
Рис. № 1.1 Зависимость скорости
Реакции от температуры
Для оценки меры чувствительности взрывчатых веществ к тепловому импульсу обычно служит  так называемая температура вспышки, которую экспериментально устанавливают при определённых условиях.
так называемая температура вспышки, которую экспериментально устанавливают при определённых условиях.
Температурой вспышки называется температура, Рис.№1.1 Зависимость скорости до которой должно быть нагрето данное количество ВВ для его воспламенения, в процессе которого химическая реакция сопровождается звуковым эффектом. Для обеспечения вспышки необходимо превышение теплопритока, обусловленного протеканием химической реакции над теплопотерями, возникающими вследствие проводимости и радиации тепла.
Таким образом, при нагревании ВВ моменту вспышки предшествует период самоускорения химической реакции. Промежуток времени от начала нагрева до момента вспышки ВВ называется временем задержки вспышки или периодом индукции.
 Из самого определения периода индукции tследует, что он должен быть обратно пропорционален скорости химической реакции К: t @ 1/ К. Используя уравнение
Из самого определения периода индукции tследует, что он должен быть обратно пропорционален скорости химической реакции К: t @ 1/ К. Используя уравнение  Аррениуса можно записать t=С exp{E/ RT}, (где С-постоянная, зависящая от состава ВВ, его количества и начальной температуры ВВ).
Аррениуса можно записать t=С exp{E/ RT}, (где С-постоянная, зависящая от состава ВВ, его количества и начальной температуры ВВ).
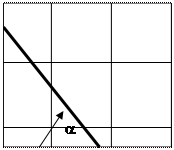
Из этого выражения видно, что с уменьшением энергии активации и увеличением температуры нагрева, период задержки будет уменьшаться. Представляя уравнение в логарифмическом виде: lnt = ln С + E/ RT не трудно увидеть линейную связь между lnt и 1/ Т. На рис. №1.2 представлена зависимость периода задержки вспышки от температуры. На графике тангенс угла b наклона прямой к оси абсцисс равен E/ R. Это позволяет на основе экспериментальных данных по зависимости времени задержки (или периода индукции) вспышки от температуры определить энергию активации.
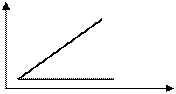
В связи с зависимостью ln С и самой энергии активации E от температуры, изображённая на рис. №1.2 прямая в разных температурных диапазонах будет иметь различные углы наклона и отсекать на оси ординат различные отрезки. На рис. №1.3 приведены зависимости периода индукции вспышки от температуры для азида бария и азида свинца. Верхние прямые на рисунке отвечают более низким температурам. На угол наклона нижних прямых определяющее влияние оказывают процессы разложения ВВ при высоких температурах.
lnτ 5

| 
| |||
| PbN6 | ВаN6 | |||
| PbN6 | ВаN6 | |||
150 170 190 105
 T
T
666 600 525 T
Рис.№1.3 Зависимость времени задержки вспышки
Следует учитывать, что энергия активации может зависеть от температуры ещё более сложным образом. Так у нитроглицерина с повышением температуры энергия активациивозрастает. Это же относится и к пироксилину. Очевидно, что такие эффекты связаны с изменением самого характера течения реакций разложения и, прежде всего, состава продуктов реакции с повышением температуры. Факт изменения состава продуктов реакции с изменением температурного диапазона установлен многими исследователями. Однако, результаты экспериментов не подвергались детальному анализу. По-видимому, с изменением состава газа меняется сущность самой физики процесса вспышки. И если при одном составе продуктов разложения возможен сток энергии из большого объёма ВВ и концентрация её вплоть до вспышки, то при другом составе продуктов такой процесс исключён и вспышка может происходить только при высоких температурах.
Для определения температуры вспышки конденсированных ВВ наиболее широкое применение нашли два следующих метода:
1.Определённое количество ВВ, начиная с некоторой температуры нагревают с постоянной скоростью. При этом фиксируют температуру при которой происходит вспышка. Метод применяют при практических испытаниях взрывчатых веществ.
2.Второй метод заключается в установлении зависимости изменения времени задержки от температуры. На основании экспериментальных данных строится зависимость, аналогичная изображённой на рисунке №1.4 .Этот метод, позволяет более точно полно характеризовать отношение
ВВ к тепловому 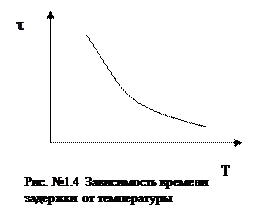 импульсу. Для каждого ВВ, при соответствующих условиях опыта, существует некоторая температура, ниже которой вспышка вообще не происходит, как бы долго мы его не нагревали.
импульсу. Для каждого ВВ, при соответствующих условиях опыта, существует некоторая температура, ниже которой вспышка вообще не происходит, как бы долго мы его не нагревали.
Минимальные температуры вспышки ВВ представляют интерес, главным образом с точки зрения вопросов, связанных с техникой безопасности при хранении больших масс ВВ
Во многих случаях практического использования ВВ инициирование взрыва осуществляется весьма кратковременными тепловыми импульсами, для которых время задержки не превосходит тысячных или даже десятитысячных долей секунды.Процессы взрыва могут быть иногда также обусловлены быстрыми (τ≤100 мкс) местными разогревами ВВ при пропускании тока конденсаторного разряда через тонкие металлические нити.
Экспериментально установленные минимальные температуры вспышки некоторых ВВ приводятся в таблице №1.2.
Таблица №1.2
Температуры вспышки некоторых ВВ.
| Название ВВ | Температура вспышки, С | Название ВВ | Температура вспышки, С |
| Гремучая ртуть | 175 - 180 | Тетрил | 190 - 200 |
| Азид свинца | 315 - 330 | Гексоген | 225 - 235 |
| Азид серебра | 310 - 320 | Тэн | 210 -220 |
| Стифнат свинца | 270 - 280 | Ксилол | 315 - 330 |
| Пироксилин | 185 - 195 | Аммотол | |
| Нитроглицерин | 200 - 205 | Бездымные пороха | 180 - 200 |
| Тротил | 300 - 310 | Дымные пороха | 290 - 310 |
Для определения температуры вспышки ВВ пользуются приборами различной конструкции. Чаще всего испытания производятся в приборе, схема которого приведена на рис. №1.5. Основными деталями прибора являются: металлическая цилиндрическая баня – а, наполненная сплавом Вуда. Обогрев бани производится электрическим током, проходящим через обмотку из нихрома. Обмотка изолирована от поверхности бани керамической изоляцией. Для уменьшения теплоотдачи и удобства работы баня укреплена в латунном футляре - б. Сверху баня закрывается металлической крышкой – в с отверстиями; через центральное отверстие проходит термометр, погружённый в сплав и защищённый от действия взрыва металлической гильзой ; другие отверстия – г служат для опускания в баню специальных гильз с ВВ. Навеска обычно равна 0,05г.
Определение производится по одному из методов, описанных выше. Для того чтобы судить о предельных условиях возбуждения взрыва необходимо прежде всего знать температуры термического воспламенения соответствующих ВВ при очень в коротких периодах задержки, характерных для передачи теплового импульса от капсюля воспламенителя капсюлю – детонатору. В то же время экспериментально установленные температуры вспышки отвечают значительно более длительным периодам задержки.
г

 в
в
б
а
Весьма приблизительное представление о порядке интересующих температур можно получить путём экстраполяции экспериментальных данных на очень короткие промежутки времени. При этом к принципиальным недостаткам такой экстраполяции следует отнести:
1) отсутствие учёта изменения самого характера химического разложения ВВ при переходе от низких температур к более высоким;
2) отсутствие контроля за составом продуктов разложения и их энергетическим состоянием;
3) исключение возможности протекания процессов концентрации энергии внутри объёма продуктов реакции при высоких температурах.
Дата добавления: 2016-02-02; просмотров: 1287;
