Энергетические ресурсы → ΔμI → работа
где ΔμI – трансмембранная разность электрохимических потенциалов иона I. Следовательно, процессы утилизации энергии и совершения за счет нее работы оказываются сопряжены через образование и использование ΔμI. Поэтому данный ион может быть назван сопрягающим ионом. Основным сопрягающим ионом в клетке эукариот является Н+, и соответственно ΔμН+ является основной конвертируемой формой запасания энергии. Вторым по значимости сопрягающим ионом является Na+ (ΔμNa+). В то время как Сa2+, K+ и Cl‑ не используются для совершения какой‑либо работы.
Биологическое окисление – это процесс дегидрирования субстрата с помощью промежуточных переносчиков водорода и его конечного акцептора. Если в роли конечного акцептора выступает кислород, процесс называется аэробным окислением или тканевым дыханием, если конечный акцептор представлен не кислородом – анаэробным окислением. Анаэробное окисление имеет ограниченное значение в организме человека. Основная функция биологического окисления – обеспечение клетки энергией в доступной форме.
Тканевое дыхание – процесс окисления водорода кислородом до воды ферментами цепи тканевого дыхания. Оно протекает по следующей схеме:
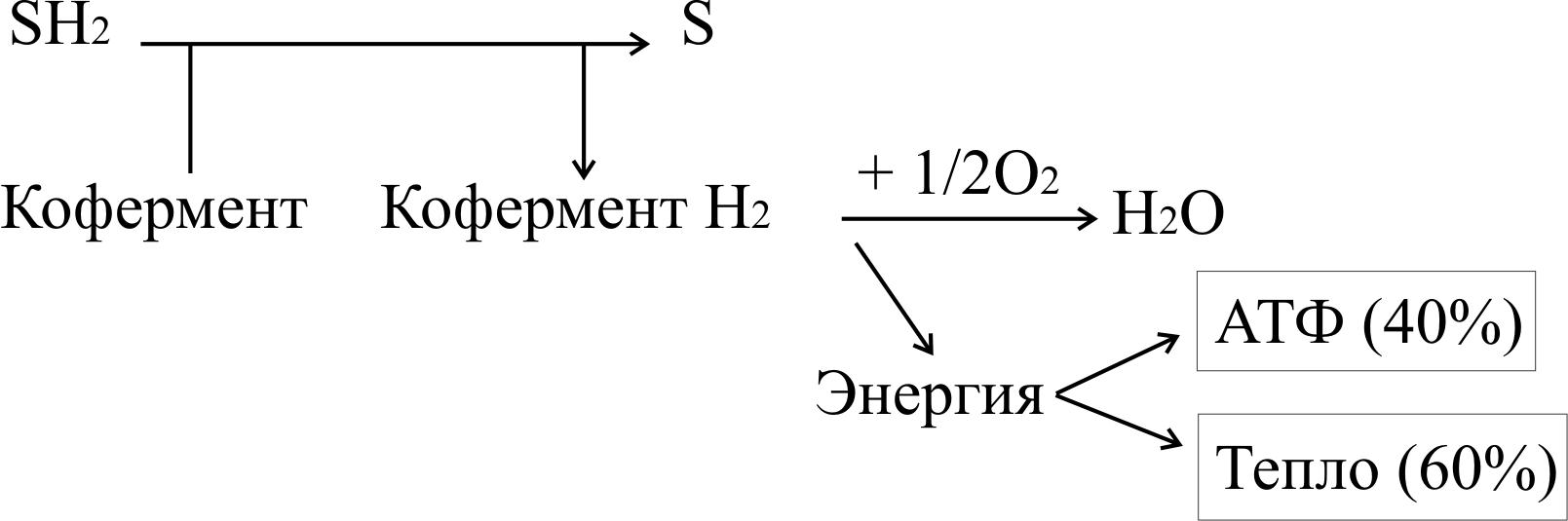
Вещество окисляется, если отдает электроны или одновременно электроны и протоны (атомы водорода), или присоединяет кислород. Способность молекулы отдавать электроны другой молекуле определяется окислительно‑восстановительным потенциалом (редокс‑потенциалом). Любое соединение может отдавать электроны только веществу с более высоким окислительно‑восстановительным потенциалом. Окислитель и восстановитель всегда образуют сопряженную пару.
Выделяют 2 типа окисляемых субстратов:
1. Пиридинзависимые – спиртовые или альдегидные – изоцитрат, α‑кетоглутарат, пируват, малат, глутамат, β‑гидроксиацил‑КоА, β‑гидроксибутират, – в их дегидрировании участвуют НАД‑зависимые дегидрогеназы.
2. флавинзависимые – являются производными углеводородов – сукцинат, ацил‑КоА, глицерол‑3‑фосфат, холин – при дегидрировании передают водород на ФАД‑зависимые дегидрогеназы.
Цепь тканевого дыхания – последовательность переносчиков протонов водорода (Н+) и электронов от окисляемого субстрата на кислород, локализованных на внутренней мембране митохондрий.
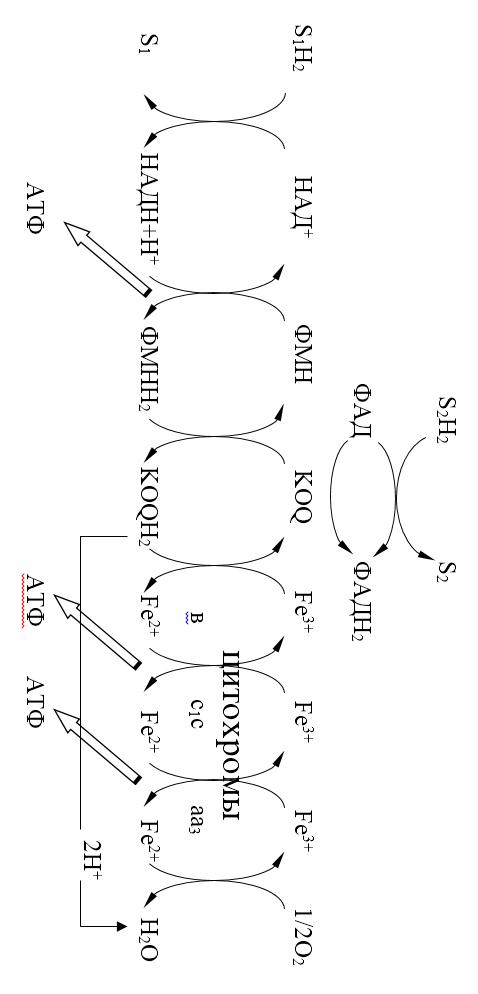
Рис. 10.1. Схема ЦТД
Компоненты ЦТД:
1. НАД‑зависимые дегидрогеназы дегидрируют пиридинзависимые субстраты и акцептируют 2ē и один Н+.
2. ФАД (ФМН) ‑ зависимые дегидрогеназы акцептируют 2 атома водорода (2Н+ и 2ē). ФМН – зависимая дегидрогеназа дегидрирует только НАДН, в то время как ФАД‑дегидрогеназы окисляют флавинзависимые субстраты.
3. Жирорастворимый переносчик убихинон (кофермент Q, КоQ) – свободно перемещается по мембране митохондрий и акцептирует два атома водорода и превращается в КоQH2 (восстановленная форма – убихинол).
4. Система цитохромов – переносит только электроны. Цитохромы железосодержащие белки, простетическая группа которых по структуре напоминает гем. В отличие от гема атом железа в цитохроме может обратимо переходить из двух – в трехвалентное состояние (Fe3+ + ē → Fe2+). Это и обеспечивает участие цитохрома в транспорте электронов. Цитохромы действуют в порядке возрастания их редокс‑потенциала и в дыхательной цепи располагаются следующим образом: b‑с1‑с‑а‑а3. Два последних работают в ассоциации как один фермент цитохромоксидаза аа3. Цитохромоксидаза состоит из 6 субъединиц (2 ‑ цитохрома а и 4 ‑ цитохрома а3). В цитохроме а3 кроме железа имеются атомы меди и он передает электроны непосредственно на кислород. Атом кислорода при этом заряжается отрицательно и приобретает способность взаимодействовать с протонами с образованием метаболической воды.
Железосерные белки (FeS) – содержат негемовое железо и участвуют в окислительно‑восстановительных процессах, протекающих по одноэлектронному механизму и ассоциированы с флавопротеинами и цитохромом b.
Дата добавления: 2016-01-30; просмотров: 984;
