Генная терапия онкологических заболеваний.
Несмотря на широкое применение хирургических методов лечения, лучевой и химотерапии, злокачественные новообразования по-прежнему остаются одной из основных причин смерти людей, поэтому задача разработки новых способов их лечения является весьма актуальной. Одним из таких перспективных способов является уничтожение пролиферирующих опухолевых клеток с помощью препарата ганцикловира [GCV; 9-(1,3-дигидрокси-2-пропоксиметил) гуанина], который, будучи сам неактивным (пролекарство), преходит в активную форму под действием тимидинкиназы вируса простого герпеса (HSVtk). Для этого предварительно проводят in vivo трансфекцию опухолевых клеток вирусом простого герпеса и через несколько дней вводят ганцикловир. Вирусная тимидинкиназа фосфорилирует ганцикловир с образованием ганцикловир-монофосфата. Киназы клетки-хозяина (опухоли) не фосфорилируют ганцикловир, зато охотно присоединяют фосфатные группы к его монофосфату с образованием ганцикловир-трифосфата, который ингибирует ДНК-полимеразу и останавливает синтез ДНК, вызывая гибель пролиферирующих клеток. Кроме того, через межклеточные контакты ганцикловиртрифосфат может проникать в нетрансфицированные опухолевые клетки, приводя и к их гибели. Одна экспрессирующая ген HSVtkопухолевая клетка может уничтожить до 10 немодифицированных клеток. Это явление называется «эффектом свидетеля»,а ген, вызывающий при определенных условиях гибель собственной клетки, называют геном «самоубийства
Эффективность системы GCV-HSVtk; доказана целым рядом доклини-ческих испытаний. Однако I фаза ее клинических испытаний, в которых участвовали больные с терминальной стадией рака, не показала регресса опухоли. Возможно, ген HSV/tk; был трансдуцирован (введен) в слишком малое число опухолевых клеток и, несмотря на «эффект свидетеля», не мог подавить рост опухоли. В настоящее время разрабатываются новые подходы, которые смогут повысить частоту трансдукции и доставить ген HSV/tk в клетки по всему объему опухоли.
Для генной терапии рака разработаны также комбинированные подходы, использующие две разные системы генов. В одном из них сочетаются GCV-HSVtk-терапия и генная иммунотерапия (рис.1 ). Одну часть опухолевых клеток трансдуцируют геном HSVtk, другую - клонированной кДНК (или геном) одного из цитокинов. Цитокины (интерлейкин-2, интерлейкин-12 и другие) играют роль сигнала, мобилизующего клетки иммунной системы и стимулирующего иммунный ответ. Показано, что опухолевые белки, которые высвобождаются из клетки, уничтоженной в результате терапии с помощью гена «самоубийства», взаимодействуют с иммунными клетками, привлекаемыми к месту локализации опухоли цитокином, и запускают противоопухолевую иммунную реакцию. Кроме того, противоопухолевые антитела, поступая в кровоток и циркулируя по всему организму, предотвращают появление метастазов.
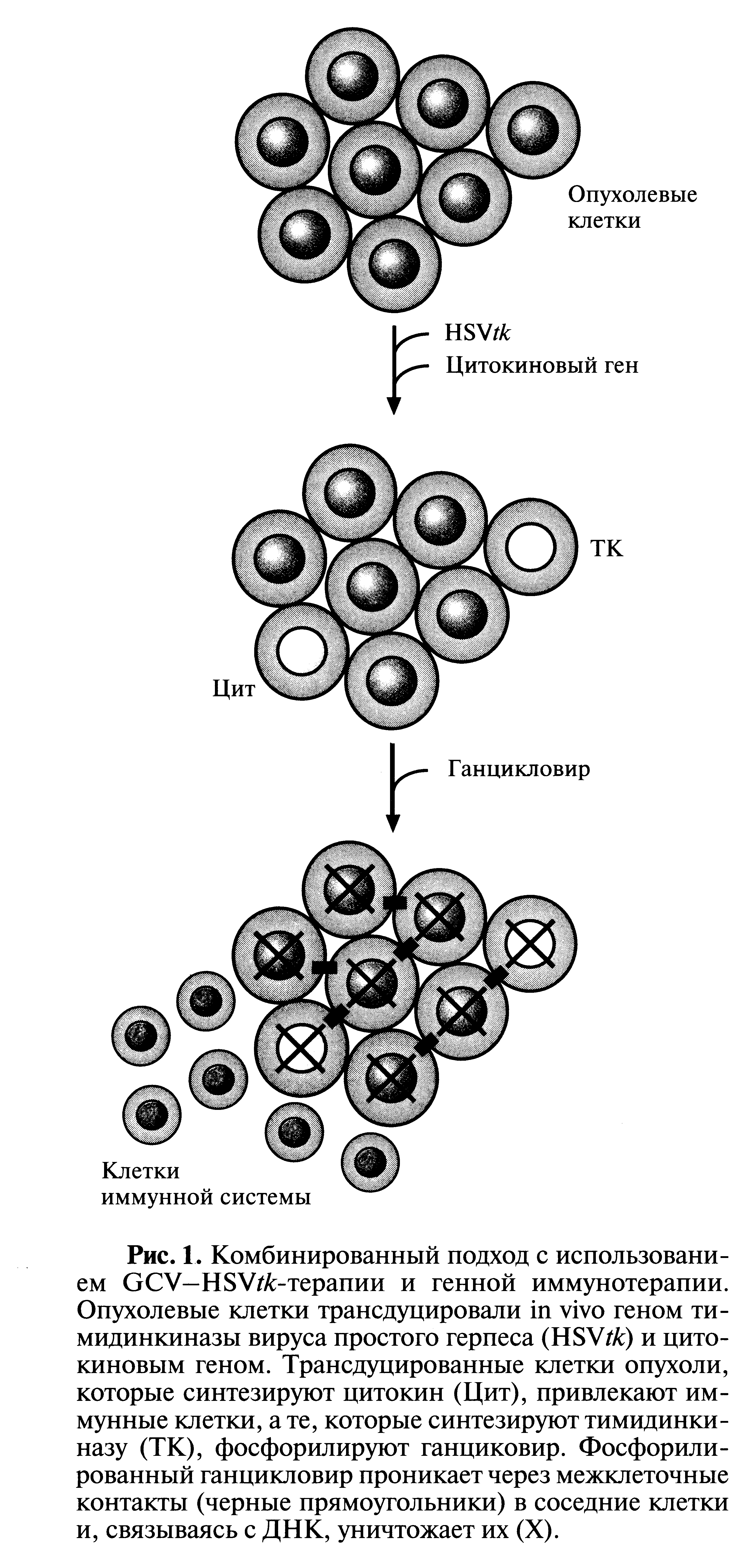
Этот подход к генной терапии рака был проверен экспериментально: в печень животных имплантировали клетки рака толстой кишки, раздельно трансдуцированные генами HSVtk одного из цитокинов. Введение ганцикловира останавливало рост опухоли в печени. Опухоль не возникала и при введении нетрансдуцированных опухолевых клеток в другие ткани такого животного. У контрольных животных в аналогичных условиях происходило развитие опухолей во всех местах введения нетрансдуцированных клеток рака толстой кишки. Несмотря на столь многообещающие результаты, прежде чем приступать к клиническим испытаниям терапии с использованием гена «самоубийства» или различных комбинаций генной терапии, необходимо установить, какие опухоли будут поддаваться такому лечению и не вызовет ли оно побочных эффектов.
Дата добавления: 2016-01-30; просмотров: 1146;
