Причина многообразия и ее следствия
Атомы этого элемента чрезвычайно легко могут образовывать цепи, выстраиваться в длинную шеренгу.
Самая короткая цепь содержит два углеродных атома, Например, молекула углеводорода этана насчитывает два звена в цепочке: Н3С–СН3. Самая длинная? Пока это не известно. Удалось получить соединение, где в цепи располагается 70 углеродных звеньев. (Нужно оговориться, что речь идет об обыкновенных соединениях, а не о полимерах. Там углеродные цепи имеют протяженность значительно большую.)
Ничего подобного мы не встретим у других элементов. Только кремний может позволить себе роскошь образовать шестизвенную цепочку. Да для германия ученые получили любопытное соединение – германоводород Ge3H8, где три металлических атома находятся в одной цепи. В семействе металлов это вообще единственный случай.
Словом, по способности к «цепеобразованию» углерод вне всякой конкуренции.

Но если бы углеродные цепочки были только линейные, органическая химия не знала бы столь баснословного количества соединений.
Цепи могут ветвиться. Могут замыкаться, образуя циклы – многоугольники. Из трех, четырех, пяти, шести и более атомов углерода.
В углеводороде бутане цепочка из четырех углеродных атомов:
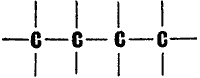
Здесь атомы вытянуты «по струнке». Но они могут разместиться и так:
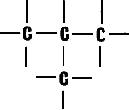
Число атомов то же самое, но связаны они друг с другом по‑иному. И само вещество имеет другие свойства и называется иначе – изобутан. Короче: «Федот, да не тот».
Из пяти углеродных атомов, помимо линейной, можно сконструировать еще пять разветвленных цепей. Каждой «конструкции» будет отвечать самостоятельное химическое вещество.
Для таких разновидностей химических соединений, в которых содержатся одни и те же атомы, правда расположенные различными способами, химики придумали специальное название – изомеры. Их тем больше, чем больше атомов углерода в молекуле. Количество изомеров растет чуть ли не в геометрической прогрессии.
А органическая химия зачисляет в свой актив сотни тысяч новых соединений.
Химические кольца
Ходит немало легенд о том, как великие ученые делали свои великие открытия.
Рассказывали, что Ньютон предавался однажды раздумью в своем саду. К ногам его вдруг упало яблоко. Это навело гениального физика на мысль о законе всемирного тяготения.
Говорили, что Менделеев увидел периодическую систему во сне. Так что ему оставалось только проснуться и изобразить свое «сновидение» на бумаге.
Словом, об открытиях и их авторах измышлялось всякое.
Но идея, пришедшая в голову знаменитого немецкого химика Кекуле, была действительно навеяна довольно‑таки любопытной картиной.
Ученые уже давно знали о бензоле – одном из важнейших органических соединений. Знали, что он состоит из шести атомов углерода и шести атомов водорода. Изучили многие его реакции.
И не ведали главного: как шестерка углеродных атомов располагается в пространстве.
Эта проблема не давала покоя Кекуле. А решил он ее так. Впрочем, дадим ему слово: «Я сидел и писал учебник, но работа не двигалась. Мысли мои витали где‑то далеко. Атомы прыгали перед моими глазами. Мой умственный взор мог различить длинные ряды, извивающиеся подобно змеям. Но смотрите! Одна из змей схватила свой собственный хвост и в таком виде, как бы дразня, завертелась перед моими глазами. Как будто вспышка молнии разбудила меня…»

Случайный образ, возникший в сознании Кекуле, помог ему сделать вывод: углеродные цепи способны замыкаться, образовывать циклы.
Вслед за Кекуле химики стали изображать строение бензола следующим образом:
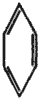
Бензольное кольцо сыграло в органической химии колоссальную роль.
Кольца могут содержать разные количества углеродных атомов. Кольца могут и сращиваться, образуя причудливые геометрические фигуры. В мире колец существует такое же разнообразие конструкций, как и среди незамкнутых цепей атомов углерода. Любая книга по органической химии чем‑то напоминает учебник геометрии, ибо чуть ли не на каждой ее странице встретишь «геометрические фигуры» – структурные формулы сложных органических соединений.
Вот какие занятные «гармошки» могут образовывать бензольные кольца:
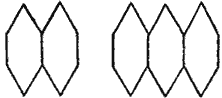
Левая «гармошка» – структурная формула нафталина. Правая – это антрацен, он содержится в каменном угле.
Третья возможность
Считалось, что элемент углерод един в трех лицах. Ученые это «триединство» именовали так: аллотропия. Иными словами, один и тот же элемент может существовать в трех аллотропных модификациях.
Три лица углерода – алмаз, графит и сажа. Они весьма не похожи друг на друга: «король твердости» алмаз, мягкие шелушащиеся чешуйки графита и матово‑черный порошок сажи. Причина такого различия – неодинаковое расположение углеродных атомов в молекуле.

У алмаза они лежат в вершинах геометрической фигуры, именуемой тетраэдром. Атомы связаны здесь чрезвычайно прочно. Потому алмаз и отличается небывалой твердостью.
Атомы углерода в графите, напротив, имеют плоскостное расположение. Отдельные же плоскости связаны между собой довольно слабо. Благодаря этому графит мягок и легко расслаивается на чешуйки.
О строении сажи много спорили. Долгое время господствовало мнение, что сажа не является кристаллическим веществом. Ее рассматривали как аморфную разновидность углерода. И вот сравнительно недавно выяснилось: графит и сажа практически одно и то же. Их молекулярное устройство одинаково. Итак, остались алмаз и графит. Третьего не дано.
Ученые, однако, задались целью искусственно создать третью разновидность углерода. Задача формулировалась следующим образом.
В алмазе и графите цепочки атомов углерода замкнутые, хотя и по‑разному расположены в пространстве. Но нельзя ли заставить углеродные атомы вытянуться в длинную линейную цепочку? Иными словами, нельзя ли получить полимерную молекулу, состоящую только из углеродов, расположенных на одной прямой?
Для изготовления любого химического продукта требуется исходное сырье. Для получения «углерода номер 3» выбор такого сырья однозначен.
Начальным продуктом может быть только ацетилен – соединение двух атомов углерода и двух атомов водорода, С2Н2.
Почему ацетилен? Да потому, что в его молекуле с атомами углерода связано наименьшее из возможных количество водородных атомов. А лишние водороды оказались бы помехой для синтеза.
У ацетилена есть еще одна особенность: он, как говорят химики, весьма реакционноспособен. Атомы углерода связаны в его молекуле тремя химическими связями (Н–С 
С–Н), причем две из них сравнительно легко разрываются и могут быть использованы на соединение с атомами других молекул, например, того же ацетилена.
Итак, первый шаг задуманного: из мономера – ацетилена приготовить полимер – полиацетилен.
Попытка эта не первая. Еще в прошлом веке немецкий химик Байер пытался провести такую реакцию. Но единственно, чего достиг, – получил учетверенную молекулу ацетилена – тетраацетилен. Однако она оказалась феноменально непрочной. Этим путем шли и другие химики разных стран. Увы, результаты их работ приносили лишь разочарование.
Только могущественные методы органического синтеза наших дней позволили, наконец, получить полиацетилен. Его родиной стал Советский Союз. Наши ученые создали новый класс органических соединений, так называемые полиины. Новорожденные вещества сразу нашли практическое применение, оказавшись превосходными полупроводниками.
Теперь предстоял второй шаг на пути к синтезу третьей разновидности углерода: изгнание из молекулы полиацетилена атомов водорода. Так, чтобы сохранилась цепочка из одних углеродов.
Процесс, с помощью которого хотели выгнать водородные атомы, на языке химиков носит длинное и нудное название – окислительная дегидрополиконденсация. Не будем вдаваться в объяснение сути процесса. В лабораторных дневниках его описание заняло десятки страниц, ибо освободить полиацетилен от водорода оказалось весьма непросто. Многие опыты кончались неудачей.
И все‑таки советские ученые достигли блестящего успеха!
…Невзрачный, напоминающий сажу, черный порошок. Химический анализ показал: на 99 процентов он состоит из чистого углерода. На девяносто девять, но пока еще не на все сто.
Собственно, на пути к полной победе предстоит сделать еще один шаг. Нужно избавиться от этого пресловутого процента водорода. Именно он мешает углеродным атомам собраться в едином ровном строю, вытянуться в параллельные цепочки. Именно он последнее препятствие на пути к «углероду номер 3».
Синтезированную «почти третью» разновидность углерода химики назвали карбином. Он уже продемонстрировал свои удивительные способности. Прекрасный полупроводник, обладает фотоэлектрическими свойствами и потрясающе устойчив к нагреванию: полторы тысячи градусов для него ничто!
И мы уверены, недалеко время, когда «стопроцентный» карбин станет реальностью.
Дата добавления: 2016-01-26; просмотров: 755;
