Посевы крови на стерильность 1 страница
Результаты микробиологического исследования крови являются решающими в подтверждении диагноза инфекционного эндокардита и выборе адекватной антибактериальной терапии. Для получения достоверных результатов, прежде всего, необходим правильный забор крови, который предполагает соблюдение следующих принципов:
· забор крови должен проводиться до начала антибактериальной терапии или (если позволяет состояние больного) после кратковременной отмены антибиотиков;
· забор крови осуществляют с соблюдением правил асептики и антисептики только путем пункции вены или артерии и с использованием специальных систем;
· полученный образец крови должен быть немедленно доставлен в лабораторию.
Техника забора крови. При проведении забора крови для микробиологического исследования следует, прежде всего, избегать контаминации обычной кожной флорой. С этой целью:
· в области пункции сосуда производится двукратная обработка поля антисептиком (2%) раствором йода, 70% спиртом или другим антисептиком); обработка кожи проводится круговыми движениями от центра к периферии;
· пальпировать вену в месте пункции следует только в стерильных перчатках; необходимо избегать повторного касания иглой кожи;
· для забора крови используют стерильные шприцы объемом 10–20 мл или специальные устройства (вакуумные флаконы);
· из вены берут 5–10 мл венозной крови в 2 флакона с питательными средами и немедленно отправляют их в лабораторию.
При остром инфекционном эндокардите, когда следует немедленно начинать антибактериальную терапию, кровь берут троекратно с интервалом в 30 мин. При подостром инфекционном эндокардите также проводится троекратный забор крови в течение 24 ч. Если в течение 48–72 ч не получен рост флоры, рекомендуется произвести посев еще 2–3 раза.
Электрокардиография
Изменения ЭКГ при инфекционном эндокардите неспецифичны. При возникновении миокардита (диффузного или очагового) могут выявляться признаки АВ-блокады, сглаженность или инверсия зубца Т, депрессия сегмента RS–Т.
Тромбоэмболия в коронарные артерии сопровождается характерными ЭКГ-признаками ИМ (патологический зубец Q, изменения сегмента RS–Т и др.) (см. главу 14).
Эхокардиография
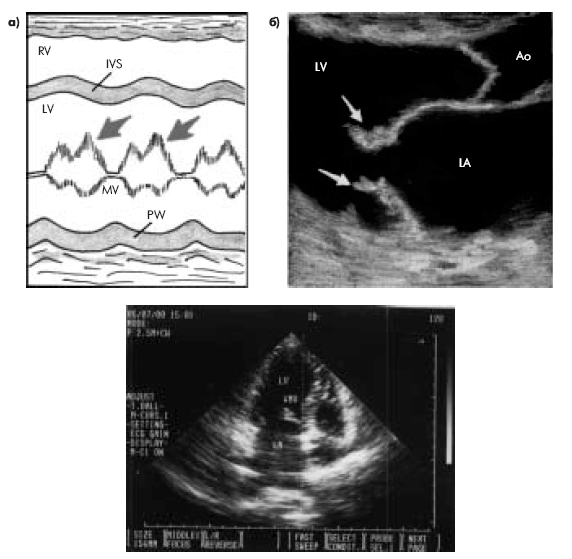
Эхокардиографическое исследование клапанного аппарата при инфекционном эндокардите имеет важное практическое значение, поскольку во многих случаях оно позволяет выявить прямые признаки этого заболевания — вегетации на клапанах, если их размеры превышают 2–3 мм. Большей информативностью (около 70–80%) в данном случае обладает М-модальное исследование. Отличаясь более высокой разрешающей способностью, оно позволяет обнаружить низкоамплитудные высокочастотные систолические вибрации, связанные с повреждением створок клапанов. Вегетации обнаруживаются в виде множества дополнительных эхосигналов, как бы «размывающих» изображение движущихся створок клапана («лохматые» створки) (рис. 9.8, а).
|
| Рис. 9.8. Эхокардиографические признаки вегетаций на створках митрального клапана: а-одномерная эхокардиограмма(схема); б-двухмерная эхокардиограмма (фрагмент); в-двухмерная эхокардиограмма из апикальной позиции четырехкамерного сердца |
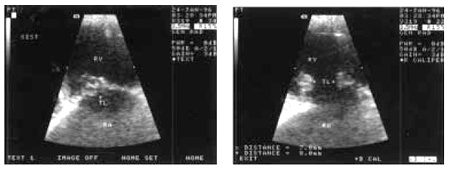
Двухмерная эхокардиография позволяет не только визуализировать вегетации, но и оценить их форму, величину и подвижность (рис. 9.8, б, в). Подвижные вегетации имеют обычно несколько вытянутую форму. Одним своим концом они прикрепляются к створкам, а другой конец свободно перемещается с током крови, как бы независимо от движения самих створок. Например, при поражении трехстворчатого клапана вегетации то всплывают в полости ПП (в систолу), то появляются в полости ПЖ (в диастолу) (рис. 9.9).
Неподвижные вегетации представляют собой небольшие утолщения на створках клапана, которые относительно прочно связаны с ними и полностью повторяют движения створок.
Одним из тяжелых осложнений инфекционного эндокардита является разрыв сухожильных нитей митрального клапана, что вызывает патологическое движение соответствующей створки. Разрыв хорд задней или передней створки сопровождается хаотичными крупноамплитудными колебаниями створок и систолическим пролабированием их в полость ЛП. При двухмерной эхокардиографии иногда можно непосредственно визуализировать разорванные хорды, свободно перемещающиеся в полости ЛЖ.
|
| Рис. 9.9. Подвижные вегетации на створках трикуспидального клапана: а-систола; б-диастола (вегетации обращены в полость правого желудочка) |
| 9.5. Критерии диагностики инфекционного эндокардита |
Диагноз инфекционного эндокардита основывается на выявлении нескольких ведущих признаков:
· лихорадка выше 38°C;
· относительно быстрое формирование недостаточности аортального, митрального или трикуспидального клапанов;
· наличие сопутствующих иммунных поражений (гломерулонефрит, миокардит, узелки Ослера, геморрагии, пятна Лукина и др.);
· эхокардиографическое выявление вегетаций на створках клапанов или признаки «нового» порока сердца;
· положительные результаты посева крови на стерильность;
· анемия, лейкоцитоз с нейтрофилезом, увеличение СОЭ;
· увеличение селезенки и др.
Диагностическое значение каждого из перечисленных признаков неодинаково. Поэтому для правильной и своевременной диагностики инфекционного эндокардита необходим анализ всей клинической картины заболевания, анамнестических данных, результатов лабораторных и инструментальных методов исследования.
В прошлом классическими признаками инфекционного эндокардита считалась триада симптомов: лихорадка, анемия, шум. В настоящее время наибольшее распространение в клинической практике получили так называемые Duke-критерии диагностики инфекционного эндокардита, отражающие современные возможности диагностики этого заболевания (табл. 9.2).
Таблица 9.2
Duke-критерии диагностики инфекционного эндокардита (в модификации)
| Большие критерии |
| 1. Положительные результаты посева крови А. Наличие в двух отдельных пробах крови одного из типичных возбудителей инфекционного эндокардита: · S. viridans · S. bovis · Группы HACEK · S. aureus · Энтерококки Б. Стойкая бактериемия (независимо от выявленного возбудителя), определяемая: · или в двух и более пробах крови, взятых с интервалом 12 ч, · или в трех и более пробах крови, взятых с интервалом не менее 1 ч между первой и последней пробами |
| 2. Эхокардиографические признаки поражения эндокарда А. ЭхоКГ-изменения, характерные для инфекционного эндокардита: · подвижные вегетации · абсцесс фиброзного кольца · новое повреждение искусственного клапана Б. Развитие недостаточности клапана (по данным ЭхоКГ) |
| Малые критерии |
| 1. Наличие заболевания сердца, предрасполагающего к развитию инфекционного эндокардита, или внутривенное введение наркотиков 2. Лихорадка выше 38°С 3. Сосудистые осложнения (эмболии крупных артерий, септический инфаркт легкого, микотические аневризмы, внутричерепное кровоизлияние, кровоизлияния в конъюнктиву) 4. Иммунные проявления (гломерулонефрит, узелки Ослера, пятна Рота, ревматоидный фактор) 5. Микробиологические данные (положительные результаты посева крови, не соответствующие основному критерию, или серологические признаки активной инфекции микроорганизмом, способным вызвать инфекционный эндокардит) 6. Эхокардиографические данные (соответствующие диагнозу инфекционного эндокардита, но не отвечающие основному критерию) |
Диагноз инфекционного эндокардита считается установленным, если присутствуют:
· 2 больших критерия или
· 1 большой и 3 малых критерия или
· 5 малых критериев.
| 9.6. Лечение |
Лечение больных инфекционным эндокардитом проводится в стационаре с соблюдением следующих основных принципов (М.А. Гуревич с соавт.):
1. Лечение должно быть этиотропным, т.е. направленным на конкретного возбудителя.
2. Для лечения следует применять только такие антибактериальные препараты, которые обладают бактерицидным действием.
3. Терапия инфекционного эндокардита должна быть непрерывной и продолжительной:
· при стрептококковой инфекции — не менее 4-х недель;
· при стафилококковой инфекции — не менее 6 недель;
· при грамотрицательной флоре — не менее 8 недель.
4. Лечение должно предусматривать создание высокой концентрации антибиотиков в сосудистом русле и вегетациях (предпочтительно внутривенное капельное введение антибиотиков).
5. Критериями прекращения лечения антибиотиками следует считать сочетание нескольких эффектов:
· полная нормализация температуры тела;
· нормализация лабораторных показателей (исчезновение лейкоцитоза, нейтрофилеза, анемии, отчетливая тенденция к снижению СОЭ);
· отрицательные результаты бактериального исследования крови;
· исчезновение клинических проявлений активности заболевания.
6. При нарастании признаков иммунопатологических реакций (гломерулонефрит, артриты, миокардит, васкулит) целесообразно применение:
· глюкокортикоидов (преднизолон не более 15–20 мг в сутки);
· антиагрегантов;
· гипериммунной плазмы;
· иммуноглобулина человека;
· плазмафереза и др.
7. При неэффективности консервативного лечения в течение 4-х недель и/или наличия других показаний (см. ниже) показано хирургическое лечение.
| 9.6.1. Антибактериальная терапия |
Несмотря на создание в последние годы большого количества высокоэффективных антибиотиков и химиопрепаратов, лечение инфекционного эндокардита остается чрезвычайно сложной задачей. Это обусловлено увеличивающейся частотой высевания высоковирулентных штаммов возбудителей (стафилококк, синегнойная палочка, грамотрицательные микроорганизмы группы НАСЕК), резистентных к антибактериальной терапии, снижением иммунологической резистентности большинства больных, увеличением числа больных пожилого и старческого возраста и другими причинами.
Кроме того, эффект антибактериальной терапии во многом определяется тем, насколько создаваемая в крови концентрация антибиотиков достаточна для того, чтобы воздействовать на возбудителя, локализующегося в глубине очага воспаления (вегетаций) и окруженного тромбин-фибриновым «защитным» сгустком.
К наиболее часто используемым для лечения инфекционного эндокардита антибиотикам с бактерицидным действием относятся:
· ингибиторы синтеза клеточной стенки бактерий — b-лактамы (пенициллины, цефалоспорины, карбопенемы);
· ингибиторы синтеза белка (аминогликозиды, рифампицин);
· ингибиторы синтеза нуклеиновых кислот (фторхинолоны).
В табл. 9.3 представлены ориентировочные схемы применения антибиотиков в зависимости от возбудителя и его чувствительности (В.П. Тюрин, А.А. Демина, В.П. Дробышева, М.А. Гуревич с соавт.).
Таблица 9.3
Схемы антибактериальной терапии больных инфекционным эндокардитом
| Антибиотики | Дозы и кратность введения | Длительность лечения |
| Пенициллинчувствительные стрептококки(S. viridans, S. bovis, S. pneumoniae, S. pyogenes и др.) | ||
| 1. Бензилпенициллин | 2–4 млн ЕД каждые 4 ч | 4 нед |
| 2. Цефтриаксон | 2 г внутривенно 1 раз в сутки | 4 нед |
| 3. Бензилпенициллин + + Гентамицин | 2–4 млн ЕД каждые 4 ч 1 мг/кг каждые 12 ч | 2 нед |
| 4. Цефтриаксон + +Гентамицин | 2 г внутривенно 1 раз в сутки 1 мг/кг каждые 12 ч | 2 нед |
| 5. Ванкомицин | 15 мг/кг каждые 12 ч | 4 нед |
| Относительно пенициллинустойчивые стрептококки | ||
| 1. Бензилпенициллин + + Гентамицин | 4 млн ЕД каждые 4 ч 1 мг/кг каждые 12 ч | 4–6 нед |
| 2. Цефтриаксон + +Гентамицин | 2 г внутривенно 1 раз в сутки 1 мг/кг каждые 12 ч | 4–6 нед |
| 3. Ванкомицин | 15 мг/кг каждые 12 ч | 4–6 нед |
| Энтерококки (E. fecalis, E. faecium и др. ) и пенициллинустойчивые стрептококки | ||
| 1. Бензилпенициллин+ + Гентамицин | 2–4 млн ЕД каждые 4 ч 1 мг/кг каждые 8 ч | 4–6 нед |
| 2. Ампициллин + + Гентамицин | 2 г каждые 4 ч 1 мг/кг каждые 8 ч | 4–6 нед |
| 3. Ванкомицин + + Гентамицин | 15 мг/кг каждые 12 ч 1 мг/кг каждые 8 ч | 4–6 нед |
| Стафилококки (S. aureus, S. epidermidis и др.) | ||
| 1. Оксациллин + + Гентамицин | 2 г каждые 4 ч 1 мг/кг каждые 8 ч | 4–6 нед 10–14 дней |
| 2. Цефазолин + + Гентамицин | 2 г каждые 8 ч 1 мг/кг каждые 8 ч | 4–6 нед 10–14 дней |
| 3. Ванкомицин | 15 мг/кг каждые 12 ч | 4–6 нед |
| Грамотрицательные бактерии (E. coli, Proteus spp., Pseudomonas spp., Klebsiella spp., Enterobacter spp., Serratia spp.) | ||
| 1. Цефепим + + Гентамицин | 2 г каждые 12 ч 1 мг/кг каждые 8 ч | 4 нед 10–14 дней |
| 2. Цефепим + + Амикациин | 2 г каждые 12 ч 1 мг/кг каждые 8 ч | 4 нед. 10–14 дней |
| 3. Имипенем | 0,5 г каждые 6 ч | 4 нед |
| Грибы Candida spp., Aspergillus spp. | ||
| Амфотерицин В + + Флуконазол | 1 мг/кг 1 раз в сутки 400 мг 1 раз в сутки | 4–6 нед 4–6 нед |
| 9.6.2. Хирургическое лечение |
Сущность оперативного вмешательства при инфекционном эндокардите заключается в санации камер сердца и радикальной коррекции внутрисердечной гемодинамики (Ю.Л. Шевченко, 1995). С этой целью проводится механическое удаление инфицированных тканей с последующей рациональной антибиотикотерапией. При необходимости осуществляют протезирование пораженного клапана.
Лучшие результаты отмечаются у пациентов, оперированных в ранние сроки инфекционного эндокардита, при сохраненном миокардиальном резерве (М.А. Гуревич). Основными показаниями к хирургическому лечению являются:
1. Перфорация или отрыв створок клапана с развитием острой сердечной недостаточности.
2. Артериальные тромбоэмболии. Оперативное вмешательство показано после первого эпизода тромбоэмболии, поскольку риск повторных тромбоэмболий достаточно высок (около 54%).
3. Абсцессы миокарда, клапанного фиброзного кольца, поскольку дальнейшее консервативное лечение бесперспективно и неизбежен летальный исход.
4. Грибковый эндокардит, который в 100% случаев приводит к смертельному исходу, если не осуществляется своевременное оперативное вмешательство.
5. Инфекционный эндокардит клапанного протеза, обусловленный особо вирулентной флорой. Летальность при продолжении консервативной терапии достигает 35–55%.
6. Неэффективность этиотропной терапии в течение 3–4 недель (сохранение лихорадки, прогрессирующая деструкция клапана и т.д.).
Глава 10. Кардиомиопатии
| 10.1. Дилатационная кардиомиопатия |

|
Дилатационная кардиомиопатия (ДКМП) — это первичное поражение миокарда, характеризующееся выраженной дилатацией полостей и нарушением систолической функции желудочков. Термин ДКМП применим только к тем случаям поражения сердца, при которых значительная дилатация полостей не является следствием нарушения коронарного кровообращения (ИБС), врожденных аномалий развития, клапанных пороков сердца, системной и легочной артериальной гипертензии и заболеваний перикарда.
Распространенность ДКМП неизвестна, поскольку до сих пор отсутствуют четкие критерии ее диагностики, что затрудняет проведение эпидемиологических исследований. Заболеваемость по данным разных авторов колеблется от 5 до 10 человек на 100 тысяч населения в год. ДКМП в 2–3 раза чаще встречается у мужчин, особенно в возрасте 30–50 лет.
| 10.1.1. Этиология |

|
В большинстве случаев этиология ДКМП неизвестна (идиопатическая форма ДКМП). Примерно у 20% больных заболевание ассоциируется с перенесенным ранее инфекционным миокардитом. Считают, что воздействие на миофибриллы персистирующих в организме инфекционных агентов (в первую очередь энтеровирусов), в том числе включение вирусной РНК в генетический аппарат кардиомиоцитов или влияние “запущенного” вирусами аутоиммунного процесса, ведет к повреждению митохондрий и нарушению энергетического метаболизма клеток.
При использовании современных молекулярно-биологических технологий, в том числе полимеразной цепной реакции (ПЦР) у части больных удается выявить присутствие энтеровирусов, в частности вирусов Коксаки В, вируса гепатита С, герпеса, цитомегаловируса и др.
У части больных обнаруживаются также высокие титры кардиоспецифических аутоантител к миозину тяжелых цепей, актину, тропомиозину и митохондриальной мембране кардиомиоцитов, а также увеличение цитокинов в крови, что подчеркивает роль аутоиммунных нарушений. Вероятно, именно больные с исходным аутоиммунным дефицитом в большей степени подвержены повреждающему воздействию вирусов и развитию ДКМП.
В происхождении ДКМП большое значение имеет также генетическая предрасположенность к возникновению заболевания. Семейные ДКМП встречаются примерно в  случаев заболевания. Для них характерно, главным образом, аутосомно-доминантное наследование. У части больных ДКМП обнаруживаются также гаплотипы НLА В27 и НLА DR4.
случаев заболевания. Для них характерно, главным образом, аутосомно-доминантное наследование. У части больных ДКМП обнаруживаются также гаплотипы НLА В27 и НLА DR4.
Наконец, имеются данные о неблагоприятном воздействии алкоголя на миокард, что может приводить к нарушению синтеза сократительных белков кардиомиоцитов, повреждению митохондрий, нарушению энергетического метаболизма клеток и, в конечном счете, к критическому снижению сократимости сердечной мышцы и расширению полостей сердца, т.е. к формированию ДКМП.
Таким образом, в генезе ДКМП имеет значение взаимодействие нескольких факторов:
- генетической предрасположенности к возникновению заболевания;
- воздействия экзогенных факторов (вирусная инфекция, алкоголь) и
- аутоиммунных нарушений.
Если на начальных стадиях развития ДКМП в ряде случаев удается подтвердить вторичную природу поражения сердца (например, наличие вирусной инфекции), то на поздних стадиях клиническая картина уже мало зависит от возможных пусковых механизмов болезни (А.В. Сумароков). Поэтому на практике в подавляющем большинстве случаев конкретные причины остаются невыясненными и ДКМП трактуется как идиопатическая форма заболевания, удовлетворяющая традиционным критериям КМП по J. Goodwin.
 Запомните
1. Возникновение ДКМП связывают с взаимодействием нескольких патогенетических факторов:
· генетической предрасположенности к возникновению заболевания;
· воздействия экзогенных факторов (вирусная инфекция, злоупотребление алкоголем);
· аутоиммунных нарушений.
2. Семейная (генетически детерминированная) ДКМП встречается примерно в Запомните
1. Возникновение ДКМП связывают с взаимодействием нескольких патогенетических факторов:
· генетической предрасположенности к возникновению заболевания;
· воздействия экзогенных факторов (вирусная инфекция, злоупотребление алкоголем);
· аутоиммунных нарушений.
2. Семейная (генетически детерминированная) ДКМП встречается примерно в  случаев заболевания. Примерно у 20% больных ДКМП ассоциируется с вирусной инфекцией. Однако в большинстве случаев диагностируется идиопатическая форма ДКМП, когда взаимодействие перечисленных этиологических факторов становится настолько неопределенным, что выделить один из них в качестве основного не представляется возможным. случаев заболевания. Примерно у 20% больных ДКМП ассоциируется с вирусной инфекцией. Однако в большинстве случаев диагностируется идиопатическая форма ДКМП, когда взаимодействие перечисленных этиологических факторов становится настолько неопределенным, что выделить один из них в качестве основного не представляется возможным.
| ||
| 10.1.2. Патогенез | ||

| ||
В результате воздействия перечисленных выше и некоторых других (в том числе пока неизвестных) этиологических факторов происходит первичное повреждение кардиомиоцитов, снижение энергетического метаболизма клеток и уменьшение количества нормально функционирующих миофибрилл. Это ведет к прогрессирующему уменьшению сократительной способности миокарда и насосной функции сердца. В результате снижения инотропной функции миокарда происходит дилатация полостей сердца, которая, согласно механизму Старлинга, в течение некоторого времени поддерживает УО и ФВ на достаточном уровне. Одновременно развивающаяся тахикардия (активация САС) также способствует сохранению сердечного выброса (МО, СИ).
Однако такая компенсация весьма невыгодна с энергетической точки зрения, поскольку согласно закону Лапласа, для создания адекватного давления в полости желудочка дилатированная стенка ЛЖ должна развивать значительно большее внутримиокардиальное напряжение (рис. 10.2). Следствиями такого прогрессирующего увеличения постнагрузки являются:
- развитие компенсаторной гипертрофии миокарда желудочков, которая способствует некоторому снижению внутримиокардиального напряжения;
- увеличение потребности миокарда в кислороде, которое со временем ведет к развитию относительной коронарной недостаточности и ишемии миокарда;
- дальнейшее повреждение кардиомиоцитов и еще большее снижение сократимости;
- развитие диффузного и очагового кардиофиброза.
В результате происходит критическое падение насосной функции сердца, повышается КДД в желудочках и развивается выраженная миогенная дилатация полостей сердца.
Эти явления усугубляются развитием относительной недостаточности митрального и трехстворчатого клапанов, что способствует еще большей дилатации предсердий и желудочков. Иными словами, формируется и быстро прогрессирует хроническая сердечная недостаточность (ХСН) с преимущественным нарушением систолической функции желудочков, застоем крови в малом и большом кругах кровообращения, падением сердечного выброса и нарушением перфузии периферических органов и тканей.
Следует отметить, что значительное увеличение массы сердца за счет гипертрофии миокарда обычно не сопровождается заметным утолщением стенки желудочков, поскольку при ДКМП всегда преобладает выраженная дилатация камер сердца, которая как бы нивелирует увеличение мышечной массы (см. рис. 10.1).
Так же как и при других формах ХСН, важное значение в ремоделировании сердечной мышцы и развитии сердечной декомпенсации имеет чрезмерная активация нейрогормональных систем организма, в том числе САС, РААС, АДГ, тканевых РАС и эндотелиальных факторов. В результате активации этих систем происходит задержка Nа+ и воды в организме, что усугубляет застойные явления в малом и большом кругах кровообращения. Повышенное содержание катехоламинов, АII, цитокинов, фактора роста опухолей a, тромбоксана АIII приводит к еще большему повреждению миокарда, периферической вазоконстрикции, а также к значительным нарушениям свертывающей и фибринолитической систем крови.
 Запомните
1. В основе формирования ДКМП лежит первичное повреждение и гибель кардиомиоцитов, гемодинамическими следствиями которых являются:
· прогрессирующее снижение сократительной способности;
· выраженная дилатация полостей сердца;
· развитие компенсаторной гипертрофии миокарда и увеличение массы сердца (без утолщения стенок желудочков);
· развитие в тяжелых случаях заболевания относительной недостаточности митрального и трикуспидального клапанов;
· застой крови в малом и большом кругах кровообращения;
· относительная коронарная недостаточность и развитие ишемии сердечной мышцы;
· развитие диффузного и очагового фиброза в миокарде;
· периферическая вазоконстрикция и нарушение перфузии периферических органов и тканей.
2. Процесс ремоделирования сердца, а также описанные гемодинамические расстройства во многом обусловлены чрезмерной активацией нейрогормональных систем организма (САС, РААС, АДГ, эндотелиальных факторов, тканевых РАС и др.). 3. Прогрессирующее повреждение сердечной мышцы и нейрогормональная активация способствуют частому развитию у больных ДКМП:
· нарушений сердечного ритма и проводимости;
· внутрисердечных тромбозов и тромбоэмболических осложнений. Запомните
1. В основе формирования ДКМП лежит первичное повреждение и гибель кардиомиоцитов, гемодинамическими следствиями которых являются:
· прогрессирующее снижение сократительной способности;
· выраженная дилатация полостей сердца;
· развитие компенсаторной гипертрофии миокарда и увеличение массы сердца (без утолщения стенок желудочков);
· развитие в тяжелых случаях заболевания относительной недостаточности митрального и трикуспидального клапанов;
· застой крови в малом и большом кругах кровообращения;
· относительная коронарная недостаточность и развитие ишемии сердечной мышцы;
· развитие диффузного и очагового фиброза в миокарде;
· периферическая вазоконстрикция и нарушение перфузии периферических органов и тканей.
2. Процесс ремоделирования сердца, а также описанные гемодинамические расстройства во многом обусловлены чрезмерной активацией нейрогормональных систем организма (САС, РААС, АДГ, эндотелиальных факторов, тканевых РАС и др.). 3. Прогрессирующее повреждение сердечной мышцы и нейрогормональная активация способствуют частому развитию у больных ДКМП:
· нарушений сердечного ритма и проводимости;
· внутрисердечных тромбозов и тромбоэмболических осложнений.
| ||
| 10.1.3. Клиническая картина | ||

| ||
Клинически ДКМП проявляется тремя основными синдромами:
1. Систолической ХСН (левожелудочковой или бивентрикулярной) с признаками застоя крови в малом и большом кругах кровообращения.
2. Частым возникновением нарушений ритма и проводимости (желудочковые аритмии, фибрилляция предсердий, АВ-блокады и блокады ножек пучка Гиса).
3. Тромбоэмболическими осложнениями (ТЭЛА и эмболия в артерии большого круга кровообращения).
Таким образом, клинические проявления ДКМП, так же как результаты инструментального и лабораторного исследований, весьма неспецифичны, что затрудняет дифференциальный диагноз. Поэтому диагноз ДКМП ставится, как правило, путем исключения других заболеваний сердца с систолической дисфункцией желудочков (ИБС, АГ, миокардит, легочное сердце и др.).
Жалобы
Заболевание длительное время может протекать бессимптомно, несмотря на наличие объективных (эхокардиографических) признаков дилатации желудочков и нарушения их функции. Обычно первые клинические проявления болезни связаны с сердечной декомпенсацией, застоем крови в малом, а затем и в большом кругах кровообращения и снижением сердечного выброса. Больные жалуются на одышку при физической нагрузке и в покое, усиливающуюся в горизонтальном положении больного (ортопноэ). В далеко зашедших случаях возникают приступы удушья, чаще развивающегося по ночам (сердечная астма и отек легких). Очень характерна быстрая утомляемость, мышечная слабость, тяжесть в ногах при выполнении физических нагрузок. Признаки правожелудочковой недостаточности (отеки ног, тяжесть в правом подреберье, увеличение живота в объеме, диспептические явления) появляются позже.
 Запомните
Наиболее важной клинической особенностью ДКМП является быстрое и неуклонное прогрессирование заболевания и признаков декомпенсации, а также рефрактерность к традиционному лечению ХСН. Запомните
Наиболее важной клинической особенностью ДКМП является быстрое и неуклонное прогрессирование заболевания и признаков декомпенсации, а также рефрактерность к традиционному лечению ХСН.
|
Примерно у  больных развиваются разнообразные нарушения ритма и проводимости, часть из которых вызывает у больных ДКМП неприятные ощущения (сердцебиения, перебои в работе сердца, приступы пароксизмальной тахикардии и мерцательной аритмии).
больных развиваются разнообразные нарушения ритма и проводимости, часть из которых вызывает у больных ДКМП неприятные ощущения (сердцебиения, перебои в работе сердца, приступы пароксизмальной тахикардии и мерцательной аритмии).
Наиболее тяжелыми осложнениями являются тромбозы и тромбоэмболии, развивающиеся у 20% больных ДКМП. Наиболее часто эти осложнения возникают у больных с фибрилляцией предсердий.
Иногда больные ДКМП отмечают боли в области сердца, которые в большинстве случаев отличаются от типичных приступов стенокардии. Боли часто имеют атипичную локализацию и, как правило, не связаны с физической нагрузкой.
Физикальное исследование
Физикальные данные, получаемые у больных ДКМП, также весьма неспецифичны. При общем осмотре выявляются известные признаки сердечной недостаточности (см. главу 2): акроцианоз, отеки ног, положение ортопноэ, увеличение живота в объеме, набухание шейных вен, иногда положительный венный пульс и др.
При исследовании легких в нижних отделах могут выслушиваться влажные мелкопузырчатые хрипы. Отмечается увеличение печени. В далеко зашедших случаях появляются признаки сердечной кахексии.
Осмотр, пальпация и перкуссия сердца
Верхушечный толчок, как правило, усилен, разлитой и смещен влево и вниз. Чаще всего можно выявить также усиленный и разлитой сердечный толчок и эпигастральную пульсацию, что указывает на наличие гипертрофии и дилатации ПЖ.
Обычно выявляется смещение влево левой границы относительной тупости сердца и вправо — правой границы. Дилатация ЛП сопровождается смещением вверх верхней границы сердца и сглаживанием “талии” сердца. Абсолютная тупость сердца обычно расширена за счет дилатации ПЖ (рис. 10.3).
Дата добавления: 2016-01-20; просмотров: 2010;
