Примеры решения задач. Рассчитать рН буферного раствора, приготовленного смешением 10 мл 0,1М раствора уксусной кислоты и 100 мл 0,1М раствора ацетата натрия (рК(сн3 соон) =4,76).
Пример 1.
Рассчитать рН буферного раствора, приготовленного смешением 10 мл 0,1М раствора уксусной кислоты и 100 мл 0,1М раствора ацетата натрия (рК(сн3 соон) =4,76).
Решение:
Рассчитываем рН кислотного буферного раствора по формуле 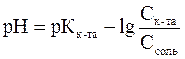 , тогда
, тогда 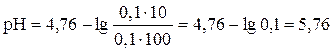
Ответ: 5,76
Пример 2.
Рассчитать буферную емкость по кислоте, если на титрование 10 мл сыворотки крови пошло 5 мл 0,1 моль/л соляной кислоты, если при титровании рН изменился от 7,36 до 5,0.
Решение:
Рассчитываем буферную емкость по формуле: 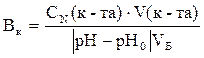
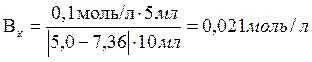
Ответ: 0,021 моль/л
Пример 3.
Буферный раствор состоит из 100 мл 0,1моль/л уксусной кислоты и 200 мл 0,2моль/л ацетата натрия. Как изменится рН этого раствора, если к ней добавить 30 мл 0,2моль/л раствора гидроксида натрия.
Решение:
Рассчитываем рН буферного раствора по формуле: 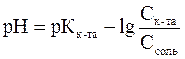
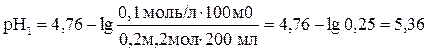
При добавлении к буферному раствору NaOH увеличивается количество соли и уменьшается количество кислоты в буферном растворе:
0,006 0,006 0,006
СH3COOH + NaOH = CH3COONa + H2O
Рассчитываем n(NaOH) = 0,03 л · 0,2 моль/л = 0,006 моль, следовательно в буферном растворе количество кислоты уменьшается на 0,006 моль, а количество соли увеличится на 0,006 моль. 
Рассчитываем рН раствора по формуле:
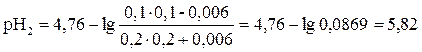
Отсюда: рН2 – рН1 = 5,82 – 5,3 = 0,52
Ответ: изменение рН буферного раствора = 0,52.
Дата добавления: 2016-01-09; просмотров: 35141;
