Алифатические (простые спирты)
Спирты. Фенолы. Простые эфиры
Замещение одного или нескольких атомов водорода в молекуле углеводорода на гидроксильную группу приводит к образованию молекулы спирта. Спирты бывают алифатическими, алициклическими и ароматическими, причем в последних ОН-группа не связана непосредственно с ароматическим ядром (например: бензиловый спирт С6Н5СН2ОН).Соединения, в которых гидроксильная группа связана с атомом углерода ароматического кольца, называют фенолами.
ОН-группа может быть связана с первичным, вторичным или третичным атомом углерода. Соответственно спирты разделяют на первичные (RCH2OH), вторичные (R2CHOH) и третичные (R3COH).
По числу гидроксильных групп спирты разделяются на одноатомные, двухатомные, трехатомные и т.д. Многоатомные спирты называют гликолями.
Алифатические (простые спирты)
Члены гомологического ряда алифатических спиртов имеют общую формулу СnН2n+1ОН.
R-OH, где R — углеводородный радикал R=СnН2n+1
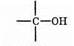
Алифатические спирты могут быть представлены как алканы, в которых один атом водорода замещен функциональной группой —ОН. Поэтому спирты называют алканолами. Названия спиртов получаются из названия соответствующих алканов с добавлением суффикса -ол. Ниже приведены названия первых членов гомологического ряда:
СН3ОН — метанол C4H9OH — бутанол
С2Н5ОН — этанол C5H11OH — пентанол
С3H7ОН — пропанол С6Н13ОН — гексанол
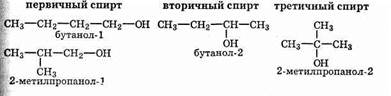
Структурная изомерия предельных (алифатических) одноатомных спиртов определяется строением углеродной цепи и положением гидроксильной группы в цепи. Например, существуют четыре изомера бутанола С4Н9ОН. Нумерацию цепи начинают с того края, ближе к которому расположена ОН-группа.
Низшие спирты (до С12) при комнатной температуре — жидкости, высшие — твердые вещества. Температуры кипения спиртов намного выше температур кипения алканов с такой же молекулярной массой. Например, t°кип (С2Н5ОН — этанол)=78°С, а t°кип (С3Н8 — пропан)=42°С; t°кип(С7Н15ОН — гептанол-1)=180°С, а t°кип (C8H18 — октан)=126°С. Причиной этого является высокая полярность связи О—Н и легкость образования водородных связей молекулами спирта. Итак, спирты имеют аномально высокие температуры кипения благодаря водородным связям.
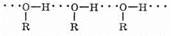
При испарении жидкости водородные связи между молекулами разрываются, что требует дополнительной затраты энергии. Следовательно, увеличение молекулярной массы приводит к росту температуры кипения, а разветвленные спирты кипят при более низкой температуре, чем неразветвленные.
Растворимость
Низшие спирты хорошо растворимы в воде, т.к. молекулы спирта легко образуют водородные связи с молекулами воды:
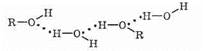
Спирты с большой молекулярной массой и большим размером углеводородного радикала (R) образуют гораздо меньше водородных связей, чем молекулы воды, занимающие тот же объем, что и молекула спирта. Поэтому растворение высших спиртов в воде энергетически невыгодно, и их растворимость невелика.
Образование азеотропных смесей
Этанол образует азеотропную смесь с водой, содержащую 95,6% этанола и кипящую при 78,1°С. Поэтому безводный этанол может быть получен только перегонкой над каким-либо осушителем (например, СаО — оксидом кальция (II)). Многие другие спирты также образуют с водой азеотропную смесь.
Вспомним, что:
при кипении жидкости состава А пар имеет тот же состав, что и эта жидкость. Это означает, что и состав, и, следовательно, температура кипения (Ткип) не изменяются в течение процесса. Такую смесь называют азеотропом, или нераздельно кипящей смесью. Азеотропы — не соединения, т.к. их составы зависят от давления.
Спирты как растворители
Спирты — хорошие растворители. Они растворяют как полярные, так и неполярные вещества. Наличие в молекуле полярной ОН-группы позволяет им растворять такие полярные вещества, как гидроксиды калия и натрия. Неполярный алкильный радикал обеспечивает растворимость в спиртах таких малополярных соединений, как углеводороды.
Плотность
Алифатические спирты легче воды, а ароматические — чуть тяжелее.
Вязкость
Этанол — подвижная жидкость с низкой вязкостью. Многоатомные спирты из-за большого числа водородных связей имеют высокую вязкость.
Получение
Промышленные источники спиртов
1. Гидратация алкенов. Каталитическая гидратация алкенов протекает по механизму электрофильного присоединения по правилу Марковникова (см. §2.4). Например, получение этанола:
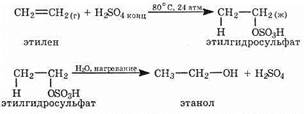
2. Природный газ как источник метанола. Метанол можно получить из природного газа. Смесь метана с водяным паром пропускают над катализатором:
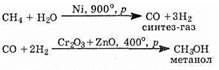
3. Ферментативный синтез этанола. Этанол получают при брожении Сахаров, вызываемом ферментами:
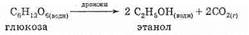
Дрожжи — это живые одноклеточные организмы, содержащие фермент зимазу, который катализирует реакцию.
Лабораторные синтезы спиртов
. Гидролиз галогеналканов. Галогеналканы гидролизуются под действием водных растворов щелочей. Реакция протекает по механизму нуклеофильного замещения:
R-Br + NaOH ®R-OH+NaBr
2. Синтез спиртов из сложных эфиров. При кипячении сложного эфира с разбавленной кислотой или щелочью образуются карбоновая кислота или ее соль и спирт:

Восстановление альдегидов, кетонов и карбоновых кислот. Спирты образуются также при восстановлении альдегидов и кетонов (см. §6), карбоновых кислот и их производных — сложных эфиров и хлорангидридов (см. §7).
СН3-СН=О+2[Н]®СН3СН2ОН СН3-СО-СН3+2[Н]®СН3-СН(ОН)-СН3
Ниже указаны промышленные и лабораторные способы синтеза спиртов.

Химические свойства спиртов
Подобно воде, спирты проявляют амфотерные свойства. Большинство химических реакций спиртов протекают с разрывом связи RO—Н, например, реакции с натрием или карбоновыми
кислотами обусловлены разрывом связи R—ОН.
Спирты — полярные соединения. Полярная связь —Оd-—Нd+ имеет слабую тенденцию диссоциировать с образованием алкоксид-аннона и протона:
R-OH«R-O-+H+
Следовательно, спирты — слабые кислоты с очень низким значением ka»10-16 моль•дм-3, где ka — константа диссоциации. Спирты — более слабые кислоты, чем вода.
Первой стадией таких реакций обычно является протонирование атома кислорода. После этого связь R—О+Н2 разрывается гораздо легче. Например, реакция этанола с иодоводородной кислотой начинается с переноса протона:
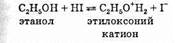
Затем алкилоксоний-катион теряет молекулу воды, превращаясь в галогеналкан:
C2H5OH+H2+I- ®С2Н5I+Н2O
Основные свойства наиболее сильны у третичных спиртов и падают в ряду: третичные > вторичные > первичные спирты
Кислотные же свойства спиртов уменьшаются в ряду: первичные > вторичные > третичные спирты
Рассмотрим реакции спиртов на примере этанола.
Реакции с разрывом связи RO—H. Кислотные свойства спиртов
1. Спирты реагируют с щелочными и щелочноземельными металлами, при этом образуется алкоксид металла и водород. Например, реакция этанола с натрием идет значительно медленнее, чем реакция натрия с водой:
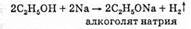
Итак, кислотные свойства спиртов выражены очень слабо. С увеличением длины углеводородного радикала скорость этой реакции замедляется.
В присутствии воды образующиеся алкоголяты разлагаются до исходных спиртов:
C2H6ONa+Н2О®С2Н6ОН+NaOH Это доказывает, что спирты — более слабые кислоты, чем вода.
2. Спирты реагируют с карбоновыми кислотами, образуя при этом сложные эфиры. Эта реакция называется реакцией зтерификации (см. §7).
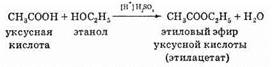
Дата добавления: 2016-01-03; просмотров: 13145;
