Дезаминирование аминокислот
В процессе дезаминирования происходит отщепление от аминокислоты аминогруппы, которая освобождается в виде аммиака. Для организма человека характерно т.н. окислительное дезаминирование, которое осуществляется в два этапа (рис. 54). На первом этапе от аминокислоты отщепляется водород. Реакция катализируется специфическими дегидрогеназами, в которых роль акцептора водорода выполняют НАД или ФАД.
1 этап
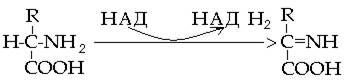
Аминокислота Иминокислота
2 этап

Иминокислота Кетокислота
Рис. 54. Реакция дезаминирования аминокислот
В качестве продукта реакции образуется иминокислота. На втором этапе иминокислота взаимодействует с водой, в результате чего образуется кетокислота и свободный аммиак.
Реакции дезаминирования обратимы. Некоторые кетокислоты могут взаимодействовать со свободным аммиаком с образованием аминокислот (реакция аминирования). В такую реакцию вступает α-кетоглутаровая кислота, в результате чего образуется глутаминовая кислота.
Другой кетокислотой, подвергающейся аминированию, является пировиноградная кислота. В результате этой реакции образуется аминокислота аланин (рис. 55).
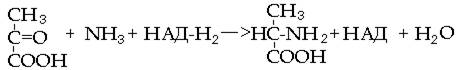
пируват аланин
Рис. 55. Реакция аминирования пировиноградной кислоты
Образующийся в ходе реакции дезаминирования свободный аммиак токсичен даже в самых малых концентрациях. Он может вызвать локальные сдвиги рН, изменения заряда на клеточных мембранах. Незначительное повышение концентрации аммиака в мышечных клетках может вызвать судороги. Особенно выраженное токсическое влияние оказывает аммиак на мозговые клетки. Поэтому в организме существуют механизмы обезвреживания и устранения аммиака.
Дата добавления: 2015-10-29; просмотров: 2421;
