Состав топлива и его теплота сгорания
Органическая часть твердых и жидких топлив состоит из большого количества сложных химических соединений, образованных пятью химическими элементами: углерод (С), водород (Н), сера (S), кислород (О) и азот (N). Кроме того, топливо содержит минеральные примеси (А), которые превращаются при сжигании в золу и влагу (W). Поэтому химический состав твердых и жидких топлив определяется не по количеству химических соединений, а по суммарной массе химических элементов в топливе в процентах на один килограмм, т. е. по элементному составу топлива.
Горючими элементами топлива являются углерод, водород, сера. Углерод является основным горючим элементом топлива, имеет высокую теплоту сгорания (34,4 МДж/кг) и составляет большую часть горючей массы топлива. Водород также имеет высокую теплоту сгорания (120,5 МДж/кг), но его содержание в топливе невелико (2-4% в твердом и 10-11% в жидком). Сера имеет невысокую теплоту сгорания (9,3 МДж/кг), и ее содержание в топливе невелико (0,3-0,5%), поэтому она не представляет ценности как горючий элемент. Но поскольку при сжигании топлива образуется диоксид серы, сернистость топлива является важной характеристикой.
Различают пять основных состояний топлива. Рабочее состояние топлива (верхний индекс р (r)) – это состояние топлива с таким содержанием влаги и зольностью, с которым оно добывается, отгружается или используется:
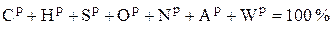 . (4.1)
. (4.1)
Аналитическое состояние топлива (верхний индекс а (а)) – состояние топлива, характеризуемое подготовкой пробы. Подготовка предусматривает размол до размеров частиц 0,2 мм и приведение в равновесие с условиями лабораторного помещения:
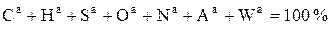 . (4.2)
. (4.2)
Сухое состояние топлива (верхний индекс с (d)) – состояние топлива без содержания общей влаги (кроме гидратной):
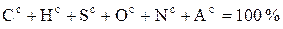 . (4.3)
. (4.3)
Горючее (условное сухое беззольное) состояние топлива (верхний индекс г (daf)) – условное состояние топлива, не содержащего общей влаги и золы:
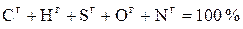 . (4.4)
. (4.4)
Органическое состояние топлива (верхний индекс о (о)) – условное состояние топлива без содержания влаги и минеральной массы:

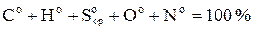 . (4.5)
. (4.5)
| Wвн | Wа | О | N | H | C | Sор | Sп | Sсфт | А |
| Органическое состояние (о) | |||||||||
  Горючее состояние (г) Горючее состояние (г)
| |||||||||
 Сухое состояние топлива (с) Сухое состояние топлива (с)
| |||||||||
| Аналитическое состояние топлива (а) | ||||||||
 Рабочее состояние топлива (р) Рабочее состояние топлива (р)
|
Рис. 4.1. Схема состояний топлива
Для получения коэффициента пересчета состава топлива, например, из горючего состояния в рабочее необходимо сделать следующие преобразования. Запишем уравнение для рабочего состояния в следующем виде, %:
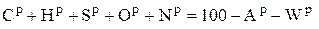 , (4.6)
, (4.6)
и разделим (1.6) на (1.4). В результате получим соотношение
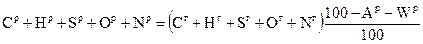 . (4.7)
. (4.7)
Таким образом, для каждого элемента, например для углерода, справедливо соотношение
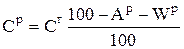 , %. (4.8)
, %. (4.8)
Аналогичным образом определяются коэффициенты пересчета для любых других состояний.
В отличие от твердого и жидкого топлива газообразное топливо представляет собой механическую смесь горючих и негорючих газов, поэтому его состав задается в объемных процентах.
Теплота сгорания характеризует энергетическую ценность топлива и представляет собой количество тепловой энергии, выделяющейся в ходе химических реакций окисления горючих элементов газообразным кислородом. Различают высшую и низшую теплоту сгорания. Высшей теплотой сгорания Qв топлива называется количество теплоты, выделяющееся при полном сгорании 1 кг твердого или жидкого топлива (1 м3 газообразного топлива) при условии конденсации водяных паров и охлаждении всех продуктов сгорания до 0 °С. Низшая теплота сгорания Qн отличается от высшей на величину теплоты испарения влаги топлива и влаги, образующейся при горении водорода. При сжигании топлива в энергетических установках температура уходящих газов превышает 100 °С, влага, содержащаяся в продуктах сгорания, остается в парообразном состоянии и теплота испарения теряется. Количество водяного пара (кг) в продуктах сгорания, которое приходится на 1 кг топлива, представляет собой сумму количества влаги, содержащейся в исходном топливе Wр/100 и образовавшейся при окислении водорода топлива 9Hр/100 ( 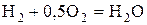 ); из одного килограмма водорода образуется 9 кг влаги). Удельная теплота конденсации водяного пара в нормальных физических условиях составляет 2500 кДж/кг. В итоге теплота конденсации водяных паров, образовавшихся из 1 кг топлива, составляет, кДж/кг:
); из одного килограмма водорода образуется 9 кг влаги). Удельная теплота конденсации водяного пара в нормальных физических условиях составляет 2500 кДж/кг. В итоге теплота конденсации водяных паров, образовавшихся из 1 кг топлива, составляет, кДж/кг:
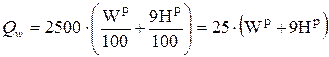 . (4.9)
. (4.9)
Тогда взаимосвязь высшей и низшей теплоты сгорания имеет вид, кДж/кг:
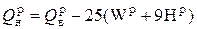 . (4.10)
. (4.10)
Наиболее надежным способом определения теплоты сгорания является ее экспериментальное измерение на специальных установках – калориметрах (рис. 1.2, СТ СЭВ 1463-78). Сущность метода заключается в том, что навеску топлива сжигают в атмосфере сжатого кислорода в герметически закрытом металлическом сосуде – калориметрической бомбе, которую погружают в определенный объем воды. Количество теплоты, выделяющееся при сгорании этого топлива, определяют по повышению температуры этой воды.
В практике электростанций теплоту сгорания используемого топлива определяют опытным путем, дающим более точные результаты. При проведении теплотехнических расчетов нередко возникает необходимость оценки теплоты сгорания топлива по данным элементного состава. Метод определения теплоты сгорания по данным элементного состава топлива основан на использовании закона Гесса, согласно которому теплота прямого превращения топлива в продукты сгорания СО2, Н2О, SО2 равна теплоте сгорания С, Н2, S за вычетом теплоты разложения исходных углеводородов топлива на простые вещества. В реальных топливах О, H и C связаны между собой в очень сложные молекулы с различными энергиями связи. Поскольку на разрыв этих связей при сжигании затрачивается различное количество энергии, поэтому до сих пор ни одно из модельных представлений не позволило получить универсальной формулы, позволяющей рассчитывать теплоту сгорания любого топлива. Наиболее удачной, т.е. простой и точной, является формула Д.И. Менделеева с эмпирически подобранными коэффициентами для соответствующих горючих элементов, ккал/кг:
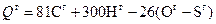 . (4.11)
. (4.11)
Теплота сгорания твердого и жидкого топлива в рабочем состоянии рассчитывается так, кДж/кг:
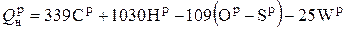 , (4.12)
, (4.12)
содержание элементов выражается в процентах.
Для газообразных топлив при точно известном их составе теплота сгорания 1м3 сухого газа, МДж/м3, может быть достаточно точно подсчитана по формуле
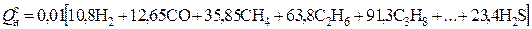 . (4.13)
. (4.13)
Здесь содержание соответствующих газовых компонентов подставляют в процентах.
Дата добавления: 2015-10-26; просмотров: 3752;
