Sp2-гибридизация
Рассмотрим на примере молекулы гидрида бора ВН3. Электронное строение атома бора в нормальном состоянии следующее В – 1s22s22p1. Он может образовать только одну ковалентную связь. Три же ковалентные связи для атома бора характерны только в возбужденном состоянии В* – 1s22s12p2
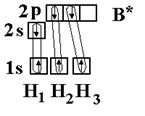
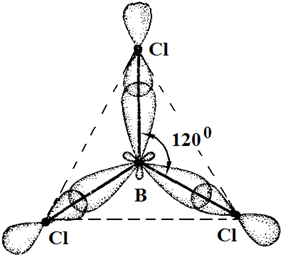
Одна связь, образованная при перекрывании двух s-орбиталей атомов В и Н, энергетически не отличается от двух других, образуемых перекрыванием s- и р-орбиталей. Три sp2-гибридные орбитали расположенные под углом 120о друг к другу, молекула имеет плоское строение. Подобная картина характерна для любых четырехатомных молекул, образованных за счет трех sp2-гибридных связей, например, для хлорида бора (BCl3).
Дата добавления: 2015-10-21; просмотров: 2443;
