Примеры решения задач. Вычисление концентрации ионов Н+ и ОН- по известному значению водородного показателя
Вычисление концентрации ионов Н+ и ОН- по известному значению водородного показателя
Пример 29. Вычислить концентрацию ионов 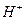 и
и 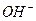 в растворе,
в растворе, 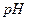 которого равен 5,25.
которого равен 5,25.
Решение: По значению 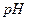 определяем концентрацию ионов
определяем концентрацию ионов 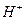 в растворе:
в растворе:
 ;
; 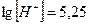 .
.
Следовательно, 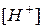 = 5,62∙10-6 моль/л.
= 5,62∙10-6 моль/л.
Концентрацию ионов 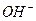 определяют по значению ионного произведения воды:
определяют по значению ионного произведения воды:
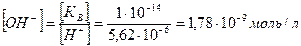
Вычисление рН в растворах сильных и слабых электролитов
Пример 30. Вычислить 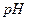 раствора, содержащего в 1 л
раствора, содержащего в 1 л
0,855 г гидроксида бария.
Решение: Диссоциация молекулы гидроксида бария:
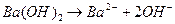
Концентрация ионов 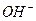 :
:
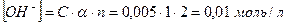 ,
,
где 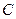 – молярная концентрация раствора, моль/л;
– молярная концентрация раствора, моль/л;
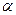 – степень диссоциации электролита (для сильных электролитов
– степень диссоциации электролита (для сильных электролитов 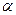 = 1, для слабых электролитов
= 1, для слабых электролитов 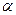 рассчитывается по закону разбавления Оствальда);
рассчитывается по закону разбавления Оствальда);
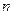 – число ионов, образующихся при диссоциации одной молекулы.
– число ионов, образующихся при диссоциации одной молекулы.
Гидроксильный показатель 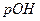 :
:
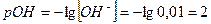 .
.
Водородный показатель 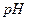 :
:
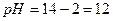 .
.
Пример 31. Вычислить 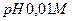 раствора уксусной кислоты, если
раствора уксусной кислоты, если 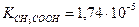
Решение: Степень диссоциации уксусной кислоты:

Диссоциация молекулы уксусной кислоты:

Концентрация ионов 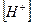 в растворе:
в растворе:
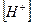 = 0,01∙4,17∙10-2∙1 = 4,17∙10-4 моль/л.
= 0,01∙4,17∙10-2∙1 = 4,17∙10-4 моль/л.
Водородный показатель 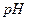 :
:
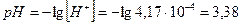 .
.
Вычисление рН при сливании растворов
Пример 32. Вычислить 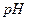 раствора, если к 25 мл 0,01 М раствора
раствора, если к 25 мл 0,01 М раствора 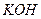 (
(  = 1 г/мл) прибавили 500 мл воды. Плотность нового раствора 1 г/мл.
= 1 г/мл) прибавили 500 мл воды. Плотность нового раствора 1 г/мл.
Решение:
1) Находим количество вещества 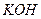 , содержащееся в
, содержащееся в
25 мл 0,01 М раствора:

2) Вычисляем молярную концентрацию нового раствора гидроксида калия, полученного после разбавления. Поскольку плотность растворов условно принята 1 г/мл, то объем нового раствора равен:
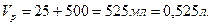
Тогда:


3) Находим концентрацию гидроксид-ионов:

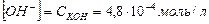
4) Находим концентрацию ионов 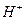 :
:
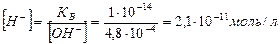
5) Вычисляем 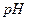 нового раствора:
нового раствора:
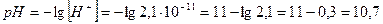
Пример 33. К 20 мл 0,04 н. раствора 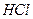 добавили 35 мл
добавили 35 мл
0,02 н. раствора 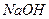 . Вычислить
. Вычислить 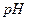 полученного раствора.
полученного раствора.
Решение:
1) В исходном растворе находим количества веществ эквивалентов:
| |


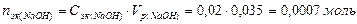
По закону эквивалентов  .
.
2) Раствор в избытке содержит:
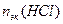 = 0,0008 - 0,0007 = 0,0001 моль.
= 0,0008 - 0,0007 = 0,0001 моль.
3) Находим концентрацию ионов 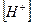 в растворе:
в растворе:
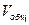 = 20+ 35 = 55 мл = 0,055 л;
= 20+ 35 = 55 мл = 0,055 л;
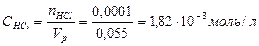
4) Вычисляем 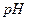 нового раствора:
нового раствора:
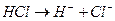
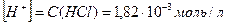 ;
;
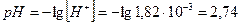 .
.
Дата добавления: 2015-10-19; просмотров: 13965;
