Число степеней свободы молекулы. Закон равномерного распределения энергии по степеням свободы молекул
Важной характеристикой термодинамической системы является ее внутренняя энергия U – энергия хаотического (теплового) движения микрочастиц системы (молекул, атомов, электронов, ядер и т. д.) и энергия взаимодействия этих частиц. Из этого определения следует, что к внутренней энергии не относятся кинетическая энергия движения системы как целого и потенциальная энергия системы во внешних полях.
Внутренняя энергия – однозначная функциятермодинамического состояния системы, т.е. в каждом состоянии система обладает вполне определенной внутренней энергией (она не зависит от того, как система пришла в данное состояние). Это означает, что при переходе системы из одного состояния в другое изменение внутренней энергии определяется только разностью значений внутренней энергии этих состояний и не зависит от пути перехода.
 Введем понятие числа степеней свободы i: это число независимых переменных (координат), полностью определяющих положение системы в пространстве. В ряде задач молекулу
Введем понятие числа степеней свободы i: это число независимых переменных (координат), полностью определяющих положение системы в пространстве. В ряде задач молекулу
Рис.11.1 одноатомного газа (рис.11.1 а) рассматривают как материальную точку, которой приписывают три степени свободы поступательного движения (i=3). При этом энергию вращательного движения можно не учитывать.
В классической механике молекула двухатомного газа в первом приближении рассматривается как совокупность двух материальных точек, жестко связанных недеформируемой связью (рис.11.1 б). Эта система кроме трех степеней свободы поступательного движения имеет еще две степени свободы вращательного движения. Вращение вокруг третьей оси (оси, проходящей через оба атома) лишено смысла. Таким образом, двухатомный газ обладает пятью степенями свободы (i=5). Трехатомная (рис.11.1 в)и многоатомная нелинейные молекулы имеют шесть степеней свободы: три поступательных и три вращательных (i=6).
Естественно, что жесткой связи между атомами не существует. Поэтому для реальных молекул необходимо учитывать также степени свободы колебательного движения.
Независимо от общего числа степеней свободы молекул три степени свободы всегда поступательные. Ни одна из поступательных степеней свободы не имеет преимущества перед другими, поэтому на каждую из них приходится в среднем одинаковая энергия, равная 1/3 значения <w0> в (7.18):
<w0>= 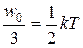 . (11.1)
. (11.1)
Дата добавления: 2015-10-05; просмотров: 1353;
