Органических молекул
Молекулярный азот представляет собой чрезвычайно инертное соединение, расщепление молекулы N2 требует больших затрат энергии. Из всех населяющих Землю организмов ферментативную фиксацию азота осуществляют лишь некоторые прокариоты. Данный процесс в их клетках катализируется нитрогеназной системой и осуществляется в процессе, который можно описать общим уравнением:
Нитрогеназная система бактерий локализуется во впячиваниях плазматической мембраны и состоит из двух компонентов: железосерного белка (4Fe 4S2-) и молибдоферредоксина (белок, содержащий молибден и железо). На одну молекулу молибдоферредоксина (MoFe) в активной нитрогеназной системе приходится 2 молекулы железосерного белка. Вспомогательными компонентами, участвующими в переносе электронов на нитрогеназную систему, служат флавиновые кофакторы и ферредоксин. Роль первичного донора электронов в этом процессе обычно выполняет NADPH.
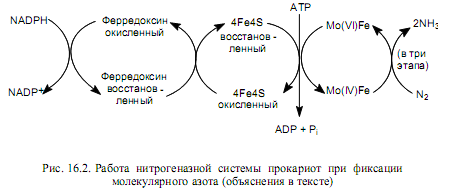
Процесс переноса электронов на молекулярный азот (рис. 16.2) осуществляется следующим образом: донор электронов восстанавливает ферредоксин, который самостоятельно либо через флавин переносит электроны на железосерные центры нитрогеназной системы. Затем АТР связывается с железосерными белками и сдвигает их окислительно-восстановительный потенциал с–0,29В до –0,4В путем изменения конформации белка. Подобное увеличение восстановительной способности железосерных белков позволяет им переносить электроны на молибдоферредоксин. На следующей стадии гидролизуется АТР, восстанавливается MoFe и нитрогеназная система диссоциирует на компоненты. Считается, что перенос пары электронов от восстановленной формы железосерных белков к молибдоферредоксину сопряжен с гидролизом четырех молекул АТР.
Восстановление молибдоферредоксина связано с переходом атома молибдена из окисленного состояния Мо(VI) в восстановленное Мо(IV), от которого электроны переносятся непосредственно на N2. Для полного восстановления молекулы азота до двух молекул NH3 требуется три последовательных 2- электронных перехода, которые будут сопряжены с гидролизом 12 (4х3) молекул АТР.
На симбиотическую азотфиксацию, в которой кроме нитрогеназной системы бактерий принимают участие и некоторые структуры растений, расходуется энергия, запасенная обоими организмами. Есть сведения, что в этом процессе потребляется до пятой части всей энергии, запасенной растением.
Нитрогеназная система восстанавливает не только молекулярный азот, но и ацетилен, азид, закись азота, цианид, нитриты и протоны. Перенос части восстановительных эквивалентов на Н+ осуществляется нитрогеназной системой в побочной реакции, поэтому наряду с аммиаком при фиксации азота всегда образуется молекулярный водород.
Сильным ингибитором нитрогеназной системы является молекулярный кислород: в его присутствии основные компоненты системы быстро инактивируются. Поэтому фиксация азота осуществляется в анаэробных участках клеток. Например, у клубеньковых бактерий специальная форма гемоглобина (леггемоглобин) защищает нитрогеназную систему от молекулярного кислорода, а у цианобактерий эту роль выполняют стенки гетероцист.
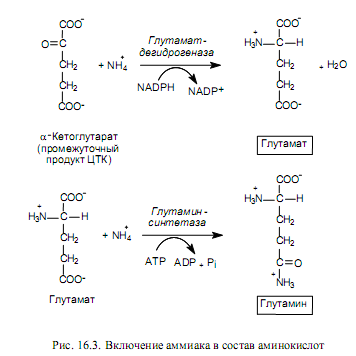
Следующей стадией включения азота в состав органических молекул является аминирование кетокислот, в результате которого возникают аминокислоты. Наиболее распространено восстановительное аминирование кетокислот. При этом основным продуктом, образующимся в данном процессе, является глутамат. Глутамат используется в качестве субстрата для включения еще одной молекулы аммиака, в результате чего синтезируется глутамин (рис. 16.3).
Перечисленные выше реакции имеют особое значение в биосинтезе аминокислот, поскольку катализирующие их ферменты наиболее активны, в результате чего данные процессы превращаются в основные пути включения аммиачного азота в состав аминокислот. В ходе последующих превращений аминогруппы глутамата и глутамина включаются в состав большинства других аминокислот. Подобные реакции носят название реакций трансаминирования.
Дата добавления: 2015-09-29; просмотров: 1065;
