Обчислення. Приклад 8. Знайти зміну ентропії при переході 6 г водню від об’єму 20 л під тиском 150 кПа до об’єму 60 л під тиском 100 кПа.
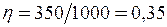 ;
;
T2 = (1 – 0,35)500 = 325 К;
Q2 = 1000 – 350 = 650 Дж.
Відповідь: 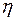 = 0,35; T2 = 325 К; Q2 = 650 Дж.
= 0,35; T2 = 325 К; Q2 = 650 Дж.
Приклад 8. Знайти зміну ентропії при переході 6 г водню від об’єму 20 л під тиском 150 кПа до об’єму 60 л під тиском 100 кПа.
Дано:  = 2·10-3 кг/моль; m =6·10-3 кг; p1 = 1,5·105 Па; V1 =
= 2·10-3 кг/моль; m =6·10-3 кг; p1 = 1,5·105 Па; V1 =
=2·10-2 м3; p2 = 105 Па; V2 = 6·10-2 м3; i = 5.
Знайти:  .
.
Розв’язок. Зміна ентропії термодинамічної системи визначається виразом
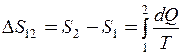 . (1)
. (1)
Тут dQ – приріст кількості теплоти, для якого перший закон термодинаміки можна записати в диференціальній формі
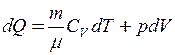 , (2)
, (2)
де CV – молярна теплоємність газу при постійному об’ємі
 . (3)
. (3)
Використовуючи рівняння Менделєєва-Клапейрона, температуру можна виразити через інші термодинамічні параметри
 . (4)
. (4)
Звідси знайдемо диференціал
 . (5)
. (5)
Після підстановки виразу (5) у (2), а потім у (1), одержимо
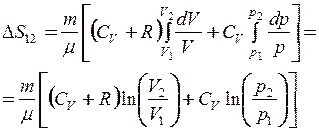 . (6)
. (6)
Остаточно, підставляючи (3) у (6), одержимо:
 . (7)
. (7)
Дата добавления: 2015-09-28; просмотров: 1665;
