Химические свойства. I Гидроксикислоты проявляют общие свойства спиртов и кислот
I Гидроксикислоты проявляют общие свойства спиртов и кислот. В зависимости от реагентов и условий проведения реакций взаимодействует ОН или -СООН группа или обе одновременно. Как кислоты они более сильны, чем соответствующие карбоновые кислоты (сказывается –I эффект ОН- группы).
П. Гидроксикислоты проявляют специфические свойства, которые обусловлены взаимным влиянием ОН- и СООН- групп.
1. Например, своеобразная реакция отщепления воды при нагревании.
Она позволяет отличить a-, b-, g- и другие гидроксикислоты.
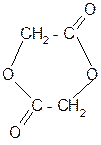
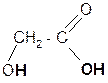 а)
а)
a t°

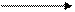
гидролиз + 2H2O
+ H+ или OH-
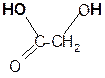
a лактиды
(циклические
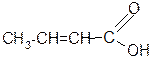
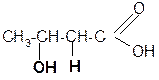 сложные эфиры)
сложные эфиры)
б) b a t°

-H2O
b -оксимасляная кротоновая кислота
кислота
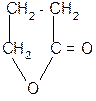 в) b a t°
в) b a t°
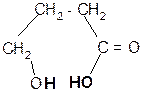
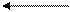
 + H2O
+ H2O
гидролиз
g H+
g-гидроксимасляная g - бутиролактон
кислота (ГОМК)
ГОМК обладает наркотическим действием, нетоксична, применяется в виде натриевой соли как снотворное средство и при неингаляционном наркозе при операциях.
г)
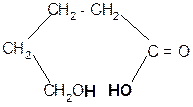
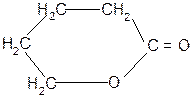 b a
b a
t°
 g + H2O
g + H2O
гидролиз
H+
d
d-гидроксивалериановая d - валеролактон
лактон
Лактиды и лактоны могут гидролизоваться в кислой среде с образованием исходных гидроксикислот.
2. Разложение a-гидроксикислот при нагревании в присутствии H2SO4:
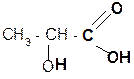 |
a t°, H2SO4
 CH3–CHO + HCOOH
CH3–CHO + HCOOH
Многоосновные кислоты ведут себя так же. Например,
а) при нагревании лимонная кислота будет вести себя как b-гидроксикислоты:
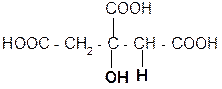 | |||
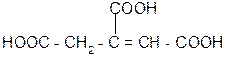 | |||
t°


-Н2О
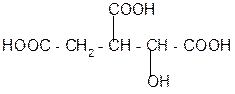 лимонная кислота цис-аконитовая к-та
лимонная кислота цис-аконитовая к-та
+ Н2О

против правила
Марковникова
изолимонная кислота
б) при действии H2SO4 и нагревании она ведет себя как a-гидроксикислота, т.е. разлагается с выделением муравьиной кислоты:
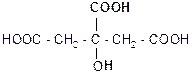
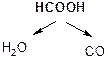
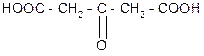 t°, H2SO4
t°, H2SO4
 +
+
ацетондикарбоновая




 кислота
кислота
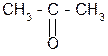 2СO2 +
2СO2 +
Таблица 1
Гидрокси – и оксоальдегиды и кетоны
| Формула | Тривиальное название | ИЮПАК – номенклатура | Местонахождение в природе и биологическая роль |
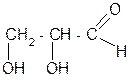 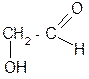
| Гликолевый, или гидроксиуксусный альдегид | 2– гидроксиэтаналь | Предшественник гликолевой кислоты |
| Глицериновый альдегид | 2,3–дигидрокси-пропаналь | Стандарт конфигурации всех «хиральных» соединений: гидрокси- и аминокислот, углеводов и др. | |
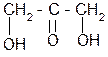
| Дигидроксиацетон | 1,3 – дигидрокси-2-пропанон | В виде фосфорно-кислого эфира встречается как промежуточный продукт при окислении глюкозы в организме |
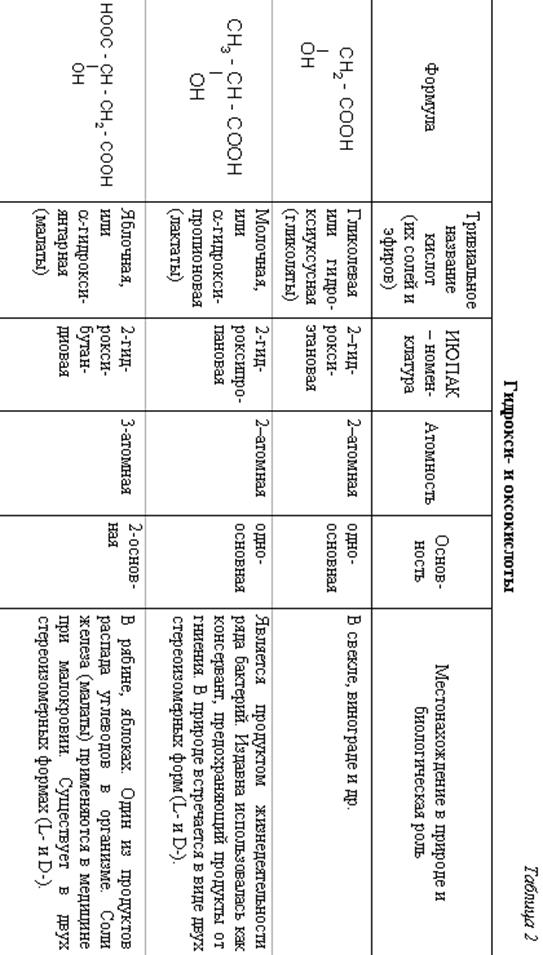
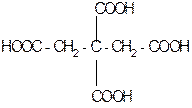 Продолжение таблицы 2
Продолжение таблицы 2
| Формула | Тривиальное Название кислот (их солей и эфиров) | ИЮПАК-номенклатура | Атомность | Основность | Местонахождение в природе и биологическая роль |
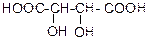
| Винная (виноградная), или a,b-дигидрокси янтарная кислота (тартраты) | 2,3-дигидрокси бутандиовая кислота | 4-х атомная | 2х основная | Содержится в виноградном соке. Является продуктом жизнедеятельности бактерий. Применяется как консервант в пищевой промышленности, в красильном деле. Соли (тартраты) применяются в радиотехнике (пьезокристаллы) и в биохимическом анализе в виде Фелинговой жидкости для обнаружения альдегидов. Существует в трех стереоизомерных формах (L-, D- и мезо-) |
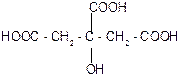
| Лимонная , или b-гидрокси-b-карбокси-глутаровая (цитраты) | 3-гидрокси-3-карбоксипентан диовая | 4-х атомная | 3-х основная | Содержится в лимонах, апельсинах, винограде, в листьях махорки. Играет важную роль в ЦТК. Соли (цитраты) применяются для консервирования донорской крови, соли железа – при малокровии. |
Дата добавления: 2015-09-28; просмотров: 2005;
