Строение атома углерода
В настоящее время органическую химию рассматривают как химию соединений углерода, но, отдавая дань уважения истории, по-прежнему продолжают называть ее органической химией. Поэтому так важно более подробно рассмотреть строение атома этого элемента, характер и пространственное направление образуемых им химических связей.
Атом углерода состоит из ядра, имеющего положительный заряд +6 (так как содержит шесть протонов), и электронной оболочки, на которой находятся шесть электронов, расположенных на двух энергетических уровнях (слоях):
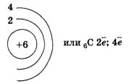
Реальное строение атома углерода гораздо сложнее, чем представлено на приведенной схеме.
Дело в том, что «живущий» в пространстве вокруг ядра электрон обладает одновременно свойствами и частицы (имеет массу 1/1840 от массы протона или нейтрона), и волны (способен к огибанию препятствий — дифракции, характеризуется определенной амплитудой, длиной волны, частотой колебаний и т. д.). Нельзя точно определить положение электрона в пространстве вокруг ядра. Поэтому говорят о большей или меньшей вероятности пребывания электрона в данной области пространства. Если бы мы могли сфотографировать атом и на снимке положение электрона отражалось бы в виде точки, то при наложении огромного числа таких снимков мы получили бы картину электронного облака. Чем больше плотность этого облака, тем с большей вероятностью электрон находится в этой области. Пространство вокруг ядра, в котором заключено 90% электронного облака, называется орбиталью. Это означает, что 90% времени электрон находится в этом ограниченном пространстве. В дальнейшем мы будем понимать термины «орбиталь» и «облако» как равноценные.
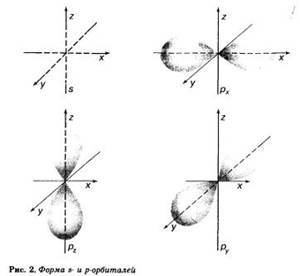
Атом углерода имеет два вида орбиталей: s-орбитали сферической формы и р-орбитали в форме гантели или объемной восьмерки (рис. 2).
Эти орбитали отличаются друг от друга не только формой, но и удаленностью от ядра атома. Чем более удалена от ядра орбиталь, тем большую энергию имеет электрон на этой орбитали. Энергия электрона — важнейшая характеристика его состояния. Причем, и это очень важно, энергия электрона в атоме может принимать только определенные значения, а сам электрон может занимать орбиталь на определенном расстоянии от ядра. Эти орбитали отличаются запасом (уровнем) энергии.
Чтобы различать энергетические уровни, их нумеруют в порядке удаления от ядра. Ближайший к ядру — первый (1), затем второй (2) и т. д.
В атоме углерода первый уровень составляет одна s-орбиталь, на которой находятся два электрона. Второй энергетический уровень атома углерода также содержит s-орбиталь, но большего размера, так как запас энергии электронов на ней выше, чем у электронов первого уровня, а также три р-орбитали. Это гантелеобразные орбитали одного размера, которые взаимно перпендикулярны, подобно осям координат х, у и z (см. рис. 2). Каждую орбиталь могут занимать два электрона, но с противоположными значениями спинов.
Спин (от англ. to spin — вращаться) — это собственный магнитный момент электрона (при введении понятия «спин» в 1925 г. предполагали, что магнитные свойства электрона как заряженной частицы вызваны его вращением вокруг собственной оси). Спин электрона появляется лишь при взаимодействии его с другими электронами и с внешним магнитным полем. Спин может иметь только два значения — положительное и отрицательное.
Чтобы представить расположение электронов в атоме, надо помнить, что каждый электрон занимает энергетически наиболее выгодное положение, при котором запас его энергии будет наименьшим. Он всегда стремится занять наиболее близкое к ядру положение и попасть на орбиталь более простой формы (например, сначала на s-, а уж потом на р-орбиталь). А если в пределах одного уровня имеется несколько одинаковых орбиталей, электроны размещаются вначале каждый на отдельной орбитали с одинаковыми спинами, а уж затем попарно, но с противоположными спинами. Соответственно электронная формула атома углерода будет иметь вид 1s22s22p2.
Очень часто строение электронных оболочек атомов отображают с помощью электронно-графических формул. В них каждая орбиталь обозначается одной клеткой; каждый электрон — стрелкой; направление стрелки соответствует направлению спина.
Изобразим электронно-графические формулы атомов углерода и водорода:
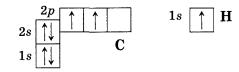
Валентность химического элемента чаще всего определяется числом неспаренных электронов. Атом углерода, как видно из электронно-графической формулы, имеет два неспаренных электрона, поэтому с их участием могут образоваться две электронные пары, осуществляющие две ковалентные связи. Однако в органических соединениях углерод не двух-, а всегда четырехвалентен. Это можно объяснить тем, что в возбужденном (получившем дополнительную энергию) атоме происходит распаривание 2s-электроновпереход одного из них на 2р-орбиталь:
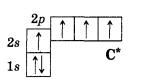
Такой атом имеет четыре неспаренных электрона и может принимать участие в создании четырех ковалентных связей.
Для образования ковалентной связи необходимо, чтобы орбиталь одного атома перекрывалась с орбиталью другого. При этом чем больше перекрывание, тем прочнее связь.
Химические связи, образующиеся в результате перекрывания электронных орбиталей вдоль линии связи, называются Ϭ-связями (сигма-связями).
Линия связи — прямая, соединяющая ядра атомов. Для s-орбиталей возможен лишь единственный способ перекрывания — с образованием Ϭ-связей.
р-Орбитали могут перекрываться с образованием Ϭ-связей, а также могут перекрываться в двух областях, образуя ковалентную связь другого вида — за счет «бокового» перекрывания:
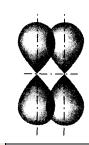
Химические связи, образующиеся в результате «бокового» перекрывания электронных орбиталей вне линии связи, т. е. в двух областях, называются π-связями (пи-связями).
| <== предыдущая лекция | | | следующая лекция ==> |
| Примеры происхождения фамилий от народного говора | | | Библиографический список 18 |
Дата добавления: 2015-09-11; просмотров: 6310;
