Примеры решения задач. Пример 32.1.Чему равна степень полимеризации изобутилена при получении полиизобутилена с молекулярной массой 56280?
Пример 32.1.Чему равна степень полимеризации изобутилена при получении полиизобутилена с молекулярной массой 56280?
Решение.Полиизобутилен (полимер) получается реакцией полимеризации изобутилена (мономера), реакция представлена схемой:




 СН3
СН3


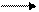 n CH2=C – CH3 – CH2 – C –
n CH2=C – CH3 – CH2 – C –
CH3 CH3 n
изобутилен полиизобутилен
Степень полимеризации nпоказывает, какое число молекул мономера вступает в реакцию полимеризации. Молекулярная масса изобутилена 56, средняя молекулярная масса полимера 56280. Следовательно, степень полимеризации
n = 56280 / 56 = 1005
Пример 32.2.Составить уравнение реакции сополимеризации бутена-1
 (CH2=CH–CH2–CH3) и стирола CH2=CH, если число молекул бутена-1 и
(CH2=CH–CH2–CH3) и стирола CH2=CH, если число молекул бутена-1 и
C6H5
стирола, входящих в состав макромолекул, находятся в соотношении 2:1.
Решение. Сополимеризация – это реакция полимеризации, в которой участвуют молекулы разных мономеров. В данном случае одним мономером является бутилен, другим стирол. Уравнение реакции сополимеризации имеет вид:
 n (CH2=CH–CH2–CH3 + CH2= CH + CH2=CH–CH2–CH3) ®
n (CH2=CH–CH2–CH3 + CH2= CH + CH2=CH–CH2–CH3) ®
C6H5
 ® (–CH2–CH–CH2–CH–CH2–CH–) n
® (–CH2–CH–CH2–CH–CH2–CH–) n


C2H5 C6H5 C2H5
Пример 32.3. Составить схему реакции поликонденсации ацетальдегида с фенолятом натрия, считая, что на 2 моль фенолята натрия приходится 1 моль ацетальдегида.
Решение.Поликонденсация – это реакция синтеза полимера из мономеров, имеющих две или несколько функциональные группы, сопровождающаяся образованием низкомолекулярных продуктов (H2O, NH3 и др.)
Данная реакция поликонденсации может быть представлена схемой:
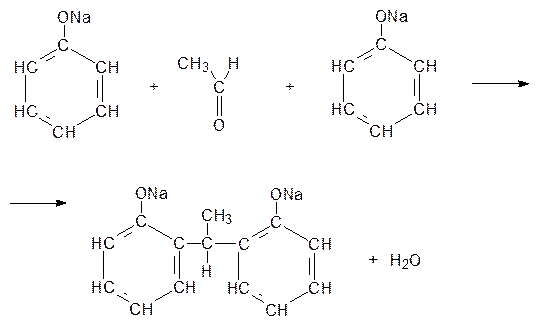
Задачи
№ 32.1. Для получения синтетического волокна “нитрон” в качестве мономера используют акрилонитрил CH2=CH–CN. Составить уравнение полимеризации этого мономера.
№ 32.2. Написать уравнение реакции полимеризации формальдегида и определить степень полимеризации в реакции получения полиформальдегида со средней молекулярной массой 45000. (Ответ: 1500).
№ 32.3. Написать уравнение реакции получения политетрафторэтилена (фторпласта-4) и определить среднюю молекулярную массу полимера, если степень полимеризации равна 1200. (Ответ: 120000).
№ 32.4. Составить уравнение реакции сополимеризации пропилена и изобутилена. Вычислить степень полимеризации, если полимер имеет молекулярную массу 160000. (Ответ: 1600).
№ 32.5. Составить уравнение реакции получения полихлорвинила, если в качестве исходного вещества взяли ацетилен.
№ 32.6. Муравьиный альдегид вступает в реакцию поликонденсации с мочевиной CO(NH2)2 и образует синтетическую карбамидную смолу. Написать уравнение реакции поликонденсации, считая, что на 2 моль мочевины необходим 1 моль формальдегида.
№ 32.7.Написать структурную формулу винилацетата. Привести схему полимеризации этого соединения.
№ 32.8. Привести схему сополимеризации акрилонитрила CH2=CH−СN и винилацетата.
№ 32.9. Привести схему получения полимера при реакции сополимеризации стирола и акрилонитрила.
№ 32.10. Написать структурную формулу метакриловой кислоты. Какое соединение получается при взаимодействии ее с метанолом? Написать уравнение реакции. Составить схему полимеризации образующегося продукта.
№ 32.11. Составить схему поликонденсации адипиновой кислоты C4H8(COOH)2 и гексаметилендиамина (NH2)2(CH2)6 .
№ 32.12. Как можно получить винилхлорид, имея карбид кальция, хлорид натрия, серную кислоту и воду? Написать уравнения соответствующих реакций. Составить схему полимеризации винилхлорида.
№ 32.13. Полимером какого непредельного диенового углеводорода является натуральный каучук? Написать структурную формулу этого углеводорода и реакцию его полимеризации.
№ 32.14. Составить схему сополимеризации бутадиена и стирола.
№ 32.15. Для получения синтетического волокна “энант” в качестве мономера используют аминоэнантовую кислоту NH2–(CH2)6–COOH. Составить схему поликонденсации аминоэнантовой кислоты.
№ 32.16. Составить схему сополимеризации изопрена и изобутилена.
№ 32.17. Написать уравнение реакции поликонденсации карбамида CO(NH2)2 с уксусным альдегидом, исходя из того, что с каждыми 3 моль карбамида вступают в реакцию 2 моль альдегида.
№ 32.18. При взаимодействии этилакриловой кислоты CH2=C(C2H5)–COOH с пропиловым спиртом C3H7OH образуется пропилэтилакрилат. Написать реакцию его получения и полимеризации. Какая масса полимера получится в результате реакции, если степень полимеризации равна 32? (Ответ: 4992).
№ 32.19. Написать уравнение реакции получения метилового эфира метакриловой кислоты и реакцию полимеризации его в полиметилметакрилат. Определить среднюю молекулярную массу полимера, если степень полимеризации равна 150. (Ответ: 13200).
№ 32.20. Волокно “лавсан” является продуктом поликонденсации терефталевой кислоты C6H4(COOH)2 и этиленгликоля. Соотношение между числом молекул терефталевой кислоты и этиленгликоля 2:1. Изобразить строение структурного звена этого полимера.
Лабораторная работа 33
Качественный анализ металлов
Цель работы: изучить качественные реакции на катионы металлов.
Задание: перевести исследуемые металлы в растворимое состояние и доказать наличие катионов определенных металлов с помощью специфическх качественных реакций. Выполнить требования к результатам работы, оформить отчет, решить задачу.
Качественный анализ – это совокупность химических, физико-химических и физических методов, применяемых для обнаружения компонентов, входящих в состав анализируемого вещества или смеси веществ. Методы качественного анализа в водных растворах сводятся к проведению химических реакций между ионами анализируемого вещества и прибавленных к ним реагентов (реактивов). Обычно проводят характерные реакции, которые могут быть замечены по какому-либо внешнему эффекту, например по образованию осадков, выделению газа, изменению окраски раствора или осадка и т.д.
Реагенты, применяемые в качественном анализе, делятся на групповые и специфические.
Специфическими реагентами называются такие реагенты, которые дают в определенных условиях характерную реакцию только с одним каким-либо ионом. Например, реактивом на ион Fe3+ является раствор гексацианоферрата (II) калия (желтая кровяная соль), который образует с катионом Fe3+ темно-синий осадок берлинской лазури:
4FeCl3 + 3K4[Fe(CN)6] = Fe4[Fe(CN)6]3↓ + 12KCl
Также для обнаружения ионов Fe3+ используется роданид аммония (NH4SCN) или калия (KSCN), который образует с катионом Fe3+ роданид железа Fe(SCN)3 кроваво-красного цвета.
Групповыми реагентами называются такие реактивы, которые дают аналогичные реакции с несколькими ионами. Ионы, одинаково относящиеся к групповому реагенту, называются ионами одной аналитической группы.
Существуют различные аналитические классификации катионов по группам. Для идентификации с помощью образования малорастворимых соединений наиболее распространенными являются кислотно-основная и сероводородная.
Кислотно-основная классификация основана на использовании в качестве групповых реагентов водных растворов кислот и щелочей. По этой классификации групповым реагентом на катионы Ca2+, Sr2+, Ba2+, Pb2+ является раствор серной кислоты H2SO4, реже – растворимые сульфаты Na2SO4, K2SO4, (NH4)2SO4. Названные катионы образуют с групповым реагентом нерастворимые сульфаты МSO4 белого цвета.
Сероводородная классификация базируется на использовании групповых реагентов: растворов HCl; H2S; (NH4)2S и (NH4)2CO3.
Для ионов Ag+, Pb2+, Hg2+ групповым осадителем служит HCl (образуются нерастворимые хлориды белого цвета); для ионов Ca2+, Sr2+, Ba2+ – (NH4)2CO3 (получаются нерастворимые карбонаты МСО3 белого цвета); для ионов Al3+, Cr3+, Fe3+, Fe2+, Mn2+, Co2+, Ni2+, Zn2+, Pb2+, Cd2+ и др. – (NH4)2S. При действии группового реагента на ионы Fe2+, Co2+, Ni2+, Pb2+, Сu2+ образуются нерастворимые сульфиды черного цвета, сульфид цинка ZnS белого цвета, CdS − желтый. Сульфиды алюминия, хрома (III), железа (III) подвергаются гидролизу, поэтому в водном растворе не образуются. Вместо сульфидов выделяются продукты их гидролиза − гидроксиды этих металлов и сероводород.
Дата добавления: 2015-09-11; просмотров: 9232;
