Ковалентний зв’язок.
У разі утворення ковалентного зв’язку між атомами з’являються спільні електронні пари з електронів, які раніше належали окремим атомам. Ці спільні електронні пари сполучених атомів певною мірою належать кожному з них. Потенціальна енергія системи атомів, що взаємодіють, у цьому разі зменшується.
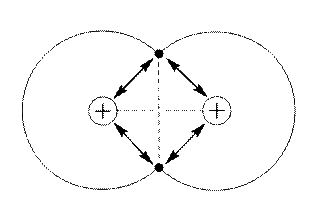
Сили притягання ( 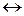 ) і відштовхування
) і відштовхування 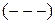 , які діють в молекулі водню.
, які діють в молекулі водню.
Між ядрами, електронами і сусідніми ядрами та електронами існують різні взаємодії.
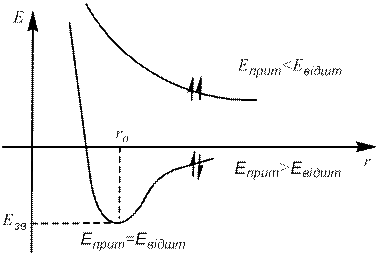
У разі, коли напрямки орієнтації спінів збігаються (спіни паралельні), зближення атомів супроводжується зростанням енергії – хімічний зв’язок не виникає. У разі протилежно спрямованих спінів зближення атомів до відстані 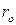 супроводжується зменшенням енергії; за
супроводжується зменшенням енергії; за 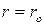 система має найменшу потенціальну енергію і перебуває в найстійкішому стані. Подальше зближення атомів спричинює різке зростання енергії системи.
система має найменшу потенціальну енергію і перебуває в найстійкішому стані. Подальше зближення атомів спричинює різке зростання енергії системи.
При утворенні хімічного зв’язку відбувається взаємопроникнення (перекривання) електронних хмар. Внаслідок цього густина негативного електричного заряду у між’ядерному просторі зростає. Ядра атомів притягуються до області перекривання орбіталей.
Такий зв’язок називається ковалентним. Він є двохелектронним та двох центровим.
Дата добавления: 2015-09-02; просмотров: 656;
